摘要
使用腐蚀失重、X射线衍射(XRD)、扫描电子显微镜与能谱(SEM-EDS)等手段研究了干湿交替环境中MgCl2对锌腐蚀行为的影响。结果表明,MgCl2对锌的腐蚀有显著的抑制作用;在沉积NaCl条件下锌表面的腐蚀产物为Zn5(OH)8Cl2·H2O、Zn4CO3(OH)6·H2O和Zn(OH)2,而在沉积MgCl2条件下锌表面的腐蚀产物只有Zn5(OH)8Cl2·H2O。在干湿交替环境中MgCl2对锌腐蚀行为的影响主要是Mg2+与氧还原反应产生的OH-结合使阴极区的pH值降低造成的。
关键词: 材料失效与保护 ; 大气腐蚀机制 ; 室内模拟加速腐蚀实验 ; MgCl2 ; 锌
锌是一种用途很广的结构金属,其生产和消耗量都很大[1]。锌的价格较低且具有出色的耐蚀性,主要用于防护钢铁材料的腐蚀。大气腐蚀是锌常见的一种腐蚀,是发生在薄液膜下的电化学腐蚀,因此受沉积在金属表面的各种吸湿无机盐类的影响[2,3,4,5,6,7]。以往大部分关于锌在沉积各种无机盐条件下的大气腐蚀机制研究,大多关注Cl-离子或SO42-离子等阴离子[3,4,8,9]。其主要原因是,阴离子经常参与腐蚀产物的形成以及Cl-离子等对金属很强的侵蚀性[10,11,12,13]。但是,阳离子对无机盐在金属表面的吸湿性、水解特性、表面液膜pH的影响以及参与形成腐蚀产物等因素也不可忽视。
在中国西部盐湖地区,MgCl2是影响金属大气腐蚀的一种重要腐蚀介质。Wang等[14]研究了耐候钢在中国青海盐湖大气环境的腐蚀演化过程,发现腐蚀产物中有特殊的含镁腐蚀产物Mg4Fe(OH)8OCl·4H2O。这种产物因其晶体结构的特殊性能吸附Cl-离子,使耐候钢在该环境下的耐候性降低。Wang等[15]研究2024-T3铝合金在中国西部盐湖大气环境下的腐蚀行为时发现了显著的点蚀、晶间腐蚀和应力腐蚀开裂,并发现了含镁腐蚀产物([Mg1-xAlx(OH)2]x+Clx-·mH2O)。他们将这些腐蚀现象归结于MgCl2·6H2O盐类在铝合金表面的沉积和干燥气候。目前虽然已有关于锌在西部盐湖环境腐蚀行为的研究报道[16]并表明Mg2+对锌的腐蚀有一定的影响,但是并没有深入探讨MgCl2影响锌大气腐蚀的机制。因为影响户外大气暴晒研究的因素较多,难以判断单因素的影响作用。鉴于此,本文模拟户外干湿交替环境研究MgCl2对锌腐蚀行为的影响机制。
1 实验方法
1.1 实验用材料
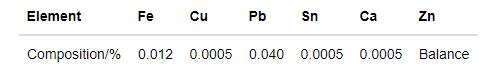
选用轧制纯锌片(纯度99.9%)作为实验材料,其成分列于表1。样品的尺寸为50 mm×25 mm×3 mm,用砂纸将测试面充分打磨。将试样清洗后滴上酒精吹干,在干燥箱中干燥2 d后取出并称量其初始质量。
表1 实验中纯锌试样的成分(质量分数)
1.2 锌的大气腐蚀实验
鉴于锌的大气腐蚀中最常见的腐蚀介质是NaCl[2,3,6,7,17],实验中将NaCl作为对比实验组的腐蚀介质,对比研究MgCl2对锌腐蚀行为的影响机制。因为同时保持阳离子沉积速率与阴离子沉积速率相等是不可能的,将实验分为三组:
(1) NaCl组(简称Na组),沉积速率为2 μmol·cm-2·d-1;
(2) MgCl2第一组(简称Mg1组),沉积速率为1 μmol·cm-2·d-1,Cl-离子的沉积速率与Na组Cl-离子的相同;
(3) MgCl2第二组(简称Mg2组),沉积速率为2 μmol·cm-2·d-1,Mg2+离子的沉积速率与Na组Na+离子的相同。
使用Weiss-Voetsch高低湿腐蚀试验箱进行腐蚀试验。实验前在每个样品的表面用微注射器沉积10 μL·cm-2的NaCl或MgCl2溶液(溶剂为水与酒精的混合液体,体积比为1:3),均匀铺开后放在35 ℃加热箱里将其干燥,最后将试样水平放置在腐蚀试验箱内进行实验。每3 h为干湿交替的一个周期,其中湿润1 h,湿度为80% RH,温度为30℃;干燥2 h,湿度为20% RH,温度为30 ℃。(由于MgCl2潮解的相对湿度为35% RH,所以干湿交替首先从湿润过程开始。)每腐蚀24 h将试样取出一次,并按照上述步骤进行涂盐干燥,然后再放入试验箱进行腐蚀实验。总腐蚀时间为528 h。
1.3 腐蚀结果的表征
1.3.1 质量损失
去除试样表面的腐蚀产物,使用的除锈液是将100 g NH4Cl溶解在1000 mL去离子水中制成的。质量损失的称量:(1)先将除锈液放在恒温水浴中加热到70℃,然后将腐蚀试样放入并静置5 min;(2)将试样取出放入盛有蒸馏水的烧杯中超声清洗5 min;(3)将试样取出用蒸馏水清洗后再用酒精浸润,吹干后放入干燥器中静置2 d。(4)将试样从干燥器中取出用精度为0.1 mg的天平称量,取3块平行试样质量损失数据的平均值。
1.3.2 XRD谱
XRD仪的型号为Rigaku-D/Max-2500PC。使用Cu靶,仪器工作参数为50 kV - 250 mA,对腐蚀表面的扫描速度为2°·min-1,扫描范围为10°~90°。
1.3.3 SEM-EDS观察
将用环氧树脂封装的试样截面打磨到2000 #砂纸,然后用粒度为1.5 μm的金刚石抛光膏抛光。使用型号为XL30-FEG的SEM-EDS观察分析试样的形貌和元素分布,电子束电压为25 kV,观察距离约为10 mm。
2 结果和讨论
2.1 腐蚀质量损失
锌的腐蚀动力学可由腐蚀质量损失表征。为了更清晰直观的描述腐蚀程度,用腐蚀厚度损失表示质量损失。锌试样的腐蚀厚度损失(μm)可表示为
![]()
式中Wt为腐蚀质量损失(g),ρ为锌的密度(7.14 g·cm-3),S为锌试样的涂盐面积。
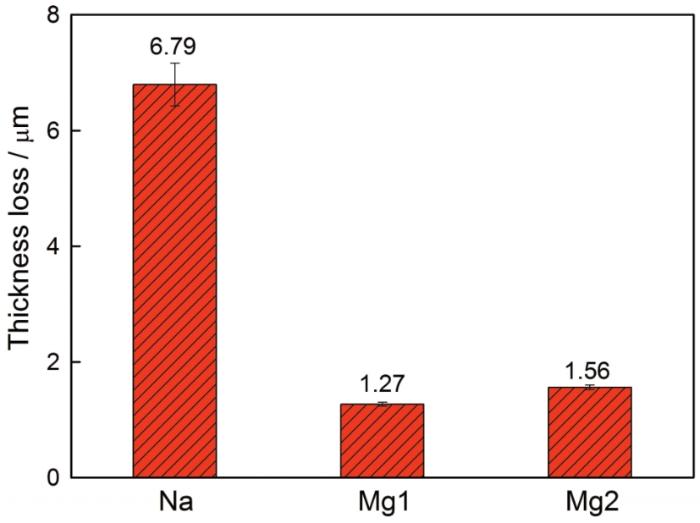
图1 沉积不同盐的锌腐蚀528 h后的腐蚀失厚
图1给出了锌腐蚀528 h后的腐蚀质量损失。可以看出,不论是锌在沉积等量Cl-离子的条件下,还是在沉积等量阳离子的条件下,Na组实验中锌的腐蚀质量损失均大于Mg组中锌腐蚀质量损失的4倍,表明在该模拟环境下MgCl2显著地抑制了锌的腐蚀。图上还可以看到,Mg2组比Mg1组锌的腐蚀质量损失稍大,表明MgCl2的沉积速率越高锌的腐蚀越快。
2.2 腐蚀产物
为了进一步探究MgCl2对锌腐蚀过程的影响,对腐蚀试样表面的腐蚀产物进行了鉴定。由于试样表面残留沉积的氯化盐,进行XRD检测前将试样放入100 mL蒸馏水中浸泡1 min,取出后分别用蒸馏水和酒精冲洗,吹干后放入干燥器中静置,24 h后再进行XRD分析。图2给出了不同实验组中锌表面腐蚀产物的XRD谱。腐蚀产物Zn5(OH)8Cl2·H2O的最强峰位于11.2°,表明该产物在Na组、Mg1组和Mg2组中均有生成,且在Mg1组和Mg2组中Zn5(OH)8Cl2·H2O是唯一检测到的不可溶腐蚀产物。腐蚀产物Zn4CO3(OH)6·H2O的最强峰位于12.8°,腐蚀产物Zn(OH)2的最强峰位于18.3°。Na组的XRD谱表明,除了腐蚀产物Zn5(OH)8Cl2·H2O,在锌表面还生成了Zn4CO3(OH)6·H2O和Zn(OH)2。此外,腐蚀产物的峰形都很尖,表明其主要是晶体。
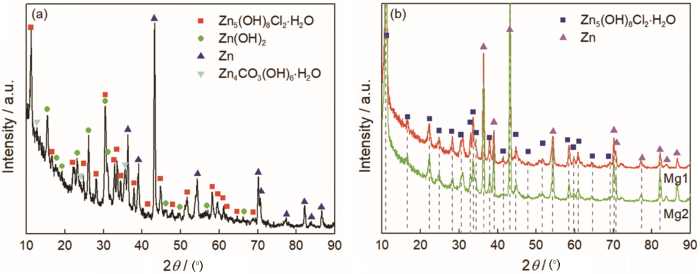
图2 锌腐蚀528 h后腐蚀产物的XRD谱
表2 锌腐蚀528h后蚀产物的XRD检测结果
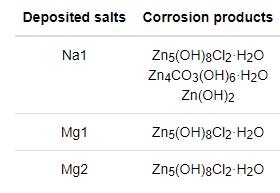
各组XRD腐蚀产物的检测结果列于在表2。锌在沉积NaCl条件下的腐蚀产物明显不同于沉积MgCl2条件下的腐蚀产物,说明MgCl2抑制了腐蚀产物Zn4CO3(OH)6·H2O和Zn(OH)2的生成。
2.3 锌腐蚀试样的形貌
2.3.1 表面形貌
图3给出了浸水处理后各组锌腐蚀试样表面的SEM照片和EDS能谱(试样表面进行了喷碳处理,故EDS结果不能分辨含碳产物的分布情况,图中×标记位置为EDS检测位置)。由图3可见,在Na组锌试样表面有一些山脊状腐蚀产物(图3a),山脊上分布一些针片状的腐蚀产物,腐蚀产物中含有Zn、O元素(图3c)。相对而言,Mg1组和Mg2组锌试样表面的腐蚀产物较平坦、分布均匀(图3d和图3g),表层腐蚀产物层均为针片状(图3e和图3h),腐蚀产物中含有Zn、O、Cl和Mg元素(图3f和3i)。
2.3.2 截面形貌
图4给出了各组锌腐蚀试样截面形貌的SEM-EDS结果(试样表面进行了喷碳处理,故EDS结果不能分辨含碳产物的分布情况,图中×标记位置为EDS检测位置)。由图4可见,Na组腐蚀产物(图4a)具有双层结构,上层的腐蚀产物层呈暗灰色,下层的腐蚀产物呈现亮灰色。上层暗灰色腐蚀产物层含Zn、O 2种元素(图4d和4e),与表面元素分析结果一致;下层亮灰色腐蚀产物层含Zn、O和Cl 3种元素。与Na组相比,Mg1组(图4b)和Mg2组(图4c) 的腐蚀产物为单层结构,含有Zn、O、Cl和Mg 4种元素(图4f和4g)。

图3 锌腐蚀528 h后表面的SEM-EDS结果
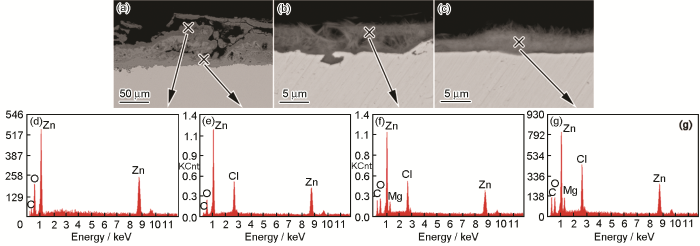
图4 锌腐蚀528 h后的截面SEM-EDS结果
根据腐蚀产物的表面和截面形貌的SEM-EDS、XRD分析,在Na组中锌试样表面形成的腐蚀产物为双层结构,腐蚀产物Zn(OH)2或Zn4CO3(OH)6·H2O主要分布在表层腐蚀产物中,而Zn5(OH)8Cl2·H2O主要分布在内层腐蚀产物中;与Na组不同,Mg组锌试样表面形成的腐蚀产物为单层结构,主要由Zn5(OH)8Cl2·H2O构成,还含有Mg元素。
2.3.3 除去腐蚀产物后的表面形貌
图5给出了各组锌腐蚀试样除去腐蚀产物后表面的SEM照片。由图5可见,在Na组锌试样表面有成片的点蚀坑,表明腐蚀较严重;而在Mg1组锌试样表面只有零星分布的小点蚀坑,表明腐蚀比较轻微;相对而言,Mg2组比Mg1组锌表面点蚀坑明显增多,点蚀坑尺寸较小且不密集,腐蚀程度居中。Na组锌的腐蚀质量损失比Mg1组和Mg2组都大4倍以上,Mg2组比Mg1组锌腐蚀质量损失稍大,与腐蚀形貌的结果一致。

图5 锌试样表面去除腐蚀产物后的SEM照片
2.4 MgCl2对锌大气腐蚀机制的影响
锌的大气腐蚀是一个电化学腐蚀过程。其阳极反应为锌的阳极溶解[9,18](方程2),阴极反应一般为氧还原反应[4,9](方程3):
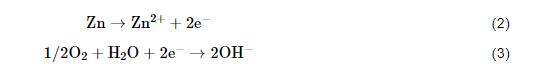
氧还原反应产生的OH-离子向阳极区迁移,锌阳极溶解产生的Zn2+向阴极区迁移,两者结合生成腐蚀产物Zn(OH)2。当锌表面存在NaCl颗粒时表面液膜中的Cl-离子向阳极区迁移,反应生成腐蚀产物Zn5(OH)8Cl2·H2O(方程4):
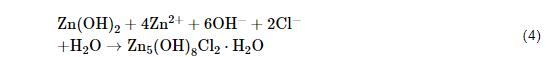
CO2是锌大气腐蚀时生成腐蚀产物Zn4CO3(OH)6·H2O的反应物[19,20]。CO2优先在大气腐蚀过程中的阴极区溶解,因为它溶解生成H+,而阴极区吸氧反应生成的OH-与之中和促进更多的CO2溶解(方程5、6和7)。随着反应的进行,在大气腐蚀反应的阴极区Zn(OH)2转化为Zn4CO3(OH)6·H2O(方程8):
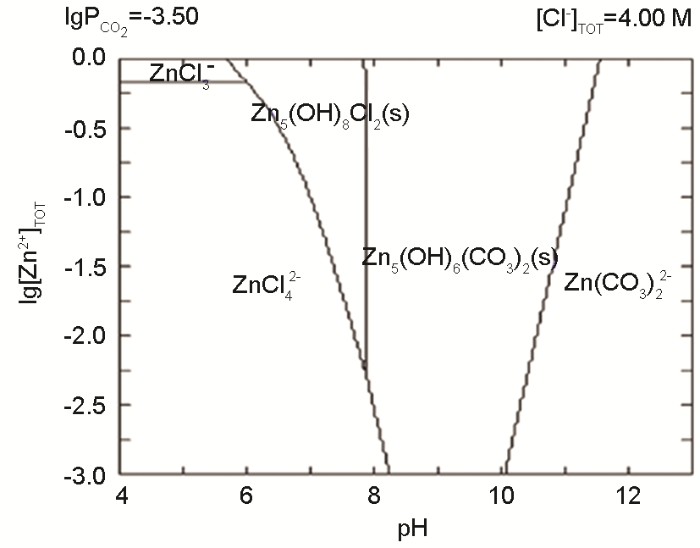
图6 锌的2价腐蚀产物在浓度为4 mol·L-1的Cl-离子溶液中腐蚀产物的优势区
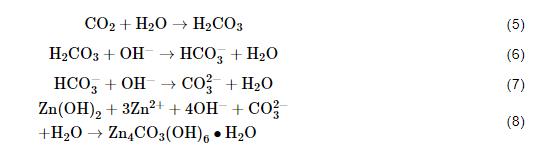
当锌表面沉积MgCl2时,XRD检测表明其表面的腐蚀产物仅为Zn5(OH)8Cl2·H2O,说明MgCl2能抑制Zn4CO3(OH)6·H2O和Zn(OH)2的生成。图6给出了锌二价腐蚀产物在4 mol·L-1的Cl-离子溶液中腐蚀产物的优势区图,其中温度为25℃、大气压强为1.013×105 Pa,空气中CO2浓度为350×10-6,Cl-离子浓度值是根据MgCl2溶液在80% RH时的理论平衡Cl-离子浓度设置的[21]。图中用腐蚀产物Zn5(CO3)2(OH)6替代了Zn4CO3(OH)6·H2O,因为后者是前者的亚稳相,随着时间的延长后者转化为前者[18]。表3给出了优势区图计算过程中使用到的反应式及其相应的平衡常数。从图6可见,腐蚀产物Zn5(CO3)2(OH)6的pH值比Zn5(OH)8Cl2·H2O的高,生成区间位于pH值8到11之间。因此可以认为,本文实验中的腐蚀产物Zn4CO3(OH)6·H2O更倾向于生成在锌大气腐蚀时的阴极区,而腐蚀产物Zn5(OH)8Cl2·H2O更倾向于生成在锌大气腐蚀时的阳极区。而MgCl2液膜中的Mg2+离子易与OH-离子结合生成Mg(OH)2沉淀(方程9)降低液膜的pH值[8,18,22],从而抑制了腐蚀产物Zn4CO3(OH)6·H2O的生成。同时,pH值的下降促进了腐蚀产物Zn5(OH)8Cl2·H2O的生成。因此,在Mg1组和Mg2组锌表面只检测到腐蚀产物Zn5(OH)8Cl2·H2O。
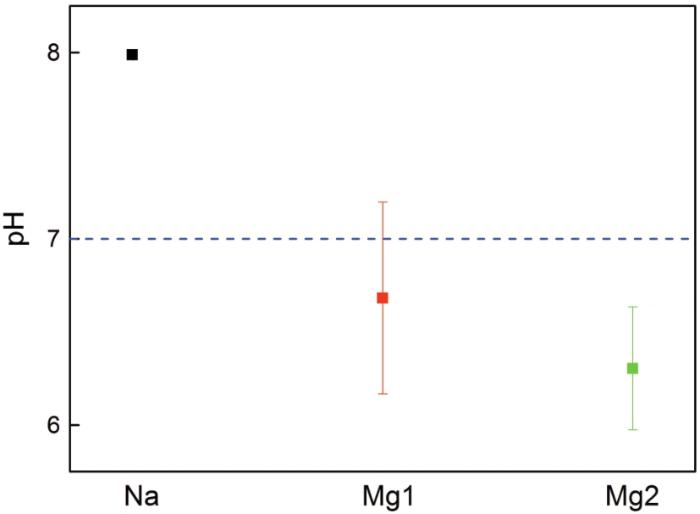
图7 腐蚀后锌试样浸泡液的pH值
图7给出了锌腐蚀试样在100 mL蒸馏水中浸泡1 min后溶液的pH值。图7表明,溶解Na组锌试样表面可溶性盐的浸泡液其pH值较高,溶液呈弱碱性;而溶解Mg组锌试样表面可溶性盐的浸泡液其pH值较低,溶液呈弱酸性。这个结果也佐证了上述推断。但是,在腐蚀产物中并没有检测到Mg(OH)2,可能转化为锌的其他腐蚀产物[8,18,22]。
![]()
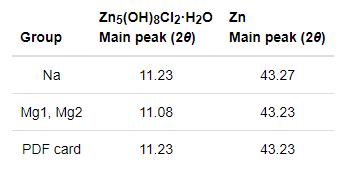
从图8可见,Mg1组和Mg2组中腐蚀产物Zn5(OH)8Cl2·H2O的衍射峰主峰均向左发生偏移。2θ角60°到62°之间的几处小峰也有不同程度的偏移(图8中右上角小图)。表4列出了腐蚀产物Zn5(OH)8Cl2·H2O和基体Zn的标准图谱主峰位置与检测主峰位置。由表4可知,基体Zn的衍射峰基本上没有偏移,说明在测量过程中Na组、Mg1组和Mg2组腐蚀产物图谱没有发生整体偏移。但是,腐蚀产物Zn5(OH)8Cl2·H2O的衍射主峰却向左偏移了0.15°。由布拉格衍射方程(方程10)可知,当入射X射线波长(方程10中λ)不变时,若同一组平行晶面衍射角(方程10中θ)减小,则其晶面间距(方程10中d)则相应增大。先前在Mg组腐蚀产物的XRD图谱中只检测到一种腐蚀产物Zn5(OH)8Cl2·H2O,但是EDS结果显示产物中含有Mg元素。由此可以推断,发生这种现象的原因可能是Mg原子替代了部分Zn原子进入到了腐蚀产物Zn5(OH)8Cl2·H2O中[8],使腐蚀产物Zn5(OH)8Cl2·H2O的晶格发生了畸变[22]。
表3 离子强度为0、温度为25℃时各反应式及其相应的平衡常数[18]

![]()
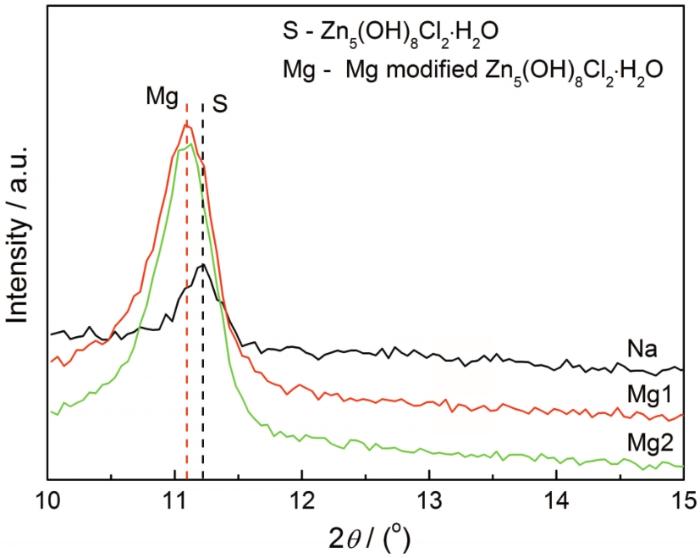
图8 XRD谱中锌腐蚀产物Zn5(OH)8Cl2·H2O峰的偏移
腐蚀质量损失结果表明,锌在Na组中的腐蚀失厚是Mg1和Mg2组的4倍以上。从盐的吸湿性角度看,MgCl2的潮解相对湿度为35% RH,NaCl的潮解相对湿度为75% RH,因此,在干湿交替过程中,在沉积MgCl2条件下锌试样的实际润湿时间比在沉积NaCl条件下的锌试样长。单从这个角度看,沉积MgCl2的锌的腐蚀质量损失应该大于沉积NaCl的锌的腐蚀质量损失。但是实际上,Mg1组和Mg2组锌的腐蚀质量损失比Na组锌的质量损失小很多。从腐蚀产物角度分析,当锌表面只覆盖腐蚀产物Zn5(OH)8Cl2·H2O(有可能是“Mg式Zn5(OH)8Cl2·H2O”)时锌的质量损失较小;而当锌表面覆盖有其他腐蚀产物Zn4CO3(OH)6·H2O和Zn(OH)2时锌的质量损失是前者的4倍以上。因此,腐蚀产物Zn5(OH)8Cl2·H2O(有可能是“Mg式Zn5(OH)8Cl2·H2O”)的形成是Mg1组和Mg2组中锌腐蚀质量损失较小的原因。
表4 不同组中腐蚀产物Zn5(OH)8Cl2·H2O的主峰位置与基体Zn主峰位置
综上所述,于NaCl相比,在干湿交替环境中MgCl2能抑制锌的腐蚀,其机制是:Mg2+离子能与锌阴极氧还原反应生成的OH-离子结合生成沉淀而降低该处液膜的pH,从而促进具有保护性的腐蚀产物Zn5(OH)8Cl2·H2O(有可能是“Mg式Zn5(OH)8Cl2·H2O”)在锌表面的均匀生成。
3 结论
(1) 不论是在沉积等量的Cl-离子条件下还是在沉积等量阳离子条件下,锌在沉积NaCl条件下的腐蚀质量损失均是沉积MgCl2条件下的4倍以上,在干湿交替环境中MgCl2能显著抑制锌的腐蚀。
(2) 锌在沉积NaCl条件下生成的腐蚀产物具有双层结构,有Zn5(OH)8Cl2·H2O、Zn4CO3(OH)6·H2O和Zn(OH)2;而锌在沉积MgCl2条件下生成的腐蚀产物为单层结构,只有Zn5(OH)8Cl2·H2O。
(3) MgCl2抑制锌腐蚀的机制为:Mg2+离子与锌阴极氧还原反应生成的OH-离子结合,生成的沉淀降低了该处液膜的pH值,从而促进了具有保护性的腐蚀产物Zn5(OH)8Cl2·H2O在锌表面的均匀生成。
参考文献
1 ZhangX G. Corrosion of zinc and its alloy [J]. Corros. Pro., 2006, 27(01): 41
1 章小鸽. 锌和锌合金的腐蚀 [J]. 腐蚀与防护, 2006, 27(01): 41
2 ChenZ Y, PerssonD, LeygrafC. Initial NaCl-particle induced atmospheric corrosion of zinc-effect of CO2 and SO2 [J]. Corros. Sci., 2008, 50(1): 111
3 ColeI S. Recent progress and required developments in atmospheric corrosion of galvanised steel and zinc [J]. Materials, 2017, 10(11): 1288
4 GraedelT E. Corrosion mechanism for zinc exposed to the atmosphere [J]. J. Electrochem. Soc., 1989, 136(4): C193
5 LiuY W, WangZ Y, CaoG W, et al. Study on corrosion behavior of zinc exposed in coastal-industrial atmospheric environment [J]. Mater. Chem. Phys., 2017, 198:243
6 NeufeldA K, ColeI S, BondA M, et al. The initiation mechanism of corrosion of zinc by sodium chloride particle deposition [J]. Corros. Sci., 2002, 44(3): 555
7 WallinderI O, LeygrafC. A critical review on corrosion and runoff from zinc and zinc-based alloys in atmospheric environments [J]. Corrosion, 2017, 73(9): 1060
8 ProsekT, ThierryD, TaxenC, et al. Effect of cations on corrosion of zinc and carbon steel covered with chloride deposits under atmospheric conditions [J]. Corros. Sci., 2007, 49(6): 2676
9 ShiY Y, ZhangZ, ZhangJ Q, et al. Review of atmospheric corrosion of zinc and zinc alloy [J]. J. Chin. Soc. Corros. Prot., 2005, 25(06): 373
9 施彦彦, 张昭, 张鉴清等. 锌及其合金的大气腐蚀研究现状 [J]. 中国腐蚀与防护学报, 2005, 25(06): 373)
10 PanC, HanW, WangZ Y, et al. Evolution of initial atmospheric corrosion of carbon steel in an industrial atmosphere [J]. J. Mater. Eng. Perform., 2016, 25(12): 5382
11 HaoX H, WangZ Y, WangC. Atmospheric corrosion of zinc at Hongyanhe nuclear power station [J]. Equipm. Environ. Eng., 2012, 9(3): 108
11 郝显赫, 王振尧, 汪川. 锌在辽宁红沿河核电站的大气腐蚀研究 [J]. 装备环境工程, 2012, 9(03): 108)
12 WangZ Y, YuG C, HanW. Atmospheric corrosion performance of zinc at several selected test sites in China [J]. Corros. Sci. Prot. Technol., 2003, 15(04): 191
12 王振尧, 于国才, 韩 薇. 我国若干典型大气环境中的锌腐蚀 [J]. 腐蚀科学与防护技术, 2003, 15(04): 191)
13 WangZ Y, YuG C, ZhengY P, et al. Investigation on interrelation of accelerated corrosion testing and atmospheric exposure of zinc [J]. J. Chin. Soc. Corros. Pro., 1999, 19(04): 48
13 王振尧, 于国才, 郑逸苹等. 锌的加速腐蚀与大气暴露腐蚀的相关性研究 [J]. 中国腐蚀与防护学报, 1999, 19(04): 48)
14 WangJ, WangZ Y, KeW. A study of the evolution of rust on weathering steel submitted to the Qinghai salt lake atmospheric corrosion [J]. Mater. Chem. Phys., 2013, 139(1): 225
15 WangB B, WangZ Y, HanW, et al. Atmospheric corrosion of aluminium alloy 2024-T3 exposed to salt lake environment in western China [J]. Corros. Sci., 2012, 59: 63
16 ZhangD, WangZ Y, ZhouY Z, et al. Initial corrosion behavior of galvanized steel in atmosphere by Qinghai Salt Lake [J]. Chin. J. Mater. Res., 2018, 32(04): 255
16 张 丹, 王振尧, 周永璋等. 镀锌钢在青海盐湖大气环境下的初期腐蚀行为研究 [J]. 材料研究学报, 2018, 32(04): 255)
17 YinQ, WangZ Y, PanC. Initial corrosion behavior of pure zinc in simulated tropical marine atmosphere [J]. Trans. Nonferrous Met. Soc. China, 2018, 28(12): 2582
18 LindstromR, SvenssonJ E, JohanssonL G. The influence of salt deposits on the atmospheric corrosion of zinc - The important role of the sodium ion [J]. J. Electrochem. Soc., 2002, 149(2): B57
19 FalkT, SvenssonJ E, JohanssonL G. The influence of CO2 and NaCl on the atmospheric corrosion of zinc - A laboratory study [J]. J. Electrochem. Soc., 1998, 145(9): 2993
20 LindstromR, SvenssonJ E, JohanssonL G. The atmospheric corrosion of zinc in the presence of NaCl the influence of carbon dioxide and temperature [J]. J. Electrochem. Soc., 2000, 147(5): 1751
21 TsutsumiY, NishikataA, TsuruT. Pitting corrosion mechanism of Type 304 stainless steel under a droplet of chloride solutions [J]. Corros. Sci., 2007, 49(3): 1394
22 HoskingN C, StromM A, ShipwayP H, et al. Corrosion resistance of zinc-magnesium coated steel [J]. Corros. Sci., 2007, 49(9): 3669
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。
-
标签: 材料失效与保护, 大气腐蚀机制, 室内模拟加速腐蚀实验, MgCl2, 锌

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414





