摘要
利用附着力测试、吸水率测试和电化学阻抗谱测试等手段,研究了淡水舱涂层在反渗透水、调质水、自来水等淡水以及盐水中的腐蚀失效行为。结果表明,自来水比盐水具有更快的渗透速度,导致涂层在淡水中会优先失效。淡水舱涂层在反渗透水、调质水和饮用水3种淡水中的腐蚀失效历程相同,根据电化学阻抗谱的变化特征可分为3个阶段:水的快速渗透、涂层/金属界面金属基体的腐蚀和涂层中颜填料对金属的缓蚀。
关键词: 涂层; 淡水; 腐蚀; 电化学阻抗谱
环氧树脂涂层因具有强的附着力、良好的力学性能和优异的耐腐蚀性能被广泛应用于金属表面的防护,环氧涂层的失效与外界离子的传输[1,2]、涂层从金属界面的剥离[3-5]密切相关,在一定程度上讲,涂层失效的本质是外界腐蚀介质通过涂层内部渗入到涂层/金属基体界面而使涂层丧失保护作用的过程。因此,涂层/金属界面的结合以及涂层对外界腐蚀介质的抵抗能力成为了决定环氧涂层寿命的两个重要因素,对于环氧涂层界面结合和致密性的改性[6-9]、环氧涂层的失效评价[10-16]引起了广泛关注。以上对于环氧涂层的研究所涉及的腐蚀介质多为含Cl-的盐水环境,对于环氧涂层在淡水环境中的腐蚀失效报道较少。
淡水舱涂层是保障海上淡水饮用安全和保持船体免受腐蚀的重要载体[17],了解不同淡水环境对涂层性能的影响对于淡水舱涂层的选择和设计具有重要的意义。本文将主要围绕涂层与金属基体的附着性能、水的传输行为和涂层致密性3个方面,对比研究淡水舱涂层在盐水和淡水中的腐蚀行为差异以及涂层在反渗透水、调质水和饮用水3种淡水环境中的腐蚀失效过程。
1 实验方法
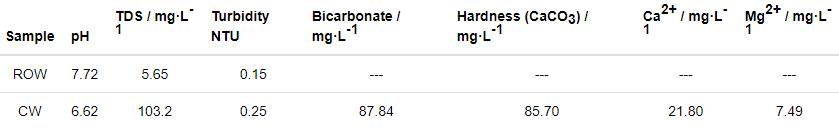
本工作研究对象为一种国产的无溶剂型环氧涂层,主要用于淡水舱的涂覆,实验基材为Q235钢板,表面经喷砂处理达到Sa2.5级,涂层喷涂厚度80~95 μm。所选择的溶液介质包括利用海水淡化技术处理得到的反渗透二级产水 (ROW),通过在反渗透水中加入50 mg/L MgCl2、35 mg/L CaCl2和90 mg/L NaHCO3所得的调质水 (CW),海水淡化处理后两种淡水中Cl-含量均小于0.02 mg/L,具体的性质如表1所示。除此之外,还引入了沈阳市的饮用水 (DW) 和3.5% (质量分数) NaCl (SW) 作为对比。
表1 两种淡水的性质
根据GB/T 5210-2006,采用PosiTest?AT-A全自动数字显示拉拔式附着力测试仪对在不同水溶液中分别浸泡0、240、480、720和1200 h的涂层样品进行了附着力测试,每个时间点测量6次,取6次测试的平均值作为该时间点的附着力值。
为了测试不同的水溶液介质在涂层中的传输行为,需制备涂层的自由膜样品,具体过程为将涂料均匀喷涂到硅胶板上,涂层厚度为约100 μm,涂层表干后将其从硅胶板上手工剥离,待其实干后,用裁刀将涂层裁成20 mm×20 mm的薄片,即为涂层自由膜样品,并记录每个样品的原始质量m0,涂层样品在浸泡t时刻的吸水率利用以下公式计算可得:
![]()
其中,Qt为涂层样品浸泡t时刻的吸水率,mt和m0为涂层样品浸泡t时刻及浸泡前的质量。
利用VersaSTAT V3F电化学工作站对浸泡不同时间的涂层样品进行了开路电位 (OCP) 和电化学阻抗谱 (EIS) 测试,其中待测样品为工作电极,铂片为对电极,饱和甘汞电极为参比电极。电化学阻抗谱测试前先进行10 min的开路电位扫描,待电位稳定后进行测试,频率测试范围105~10-2 Hz,正弦波扰动振幅为20 mV。
2 结果与讨论
2.1 淡水舱涂层在盐水和淡水中的失效机制
2.1.1 涂层附着性能
淡水舱涂层与金属基体界面的湿态附着力能直观地体现涂层在实际服役过程中的附着性能,利用拉开法分别测试了淡水舱涂层在盐水和饮用水中分别浸泡0、240、480、720和1200 h后的附着力,得到淡水舱涂层湿态附着力随时间的变化,如图1所示。可以看出,无论是在盐水中还是饮用水中,淡水舱涂层随浸泡时间的增加,附着力均没有下降的趋势。淡水舱涂层在两种溶液中湿态附着力随时间的变化趋势不同,在盐水中,其附着力表现为波浪式上升的趋势,1200 h浸泡后已由初始的约5 MPa增加到约8 MPa,在饮用水中,其附着力表现为先增加后降低的变化特征,1200 h浸泡后附着力与初始值基本一致。
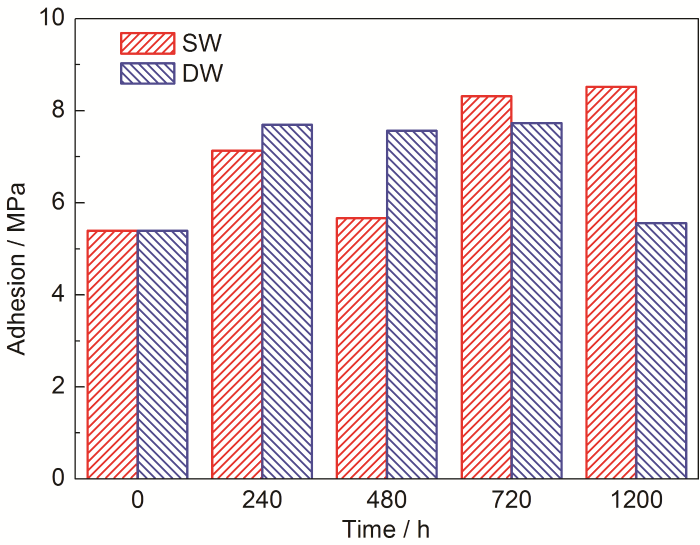
图1 淡水舱涂层在盐水和饮用水中湿态附着力随时间的变化
在盐水和饮用水环境下淡水舱涂层浸泡不同时间拉拔测试后的典型宏观形貌如图2所示。由图2a可知,在盐水中浸泡240 h后,金属基体表面已见明显腐蚀点,随着浸泡时间的增加,基体表面腐蚀区域增多。从断裂形式上分析,浸泡240和480 h后,涂层为混合型断裂,表现为金属基体表面仍有一部分涂层残留,浸泡720和1200 h后断裂形式表现为完全断裂。与在盐水中的情况相似,淡水舱涂层在浸泡240 h后,金属基体表面已产生肉眼可见腐蚀点,随着浸泡时间的增加,锈蚀区域的数量和面积不断增多,且比在盐水中的锈蚀更严重。从断裂形式上判断,淡水舱涂层在饮用水中均为完全断裂,金属基体表面绝大部分涂层已从金属表面剥离。

图2 盐水和饮用水浸泡环境下拉拔测试后淡水舱涂层典型的宏观形貌
2.1.2 介质的水传输性能
淡水舱涂层在盐水和饮用水中的水传输动力学曲线如图3所示。从图中可以明显看出,淡水舱涂层在两种溶液中的水传输过程均可分为两个阶段:吸收阶段和饱和阶段,且达到饱和阶段的时间都在50 h左右。所不同的是,同一时间节点淡水舱涂层在饮用水中具有更高的吸水率,饱和吸水率高达1.3%,明显高于盐水中的饱和吸水率1%。由此说明,饮用水较盐水具有更高的水渗透压,更容易通过涂层渗透到基体,这也就解释了为什么淡水舱涂层在饮用水中更容易锈蚀 (图2)。
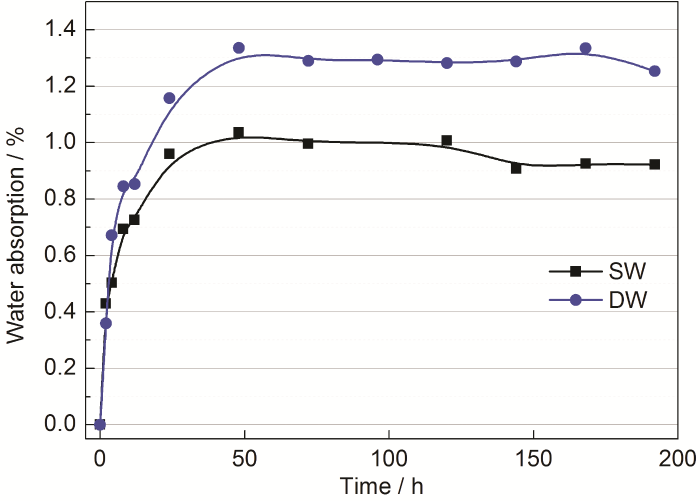
图3 淡水舱涂层在盐水和饮用水中的水传输动力学曲线
2.1.3 涂层致密性
涂层的致密性与涂层的电化学性质密切相关,可通过研究涂层的电化学失效历程监测涂层致密性的变化。淡水舱涂层在盐水和饮用水中开路电位随时间的变化如图4所示,可以看出,淡水舱涂层在两种溶液中开路电位的变化趋势完全不同,在盐水中的开路电位变化可分为3个阶段:第1阶段电位快速降低阶段,电位由开始时的0.15 V快速下降至96 h的-0.33 V,第2阶段电位波动阶段,由96 h的-0.33 V升高至480 h的-0.12 V而后迅速降低至600 h的-0.57 V,第3阶段电位平稳阶段,600~1200 h电位稳定在-0.6 V左右。为了便于比较,淡水舱涂层在饮用水中的开路电位也可分为3个阶段:第1阶段电位下降阶段,0~96 h,开路电位由-0.05 V降至-0.07 V,在96~600 h电位快速上升阶段,由-0.07 V升高至-0.03 V,96~1200 h电位波动上升阶段,由-0.03 V波浪式上升至-0.02 V。
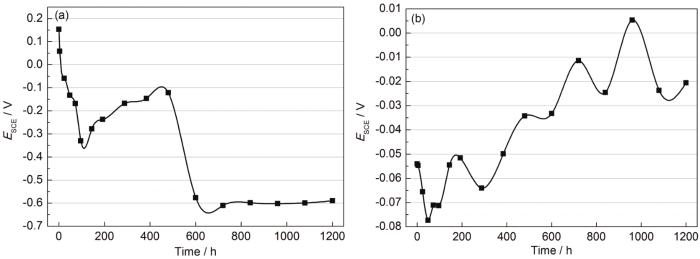
图4 淡水舱涂层在盐水和饮用水开路电位随时间的变化
根据淡水舱涂层在盐水中开路电位的变化特征,淡水舱涂层在3个阶段的电化学阻抗谱如图5所示。从图5中可以看出,淡水舱涂层在0~96 h电化学阻抗谱呈现容抗弧的特征,且容抗弧的半径随着浸泡时间的增加迅速减小 (图5a),电化学阻抗模值由0 h的1.1×1011降至96 h的2.9×109 Ω·cm2,降低了约2个数量级 (图5b),高频相位角接近90°,低频相位角随着浸泡时间的增加不断降低 (图5c)。在96~600 h,淡水舱涂层阻抗谱依然表现出容抗弧的特征,且双容抗弧的特征愈发明显,容抗弧的半径随浸泡时间的增加继续降低 (图5d),低频阻抗模值由96 h的2.9×109 Ω·cm2降低到600 h的2.7×108 Ω·cm2,阻抗模值再次降低1个数量级 (图5e),随着频率的降低,相位角不断降低 (图5f)。在600~1200 h,淡水舱涂层阻抗谱表现出高频容抗和低频扩散的特征 (图5g),阻抗模值和相位角维持在一个相对稳定的状态 (图5h和i)。
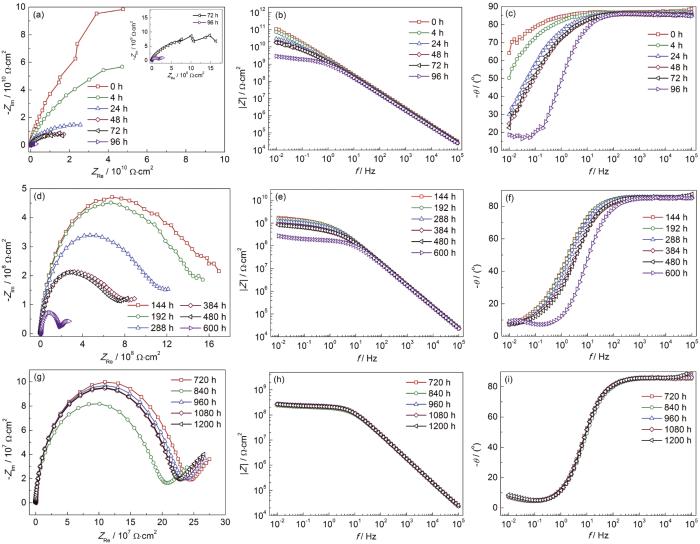
图5 淡水舱涂层在盐水中浸泡不同时间的电化学阻抗谱
淡水舱涂层在饮用水中3个阶段电化学阻抗谱如图6所示。淡水舱涂层在0~96 h电化学阻抗谱呈现容抗弧的特征,且容抗弧的半径随着浸泡时间的增加迅速减小 (图6a),电化学阻抗模值由0 h的8.8×1010 Ω·cm2降至96 h的9.8×109 Ω·cm2,电化学阻抗模值降低了约1个数量级 (图6b),高频相位角接近90°,低频相位角随着浸泡时间的增加不断降低 (图6c),这与其在盐水中0~96 h阶段的变化特征相似。在96~600 h,淡水舱涂层阻抗谱依然表现出容抗弧的特征,容抗弧的半径随浸泡时间的增加继续降低 (图6d),低频阻抗模值呈现缓慢下降的趋势,由96 h的9.8×109 Ω·cm2降低到600 h的3.5×109 Ω·cm2,降低了2倍多 (图6e),随着频率的降低,相位角不断降低,相位角的形状已基本不变 (图6f),这与其在盐水中96~600 h的变化特征保持一致。在600~1200 h,淡水舱涂层阻抗谱依然表现出容抗弧的特征,且容抗弧的半径大小和低频阻抗模值的变化趋势与其开路电位的变化相似,呈现波动式上升的趋势 (图6g和h),相位角的形状随浸泡时间的增加已基本不再变化 (图6i)。
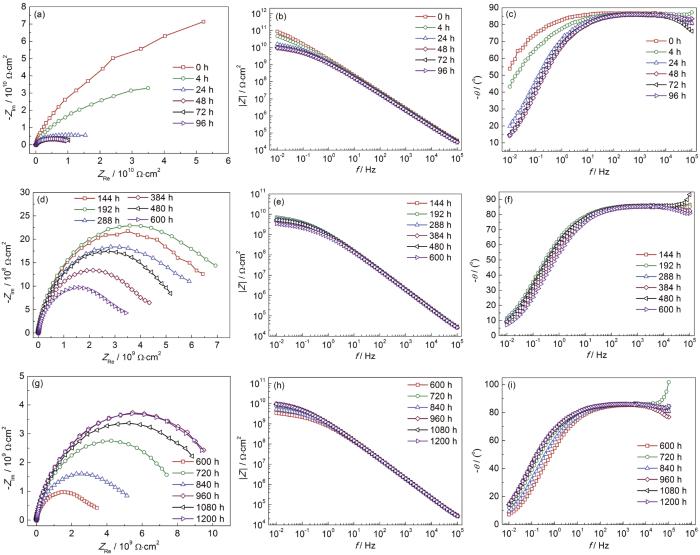
图6 淡水舱涂层在饮用水中浸泡不同时间的电化学阻抗谱
淡水舱涂层在盐水和饮用水中电化学阻抗谱低频模值随时间的变化如图7所示。可以看出,在涂层失效历程的0~96 h阶段,淡水舱涂层在盐水和饮用水中的阻抗模值随浸泡时间的增加均表现为快速降低的趋势,由1011降低到1010 Ω·cm2,降低了约1个数量级,但涂层在盐水中的低频阻抗模值要高于其在饮用水中的值,这是由于饮用水在涂层中的传输速度要明显高于盐水 (图3),迅速破坏了涂层的致密性。随着浸泡时间的增加,涂层失效进入到96~600 h阶段,淡水舱涂层在盐水中电化学阻抗谱的低频模值持续降低,降低约1.5个数量级,而其在饮用水中电化学阻抗谱的低频模值缓慢降低,维持在109 Ω·cm2这个数量级,比其在盐水中的模值高出1个数量级,造成这种差异的主要原因是此时盐水和饮用水均已渗入到涂层/金属界面,所不同的是盐水对金属基体的破坏速度明显高于饮用水,使得涂层体系的阻抗模值持续降低。涂层失效进入到600~1200 h阶段,淡水舱涂层在盐水中的低频模值已趋于平稳,保持在108 Ω·cm2这个数量级,而其在饮用水中的低频模值出现缓慢上升而后趋于稳定的变化特征,稳定在1010 Ω·cm2,导致最终淡水舱涂层在饮用水中的低频阻抗模值比其在盐水中高出约1.5个数量级。
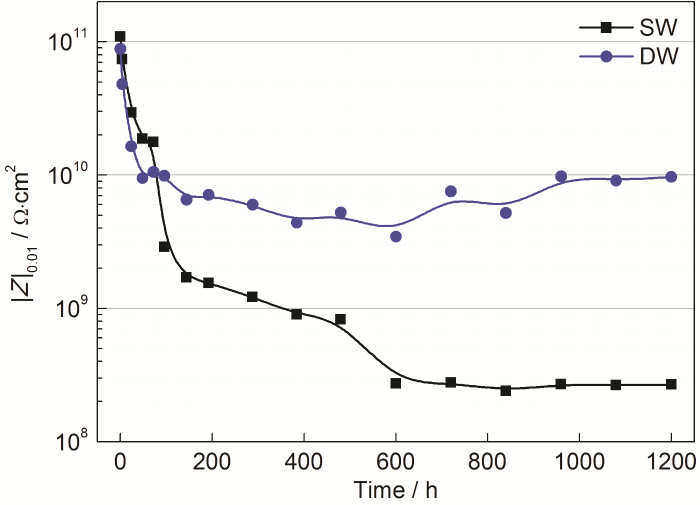
图7 淡水舱涂层在盐水和饮用水中电化学阻抗谱低频模值随时间的变化
2.2 淡水舱涂层在不同淡水中的失效机制
为了研究淡水舱涂层在不同淡水中的失效机制,选择了经海水淡化处理的反渗透水、在反渗透水基础上通过调整离子浓度得到的调质水以及饮用水3种淡水。淡水舱涂层在饮用水中的失效历程已在上节论述,这里不再重复赘述,着重介绍其在反渗透水和调质水中的失效机理。
2.2.1 淡水舱涂层在不同淡水中的附着性能
分别测试了淡水舱涂层在3种淡水中浸泡不同时间后的涂层附着力,测试结果如图8所示。可以看出,第一,淡水舱涂层经不同淡水浸泡后附着力并无明显降低的现象,相反,经过1200 h的浸泡,其在反渗透水和调质水中的附着力反而出现了上升的现象,这可能与涂层中的防腐助剂和防锈颜料有关;第二,淡水舱涂层在不同淡水中附着力随浸泡时间的增加并无明显的变化规律。
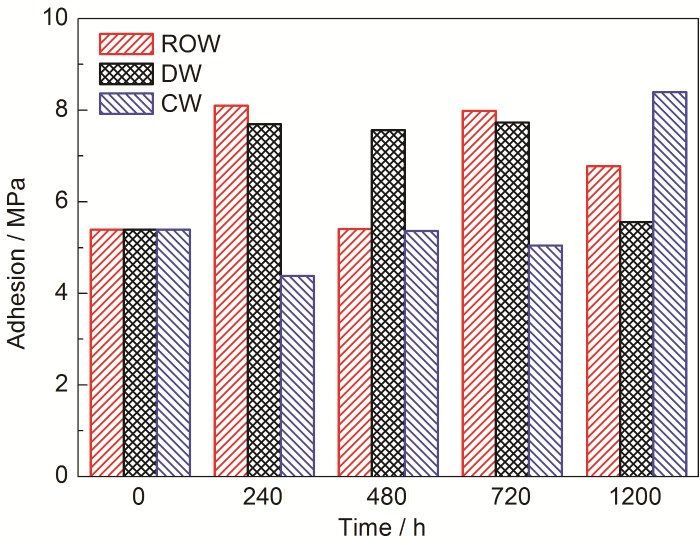
图8 淡水舱涂层在不同淡水中附着力随浸泡时间的变化
淡水舱涂层在反渗透水和调质水中浸泡不同时间附着力测试后的宏观形貌分别如图9所示。从图中可以看出,对于两种不同的淡水,在浸泡240 h后,金属基体表面均可见明显的锈点,说明此时两种水介质均已渗透涂层到达涂层/金属界面,造成了金属基体的腐蚀。此时,金属基体上还有部分涂层残留,随着浸泡时间的增加,涂层已基本完全被拔开,金属基体表面锈蚀程度增加。

图9 淡水舱涂层在反渗透水和调制水中浸泡不同时间附着力测试后的宏观形貌
2.2.2 淡水舱涂层在不同淡水中的水传输性能
淡水舱涂层在3种淡水环境中的水传输动力学曲线如图10所示。可见,涂层在3种淡水中的水传输过程均可分为两个阶段:吸收阶段和饱和阶段,且达到饱和阶段的时间都在50 h左右。所不同的是,调质水和饮用水中具有更高的吸水率,饱和吸水率高达1.3%,稍高于反渗透水中的饱和吸水率1.2%。
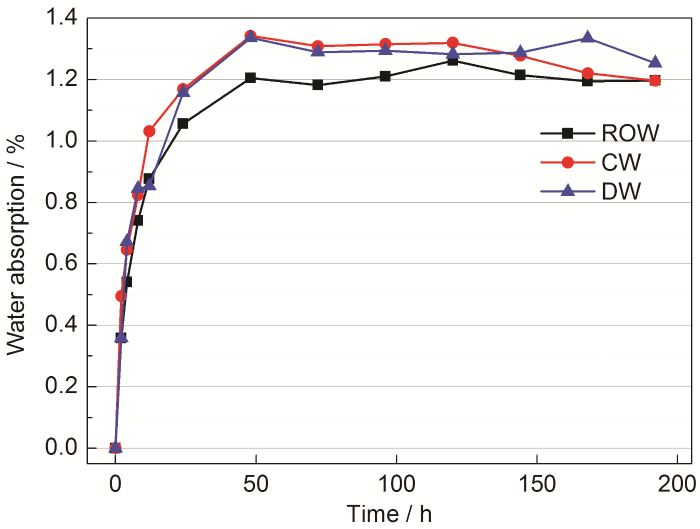
图10 淡水舱涂层在3种不同淡水环境的水传输动力学曲线
2.2.3 淡水舱涂层在不同淡水中的致密性能
淡水舱涂层在3种淡水环境中开路电位随时间的变化如图11所示。可以看出,涂层在3种淡水环境中开路电位随时间的变化特征基本一致,均表现为波动式上升的趋势。所不同的是,涂层在反渗透水中的开路电位始终最高,其次是调质水,最低的为饮用水。为了方便和饮用水做对比,同样将涂层在反渗透水和调质水中的失效历程分成0~96,96~600和600~1200 h 3个阶段。
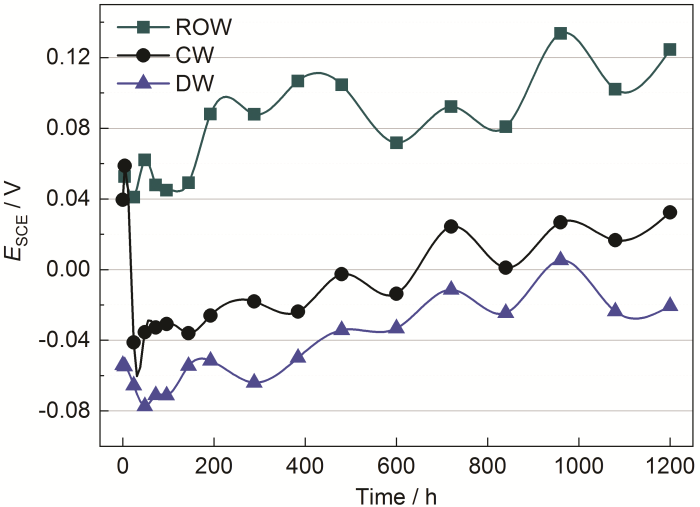
图11 淡水舱涂层在3种淡水环境中开路电位随浸泡时间的变化
淡水舱涂层在反渗透水中3个阶段的电化学阻抗谱如图12所示。淡水舱涂层在0~96 h电化学阻抗谱呈现容抗弧的特征,且容抗弧的半径随着浸泡时间的增加迅速减小 (图12a),电化学阻抗模值由0 h的9.3×1010 Ω·cm2降至96 h的1.0×1010 Ω·cm2,电化学阻抗模值降低了约1个数量级 (图12b),高频相位角接近90°,低频相位角随着浸泡时间的增加不断降低 (图12c),整体表现出两个时间常数的特征。在96~600 h,淡水舱涂层阻抗谱依然表现出容抗弧的特征,容抗弧的半径随浸泡时间的增加继续降低 (图12d),低频阻抗模值呈现缓慢下降的趋势,由96 h的1.0×1010 Ω·cm2降低到600 h的4.6×109 Ω·cm2,降低了1倍多 (图12e),随着频率的降低,相位角不断降低,但随时间的增加,相位角的形状已基本不变 (图12f),依然表现出两个时间常数的特征。在600~1200 h,淡水舱涂层阻抗谱依然表现出容抗弧的特征,且容抗弧的半径大小和低频阻抗模值的变化趋势与其开路电位的变化相似,呈现波动式上升的趋势 (图12g和h),相位角的形状随浸泡时间的增加已基本不再变化 (图12i)。
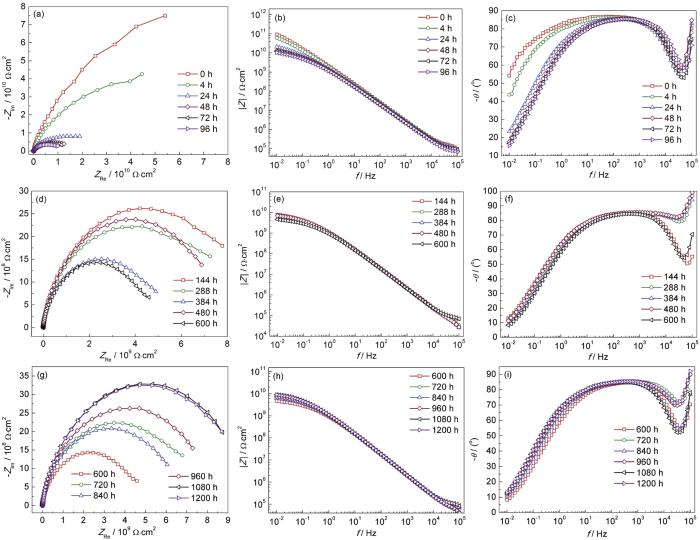
图12 淡水舱涂层在反渗透水中浸泡不同时间的电化学阻抗谱
淡水舱涂层在调质水中3个阶段的电化学阻抗谱如图13所示。淡水舱涂层在0~96 h电化学阻抗谱呈现容抗弧的特征,且容抗弧的半径随着浸泡时间的增加迅速减小 (图13a),低频阻抗模值由0 h的9.1×1010 Ω·cm2降至96 h的1.1×1010 Ω·cm2,降低了约1个数量级 (图13b),高频相位角接近90°,低频相位角随着浸泡时间的增加不断降低 (图13c),整体表现出两个时间常数的特征。在96~600 h,淡水舱涂层阻抗谱依然表现出容抗弧的特征,容抗弧的半径随浸泡时间的增加继续降低 (图13d),低频阻抗模值呈现缓慢下降的趋势,由96 h的1.1×1010 Ω·cm2降低到600 h的4.8×109 Ω·cm2,降低了1倍多 (图13e),随着频率的降低,相位角不断降低,但随时间的增加,相位角的形状已基本不变 (图13f),依然表现出两个时间常数的特征。在600~1200 h,淡水舱涂层阻抗谱容抗弧的特征依然没有改变,且容抗弧的半径大小和低频阻抗模值的变化趋势与其开路电位的变化相似,呈现波动式上升的趋势 (图13g,h),相位角的形状随浸泡时间的增加已基本不再变化 (图13i)。
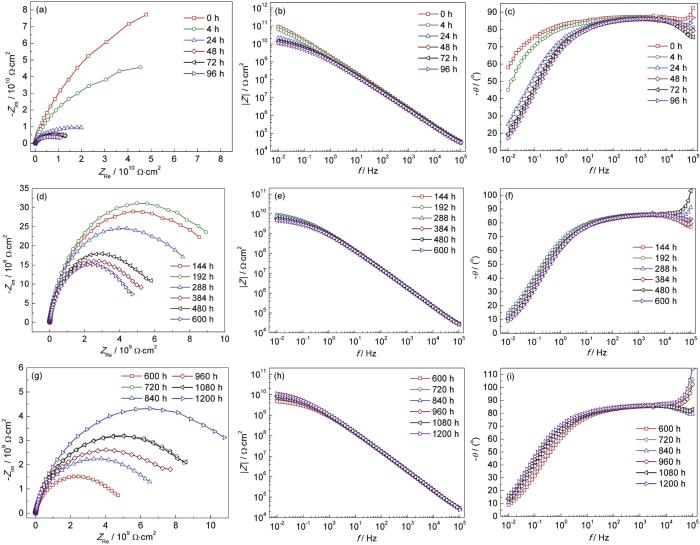
图13 淡水舱涂层在调质水中浸泡不同时间的电化学阻抗谱
综合以上分析可知,淡水舱涂层在反渗透水、调质水和饮用水3种淡水环境中表现出相同的腐蚀失效机制,腐蚀失效历程均可分成3个阶段,每个阶段低频阻抗模值随时间的变化如图14所示。第1阶段,随着水介质的快速渗透,涂层的阻抗模值迅速降低,由数量级1011 Ω·cm2降至1010 Ω·cm2,降低幅度达1个数量级,其中饮用水的阻抗模值要低于反渗透水和调质水,如图14a所示,主要原因是3种淡水中饮用水在涂层中的扩散速度最快 (图10)。第2阶段,水质已渗透到涂层/金属界面,并造成了金属基体的腐蚀 (图2b、图9),导致涂层的阻抗模值继续降低,降低的幅度较第1阶段有所减小,600 h过后阻抗模值降低为96 h的一半,维持在这个109 Ω·cm2数量级,并且饮用水中的阻抗模值依然最小,如图14b所示。第3阶段,在涂层中防腐助剂、防锈颜填料等的综合作用下,涂层的阻抗模值再次上升到第2阶段开始时的水平,如图14c所示。
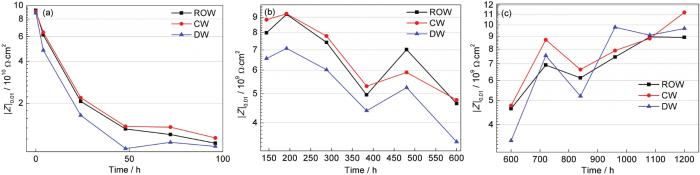
图14 淡水舱涂层腐蚀失效过程中低频阻抗模值随时间的的变化
3 结论
(1) 淡水舱涂层在盐水和饮用水中的附着力随着浸泡时间的增加均没有降低的趋势,淡水舱涂层中饮用水比盐水具有更快的渗透速度,导致涂层在淡水中会优先失效,随着腐蚀介质不断渗透到涂层/金属界面,由于盐水比饮用水对金属基体的腐蚀性更强,导致最终涂层在饮用水中的阻抗模值明显高于其在盐水中的值。
(2) 涂层在反渗透水、调质水和饮用水3种淡水中的腐蚀失效过程相同,电化学阻抗谱特征上可分为明显的3个阶段:阻抗谱的快速下降,缓慢下降和上升阶段,造成以上特征的原因分别是水的快速渗透、涂层/金属界面的腐蚀和防锈颜填料的缓蚀。
参考文献
[1]
Dong Y H, Zhou Q.
Relationship between ion transport and the failure behavior of epoxy resin coatings
[J]. Corros. Sci., 2014, 78: 22
[本文引用: 1]
[2]
Posner R, Marazita M, Amthor S, et al.
Influence of interface chemistry and network density on interfacial ion transport kinetics for styrene/acrylate copolymer coated zinc and iron substrates
[J]. Corros. Sci., 2010, 52: 754
[本文引用: 1]
[3]
Bi H C, Sykes J.
Cathodic delamination of unpigmented and pigmented epoxy coatings from mild steel
[J]. Prog. Org. Coat., 2016, 90: 114
[本文引用: 1]
[4]
Sørensen P A, Dam-Johansen K, Weinell C E, et al.
Cathodic delamination: Quantification of ionic transport rates along coating-steel interfaces
[J]. Prog. Org. Coat., 2010, 67: 107
[5]
Khun N W, Frankel G S.
Effects of surface roughness, texture and polymer degradation on cathodic delamination of epoxy coated steel samples
[J]. Corros. Sci., 2013, 67: 152
[本文引用: 1]
[6]
Shi C, Shao Y W, Xiong Y, et al.
Influence of silane coupling agent modified zinc phosphate on anticorrosion property of epoxy coating
[J]. J. Chin. Soc. Corros. Prot., 2020, 40: 38
[本文引用: 1]
师超, 邵亚薇, 熊义等.
硅烷偶联剂改性磷酸锌对环氧涂层防腐性能的影响
[J]. 中国腐蚀与防护学报, 2020, 40: 38
[本文引用: 1]
[7]
Liu X L, Shao Y W, Zhang Y J, et al.
Using high-temperature mechanochemistry treatment to modify iron oxide and improve the corrosion performance of epoxy coating-I. High-temperature ball milling treatment
[J]. Corros. Sci., 2015, 90: 451
[8]
Liu X L, Shao Y W, Zhang Y J, et al.
Using high-temperature mechanochemistry treatment to modify iron oxide and improve the corrosion performance of epoxy coating-II. Effect of grinding temperature
[J]. Corros. Sci., 2015, 90: 463
[9]
Deyab M A, Ouarsal R, Al-Sabagh A M, et al.
Enhancement of corrosion protection performance of epoxy coating by introducing new hydrogenphosphate compound
[J]. Prog. Org. Coat., 2017, 107: 37
[本文引用: 1]
[10]
Montazeri S, Ranjbar Z, Rastegar S.
A study on effects of viscoelastic properties on protective performance of epoxy coatings using EIS
[J]. Surf. Coat. Technol., 2017, 111: 248
[本文引用: 1]
[11]
Creus J, Mazille H, Idrissi H.
Porosity evaluation of protective coatings onto steel, through electrochemical techniques
[J]. Surf. Coat. Technol., 2000, 130: 224
[12]
Upadhyay V, Battocchi D.
Localized electrochemical characterization of organic coatings: A brief review
[J]. Prog. Org. Coat., 2016, 99: 365
[13]
Posner R, Wapner K, Amthor S, et al.
Electrochemical investigation of the coating/substrate interface stability for styrene/acrylate copolymer films applied on iron
[J]. Corros. Sci., 2010, 52: 37
[14]
Nazarov A, Le Bozec N, Thierry D.
Assessment of steel corrosion and deadhesion of epoxy barrier paint by scanning Kelvin probe
[J]. Prog. Org. Coat., 2018, 114: 123
[15]
Cambier S M, Posner R, Frankel G S.
Coating and interface degradation of coated steel, Part 1: Field exposure
[J]. Electrochim. Acta, 2014, 13: 30
[16]
Cambier S M, Frankel G S.
Coating and interface degradation of coated steel, Part 2: accelerated laboratory tests
[J]. Electrochim. Acta, 2014, 136: 442
[本文引用: 1]
[17]
Shi Y, Fang Q, Guo C Q, et al.
Preparation of environmentally friendly ship fresh water tank coatings and study on its properties
[J]. China Coat., 2016, 31(10): 29
[本文引用: 1]
石勇, 方倩, 郭常青等.
环境友好型长寿命淡水舱涂料的制备及性能研究
[J]. 中国涂料, 2016, 31(10): 29
[本文引用: 1]
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414





