外加电流阴极保护是保护金属免受电腐蚀的常用方法。本文我们将解释这种方法的工作原理以及常见的应用。最后给出一个船体仿真模型。在该模型中,对轴、螺旋桨阴极保护系统产生的电场信号进行分析是仿真非常重要的一个方面。
防止电偶腐蚀
若将金属放入电解液中,将始终面临电偶腐蚀的风险。这种类似的反应会发生在水环境,土壤,混凝土,以及大气环境下。当潮湿的空气凝结在金属表面上时,会形成一层电解液薄膜。当金属周围被电解液环绕,并且电解液能够将其中的离子从金属的一端传输到另一端时,就会受到腐蚀。即使是看似相同类型的金属(铸铁),也会由于金属中的杂质或金属本身的不同而被腐蚀,这种腐蚀可能是由于金属与结构的其他部分具有不同的电化学势造成的。

板上螺栓的电偶腐蚀。D3j4vu 提供的自己的作品。通过 Wikimedia Commons 在 CC BY-SA 3.0 下获得许可。
如果不对金属进行保护,电偶腐蚀会导致点蚀、缝隙腐蚀等问题。为了缓解此类问题,可能需要通过聚合物涂层来将金属与电解质环境隔离开。但是,随着时间的流逝,此类涂层可能会因撞击或穿透而被破坏,最终导致腐蚀。
在许多情况下,如果金属的第一道保护屏障被破坏,通常会采用另一种方法来避免电偶腐蚀。这种方法就是通过结构极化,使暴露的金属成为系统的阴极来实现的。暴露的金属受阴极反应控制,阳极反应造成的材料损失可以忽略不计。通常有下列两个方法来保护金属不受腐蚀:
通过牺牲阳极来实现阴极保护(SACP)
使用电化学平衡电位较低的牺牲金属
通过外加电流来实现阴极保护(ICCP)
使用外部电流源(通常是整流器),产生直流电流,使金属表面极化成阴极电位区
电流源与一些由惰性材料制成的阳极相连接,不像牺牲阳极那样消耗电流
ICCP 方法通常用于陆上管道,港口,混凝土结构,船舶等。由于其具有高电流输出和易于安装等特点,它也是海上石油平台加装腐蚀防护系统的一种常用方法。
ICCP 的一个主要缺点是电流输出可能很大,这会导致附近金属表面产生非常负的极化。这可以使阴极极化成一个发生析氢的区域。对于某些结构,氢会扩散到金属表面并在金属中产生氢脆和氢致应力开裂 (HISC)的风险。
SACP 可能更常用于钢结构,因为析氢的风险不太明显。在大型船舶上,这是一种非常常见的阴极保护方法。用于将施加电流的阳极嵌入容器的船体表面,与具有相同电流容量的牺牲阳极相比,其产生的阻力要小得多。
模拟通过外加电流实现的阴极保护
如果想要在一个几何大结构的背景下捕获物理和电化学的所有细节,对腐蚀进行建模会极具挑战性。幸运的是,在对较大规模的阴极保护(例如船体,管道或石油平台)建模时,可以做一些假设和简化。
首先,从控制方程式和电解液质充分混合的假设入手,将方程式进行简化,以便可以只计算由离子迁移引起的电解液质中的电流平衡。这就会把控制方程式简化为拉普拉斯方程式,其中电解液质的电导率作为材料参数输入。
电流密度平衡的方程式为
![]()
其中
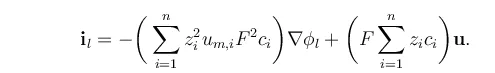
其中, 是电解液中的电流密度,n 是物种的数量,z 是离子的电荷, 是离子的迁移率,F 是法拉第常数,c 是物种的浓度, 是电解液的电位,u 是描述电解液流动的速度矢量。
上面方程式右侧的第二项包含了电中性条件,它等于零。方程式右边第一项括号内的系数等于电解液的电导率。这就得到了完全混合电解液中电流密度的表达式:
![]()
在所有的金属表面上,可以同时发生阳极和阴极反应。这些反应可以用 Butler-Volmer 或 Tafel 方程确定的电流密度来表示。Butler-Volmer 方程给出了表面上电化学势函数的电化学反应速率。使用法拉第定律,由于涉及到电子,因此得到了电流密度(参考文献1).Butler-Volmer 方程式可以描述发生在阴极上的析氢反应:
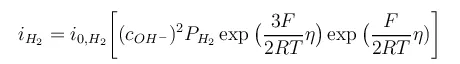
其中 为交换电流密度, 是无量纲氢氧根离子浓度,为无量纲氢分压,R 为通用气体常数,T 为温度和 η 活化过电位。
活化过电位定义为:
![]()
其中,表示电级表面电势, 表示相对系统中所有反应共有的特定参考电极测得的平衡电极电势。
通过给出这些方程式中不同的参数,可以得到极化曲线,如下图所示:
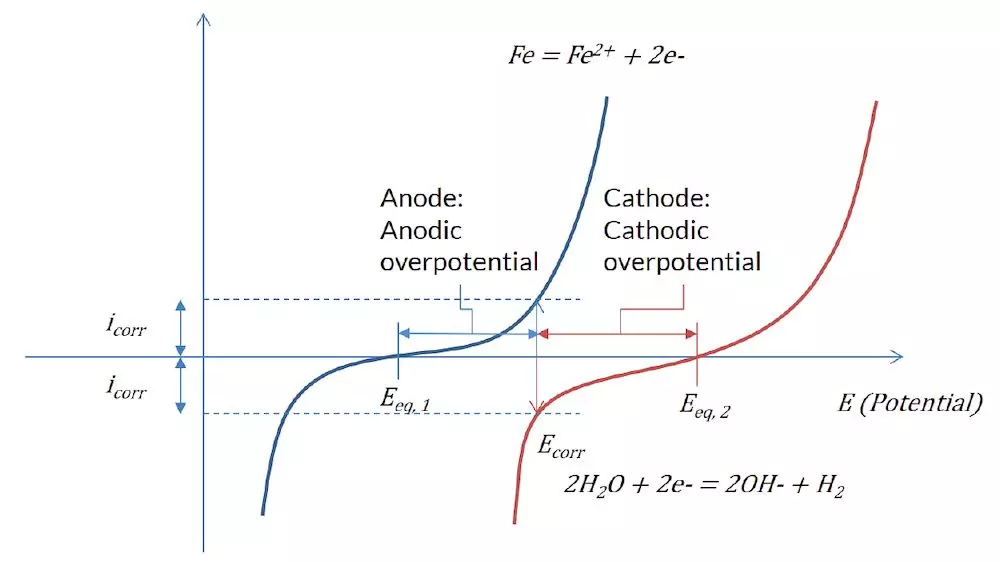
图1:在次贵金属 表面(蓝色)和较贵金属 表面(红色)处反应的 Butler–Volmer 表达式。
这些极化曲线通常也用埃文斯图(Evans diagram)表示:
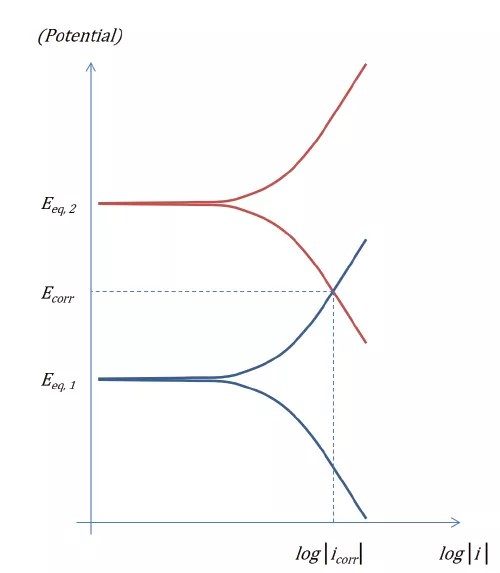
图 2:在没有欧姆和质量输运损耗的情况下,两个电极反应的埃文斯图。
对于外加电流阳极,通常需要设置电流密度,以使系统在参考电位上达到给定的电解液电势。这构成了模拟外加电流的阴极保护所需的材料参数和边界条件。
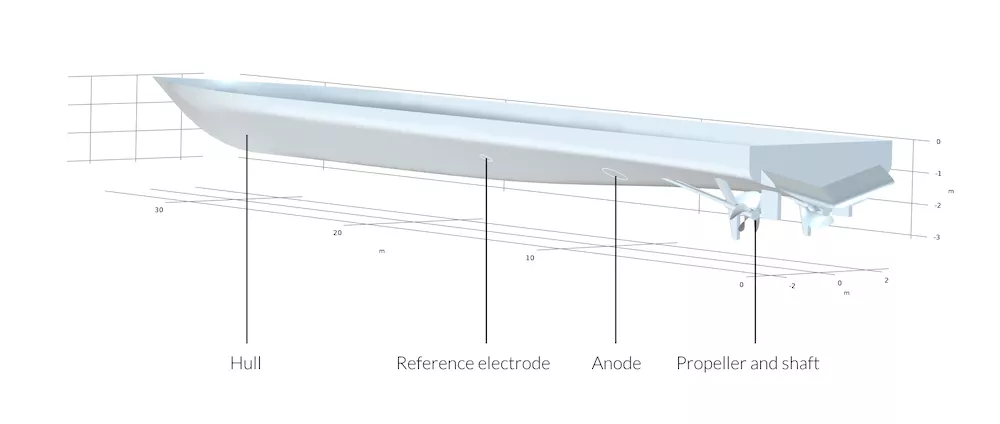
图 3:船体示意图,其中包括参考电极,阳极,螺旋桨和轴的位置。
在船体上建立 ICCP 模型
在给定的示例(也可以在官网案例库中找到:cn.comsol.com/models),我们研究了带有轴和螺旋桨的船体,该船体和螺旋桨受到外加电流的保护。还研究了涂层螺旋桨与未涂层螺旋桨的区别。目的是评估两种不同情况下沿船龙骨的剖面情况。这在海军军事应用中很重要,因为在海军应用中,大家会想知道海水中电磁信号的大小。
当我们导入几何图形并定义了电解质域后,有几个关键步骤如下:
定义参考电极(图4)
在几何稳定的外加电流阳极处添加电解液电位边界条件,并将该条件设置为0 V
请参考暴露金属表面设置中的参考电位,并将参考电位与参考电位上所需的保护电位差进行对比(图5)。
输入暴露在电解液中的各种金属相应的平衡电位和反应参数(图 6)
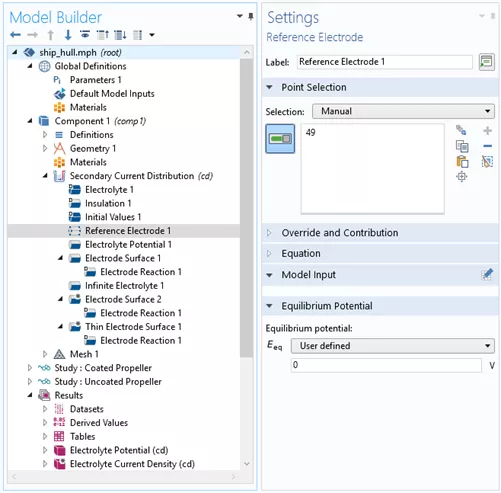
图 4:参考电位在某一点的设置。
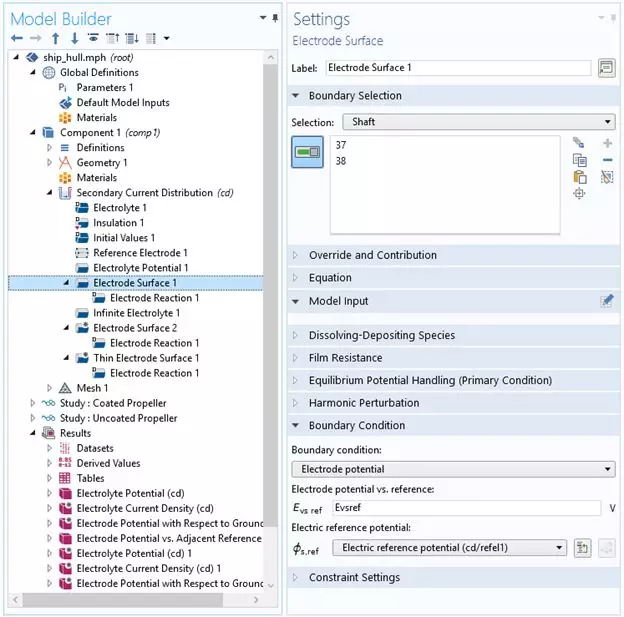
图 5:用外加电流保护的金属电极表面的设置。
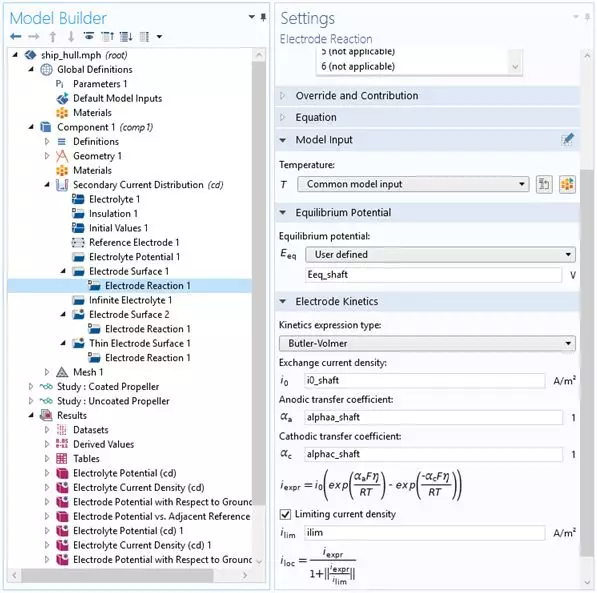
图 6:模型中轴上受保护金属上的电极反应设置。
结论
电极电位与参考电位之间的比较是评估海洋腐蚀时最常用的量。通过查看不同的电位,可以清楚地知道这些物体是否受到保护,以及是否可能有一些区域会发生析氢等,如果有,那么应采用更好的电屏蔽措施。船体表面的电势如下图所示。
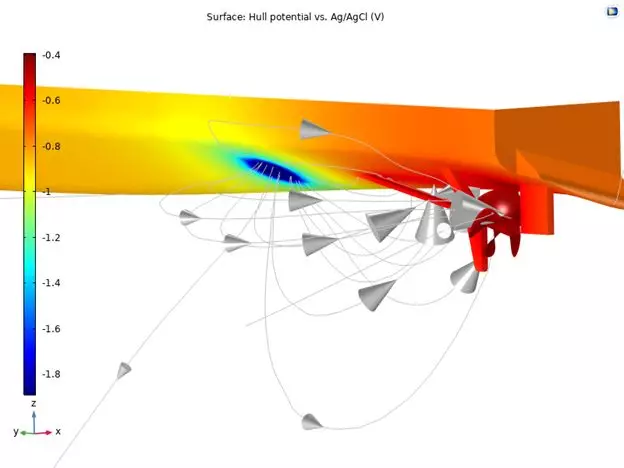
图 7:带有 625 合金螺旋桨的和镍铝青铜(NAB)轴的船体在外加电流阴极保护下相对 Ag / AgCl 参考电极的电极电势。
在这个模型中,通过研究沿船体龙骨的相对 Ag/AgCl 的电极电位,你将了解到使用涂层或未涂层的螺旋桨会怎样影响电场信号。同时也可以看到,带涂层的螺旋桨在电解液电位上变化较小,因此在船舶周围的电场会给一个较小的信号。
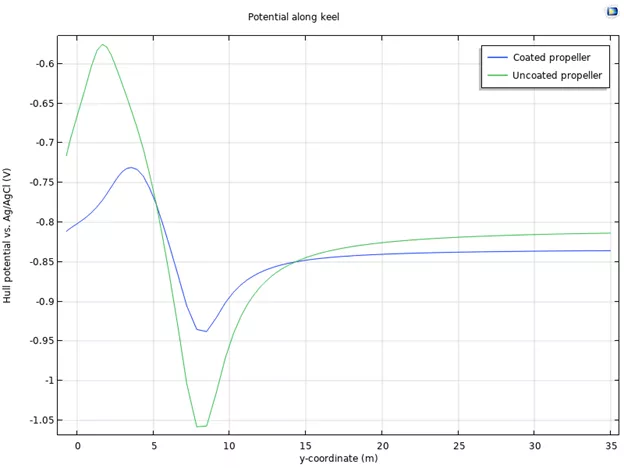
图 8:带有涂层和未涂层螺旋桨的船体龙骨的,相对 Ag / AgCl 参考值的电位。
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414





