齐锴,邱于兵,陈振宇,郭兴蓬*
华中科技大学化学与化工学院,材料化学与服役失效湖北省重点实验室,湖北,武汉,430074,
Email: guoxp@mail.hust.edu.cn

作者简介
姓名:郭兴蓬
部门:华中科技大学 化学与化工学院 材料与环境化学研究所
职务(职称):教授、博导
电话:027-87558221
邮件:guoxp@mail.hust.edu.cn
关键词 环境化学
简介:教育与工作经历
1978.9~1982.7 湖南大学化学化工系(获学士学位)
1982.9~1985.5 华中理工大学化学系(获硕士学位)
1985.5~1991.12华中理工大学化学系 助教、讲师
1992.1~1996.3 日本国立新潟大学大学院(获博士学位)
1996.4~1999.10(日本)帝国石油技术研究所 研究员
1999.10~现在 华中科技大学化学与化工学院教授
本科教学与研究生教学
主讲本科生课程“工程化学”、“应用电化学”,硕士研究生课程“电化学方法”,博士研究生课程“材料腐蚀学”
研究生招生培养专业/授予学位:材料物理与化学/工学博士,材料学/工学博士;应用化学/工学硕士,物理化学/理学硕士
研究方向
腐蚀与控制:腐蚀电化学与监检测技术/缓蚀剂原理与应用/微系统腐蚀/油气田特殊环境下的腐蚀失效机理与防护
应用电化学:材料电化学/环境电化学
学术兼职及参加学会
教育部高等学校材料物理与化学教学指导委员会委员;国家留学基金会评审专家;中国腐蚀与防护学会副理事长、缓蚀剂专业委员会主任委员;中国石油学会腐蚀与防护专业委员会副主任委员;湖北省腐蚀与防护学会副理事长;美国NACE高级会员;日本电化学学会腐蚀专业委员会会员;湖北省化学化工学会理事;腐蚀与防护国家重点实验室学术委员会委员;海洋腐蚀与防护国防重点实验室学术委员会委员;材料化学与服役失效湖北省重点实验室学术委员会副主任。
主要科研项目(2006~)
金属/溶液界面纳米尺度下缓蚀膜的力学—电化学行为及机理研究(国家自然科学基金)
微系统金属材料腐蚀行为及机理研究(国家自然科学基金)
薄层液膜下金属材料的腐蚀与电化学迁移行为及机理研究(国家自然科学基金)
酸性油气田管道腐蚀安全智能监测系统研究(863)
CO2驱注采井缓蚀剂筛选和缓蚀机理研究(973子课题)
土壤腐蚀原位监测技术和形态定量表征方法研究(国家科技基础条件平台建设)
Suitable inhibitors to prevent corrosion for 13Cr and super 13Cr martensitic stainless steel in completion fluid(国际合作研究)
中低CO2高矿化度水气井的缓蚀剂及应用技术研究(中石油长庆油田)
高含H2S/CO2气田地面集输系统缓蚀剂技术研究(中石化胜利油田)
海洋油气田CO2腐蚀缓蚀剂及应用研究(中海油南海西部油田)
CO2驱复合型缓蚀剂配方体系及加注工艺技术研究(国家重大专项子课题)
Investigation on Corrosion Inhibitors for Magnesium Alloys(国际合作研究)
获奖成果与专利
高含CO2海洋油气田缓蚀技术的研究及应用(湖北省科技进步二等奖)
高含CO2油气田缓蚀技术的研究及应用(中国腐蚀与防护学会科技进步二等奖)
330K及以上高压交流电线路对金属管线的影响与防护研究(国家电网公司三等奖/合作,第二单位)
Rapid determination of Tafel slopes by an integral method of coulostatically induced transients (山东省自然科学学术创新奖三等奖/合作,第二单位)
一种水溶性CO2缓蚀剂的合成工艺及性能评价(发明专利,ZL02139204.8)
基于电化学噪声的局部腐蚀分析方法和装置(发明专利,ZL200610124756.2)
一种电偶电化学噪声腐蚀监测探针(发明专利,201010585395.8)
抑制镁合金在汽车冷却液中腐蚀的缓蚀剂(发明专利,201010203451.7)
高稳定性全钒液流电池阳极电解液及其制备方法(发明专利,201110078073.9)
研究论文
共发表论文150余篇,其中SCI收录论文60余篇。近5年来在国内外学术期刊发表论文90余篇(SCI收录44篇),其中在Electrochimica Acta, Corrosion science, J. the Electrochemical society等国际学术期刊发表论文44篇,在物理化学学报、中国腐蚀与防护学报等国内学术期刊发表论文47篇。
摘 要:材料在环境介质的作用下发生的破坏(结构或功能的丧失)现象称之为腐蚀,导电高分子材料在使用环境中的降解也是一种腐蚀过程。本文通过循环伏安法和交流阻抗法比较了掺杂不同尺寸阴离子的聚吡咯膜在碱性环境中腐蚀前后的电化学活性和电导性的变化,研究了掺杂离子对聚吡咯稳定性的影响。实验表明,掺杂阴离子的尺寸越大,聚吡咯抗腐蚀的性能越好,在碱性环境中浸泡后,仍能保持良好的电化学活性和电导性。IR和XPS分析数据结果证明:掺杂阴离子尺寸越大,其位阻效应越大,越不容易从聚吡咯膜内脱出,很难与OH-进行交换,亲核基团仅能进攻聚吡咯表层结构而无法侵入膜内部,故在碱性溶液中具有良好的环境稳定性。
关键词:导电高分子材料;聚吡咯;腐蚀;掺杂阴离子
1 前言
导电高分子材料具有金属和半导体特性、结构多样化、可逆的掺杂和脱掺杂、比重轻等优异的物理化学性能,因而在二次电池、超级电容器、太阳能电池、传感器、电磁屏蔽、隐身技术、生命科学、人工肌肉、分子器件、光/电子器件和金属防腐等领域有着广泛应用,自发现之日起就成为了材料科学的研究热点[1-4]。在导电高分子材料走向商业应用的进程中,首先需要关注和解决的关键问题就是稳定性,尤其是电化学活性的稳定。根据现代腐蚀理论 [5],腐蚀的定义不仅仅局限于金属材料,凡是材料受环境介质的化学作用而破坏的现象都可以称之为腐蚀,故导电高分子材料在外界环境作用下的降解老化、功能丧失也是一种腐蚀过程。#p#副标题#e#
在诸多导电高分子中,掺杂聚吡咯(Polypyrrole,PPy)具有相对较高的电导率、良好的环境稳定性和优良的生物兼容性以及易于采用化学或电化学的方法合成等特点,被认为是最具商业前景的导电高分子材料之一,引起了人们的广泛关注。但稳定性是限制其商业应用的重要因素,尤其是聚吡咯的许多重要应用都是在水溶液中实现的,如人工肌肉、电极材料、催化剂载体、传感器等 [6]。一般认为聚吡咯发生腐蚀是由于其主链单元受到H2O、OH-、CH3OH、NH3等亲核基团的进攻而发生过氧化,导致共轭结构遭到破坏 [7],进而影响到其物理化学性质,尤其是电化学活性的损失,造成材料失效。
溶液pH值对聚吡咯稳定性影响的研究至今已有大量报道 [8-9],但对于其他因素影响的研究仍有待进一步深入。掺杂离子对聚吡咯的性质有着重要的影响,根据我们之前的研究,掺杂离子的尺寸在很大程度上决定了聚吡咯的离子交换性能 [10],但其对聚吡咯稳定性的影响仍不是很清楚。本文通过循环伏安法和交流阻抗法比较了掺杂不同尺寸阴离子的聚吡咯膜在碱性环境中腐蚀前后的电化学活性和电导性的变化程度,研究掺杂离子对聚吡咯稳定性的影响,并通过红外和XPS分析所得结果,对这一影响的机理进行了讨论。
2 实验部分
2.1 电化学合成
电化学合成使用CS350电化学工作站采用三电极体系,铂片为工作电极(面积0.25 cm2),使用前用氧化铝研磨膏抛光,丙酮擦拭,放入蒸馏水中备用。铂电导电极为辅助电极,饱和甘汞电极为参比电极(文中电位均相对于SCE)。电化学聚合反应在室温(~25℃)下密闭电解槽中进行。吡咯单体(Pyrrole,Py,SAFC, >98%)使用前蒸馏提纯,冰箱中避光保存备用。合成用电解液分别为0.1mol/L Py + 0.1mol/L氯化钠(NaCl),0.1mol/L Py + 0.1mol/L硝酸钠(Na2SO4),0.1mol/L Py + 0.1mol/L硫酸钠(Na2SO4),0.1mol/L Py + 0.1mol/L对甲苯磺酸钠(NapTS),0.1mol/L Py + 0.01mol/L十二烷基苯磺酸钠(NaDBS)和0.1mol/L Py + 0.001mol/L聚苯乙烯磺酸钠(NaPSS)。聚合反应前通N2除氧20 min。电化学合成采用恒电流法,合成电流密度为1mA/cm2,合成时间800 s。合成完成后,聚吡咯电极用蒸馏水清洗备用。
2.2 不同聚吡咯膜在碱性环境中降解前后的电化学测试及光谱分析
聚吡咯膜的稳定性通过比较其在碱性溶液中降解前后的电化学活性和电导性的变化程度来进行评价,其中聚吡咯膜的电化学活性和电导率分别用循环伏安(CV)和交流阻抗(EIS)测试。新合成的不同聚吡咯膜分别在1mol/L NaOH + 0.1mol/L NaCl浸泡3h,然后再在N2除氧0.1mol/LNaCl溶液中常温下进行CV测试,扫描速率为20mV/s。聚吡咯膜本体电阻(电导性)降解前后的变化采用阻塞电池体系通过交流阻抗进行测量。聚吡咯膜的结构和组分在碱性溶液中降解前后的变化通过FTIR(Vertex 70)和XPS(VG Multilab 2000)进行分析。
3 结果与讨论
3.1 电化学测试结果
聚吡咯材料在水溶液介质中的降解,尤其是在碱性环境中,主要是由于其主链结构受到亲核基团的进攻。聚吡咯的降解可以通过其电化学氧化还原活性的变化进行评价,即循环伏安曲线氧化还原峰及电流容量的变化。图1为掺杂不同尺寸对阴离子的聚吡咯膜在1mol/L NaOH + 0.1mol/L NaCl溶液中降解3h前后在0.1mol/L NaCl溶液中稳定后的CV测试循环伏安图。图1a可以看出,掺杂小尺寸阴离子SO42-的聚吡咯膜在NaOH溶液中降解3h后循环伏安电流容量明显降低,其电化学活性基本消失。掺杂中等尺寸对阴离子pTS-的聚吡咯膜在NaOH溶液中浸泡3h后,保持了大部分的电化学活性,如图1b所示。而掺杂大尺寸对阴离子PSS-的聚吡咯膜在碱性溶液中浸泡3h后仍然能很好地保持其电化学活性(图1c)。
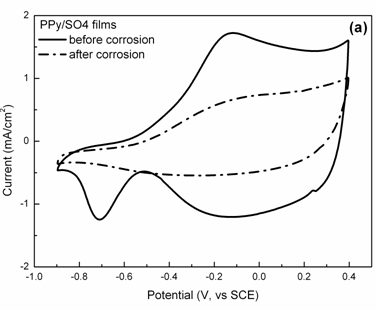
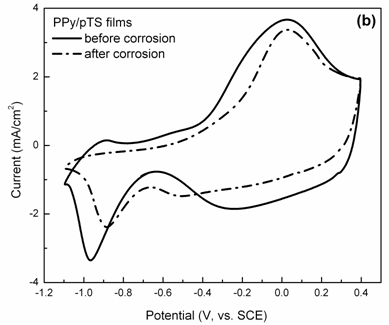
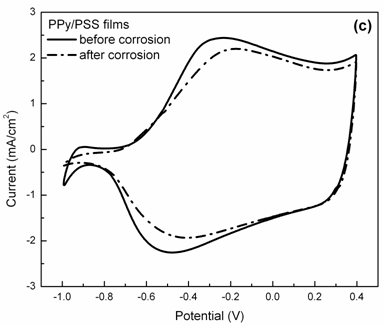
图1 不同聚吡咯膜在1MNaOH+0.1MNaCl中降解3h前后在0.1MNaCl中的循环伏安图:(a)掺杂小尺寸对阴离子聚吡咯膜PPy/SO4;(b)掺杂中等尺寸对阴离子聚吡咯膜PPy/pTS;(c)掺杂大尺寸对阴离子聚吡咯膜PPy/PSS
聚吡咯膜的降解度可以使用式(1),通过比较其降解前后的循环伏安电流容量值进行衡量:
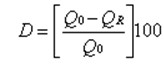 (1)
(1)
其中,Q0是新合成的聚吡咯膜在0.1mol/L NaCl中的循环伏安电流容量,QR是在碱溶液中浸泡3h后的聚吡咯膜在0.1mol/L NaCl中的循环伏安电流容量。图2给出了掺杂不同尺寸对阴离子的聚吡咯膜在碱环境中处理3h后的降解度。从图2可明显看出,掺杂小尺寸对阴离子的聚吡咯膜的降解度高达60%;随着掺杂离子尺寸的增大,其降解度逐渐降低;掺杂大尺寸对阴离子的聚吡咯膜的降解度仅为10%。
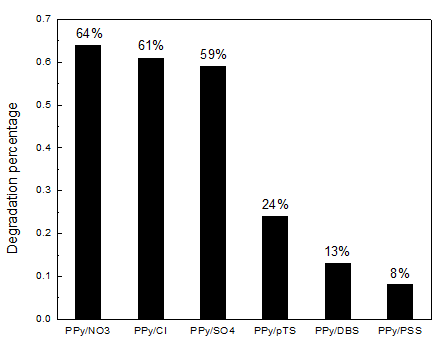
图2 掺杂不同尺寸对阴离子聚吡咯膜的降解度
表1为不同聚吡咯膜在降解前后膜本体电阻的变化。从表中可以看出,聚吡咯膜掺杂离子的尺寸越大,在碱性环境中降解3h后其膜本体电阻越小,即仍能保持良好的电导性。显然,上述结果表明,掺杂阴离子的尺寸越大,聚吡咯抗腐蚀的性能越好,在碱性环境中浸泡一段时间后,仍能保持良好的电化学活性和电导性。
表1 掺杂不同尺寸对阴离子聚吡咯膜降解前后膜本体电阻的变化(单位: Ω·cm-2)
| 聚吡咯膜 | PPy/NO3 | PPy/Cl | PPy/SO4 | PPy/pTS | PPy/DBS | PPy/PSS |
| 降解前 | 0.13 | 0.1 | 0.09 | 0.03 | 0.045 | 0.016 |
| 降解后 | 123 | 105.5 | 133.9 | 60 | 6.7 | 5.3 |
3.2 FTIR分析测试结果
为了了解掺杂不同尺寸对阴离子的聚吡咯膜在降解前后结构的变化,将新合成和碱处理后的聚吡咯膜从铂电极上剥离,朝向溶液的一面称之为膜表面,朝向铂电极的一面称之为膜内部,对膜表面和内部进行FTIR分析测试,其结果如图3示。
比较PPy/SO4膜在碱环境中降解3h前后膜表面和内部的FTIR谱图可知,降解后的聚吡咯膜表面和内部均在1700cm-1处出现明显的吸收峰,说明结构中C=O的存在,即发生了过氧化;而且3000cm-1左右范围内峰减弱甚至消失,说明过氧化造成的N和β-C上的去质子化。#p#副标题#e#
而对比PPy/PSS膜在碱环境中降解3h后前后膜表面和内部的FTIR谱图发现,在1700cm-1处膜表面出现吸收峰,而膜内部未出现,说明膜表面受到亲核基团的进攻而发生了一定的过氧化,但OH-并没有侵入膜内部结构,故其内部仍保持完好。
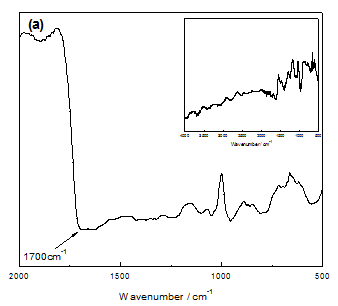
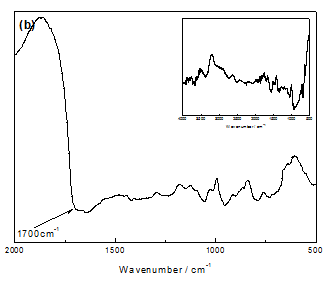
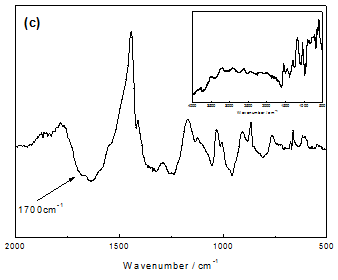
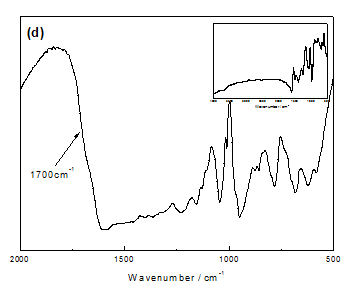
图3 不同聚吡咯膜在降解前(小图)后的红外图谱:(a)PPy/SO4膜表面;(b)PPy/SO4膜内部:(c)PPy/PSS膜表面;(d)PPy/PSS膜内部
3.3 XPS分析测试结果
掺杂不同尺寸对阴离子(SO42-,PSS-)的聚吡咯降解前后膜成分的变化通过XPS测试进行分析。图4为掺杂不同尺寸对阴离子的聚吡咯膜的N 1s XPS能谱及分峰拟合,表2是XPS测试结果的定量分析。
未经碱溶液降解处理的聚吡咯膜的N 1s XPS能谱由两个小峰组成,其结合能分别为399.6 eV和401.1 eV。结合能为399.6 eV的小峰表示聚吡咯主链上-NH-结构的N,401.1 eV结合能的小峰表示因形成极化子或双极化子而产生的带有正电荷的Nδ+。聚吡咯膜的掺杂度在一定程度上可以通过Nδ+/NTotal值进行衡量。碱溶液浸泡3h后的聚吡咯膜的N 1s XPS能谱由三部分组成,结合能分别是398.2 eV,399.6 eV和401.1 eV,其中398.2 eV结合能的峰表示降解去质子化=N-结构的N。由于掺杂离子中含有S元素,故S/NTotal值也可用来表征聚吡咯膜的掺杂度。
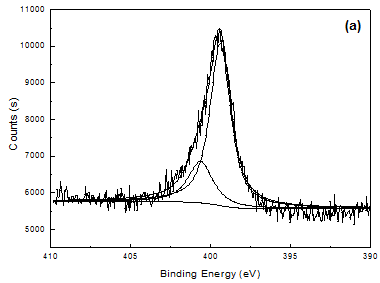
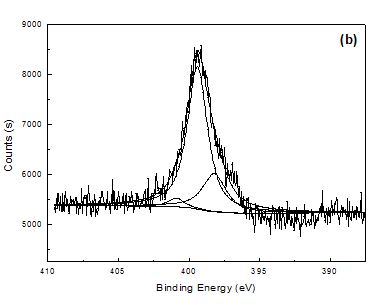
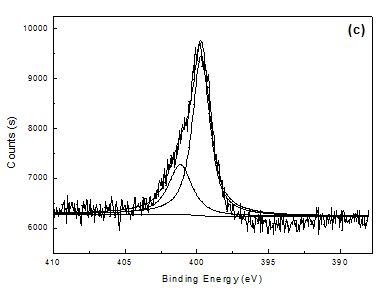
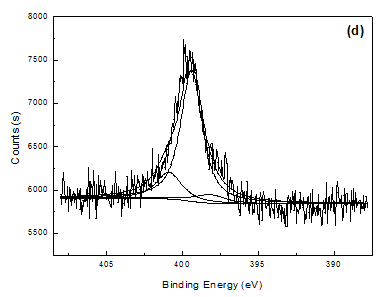
图4 不同聚吡咯膜的N 1s XPS能谱及拟合结果:(a)降解前PPy/SO4;(b)降解后PPy/SO4;(c)降解前PPy/PSS;(d)降解后PPy/PSS
通过表2可知,掺杂大尺寸对阴离子的PPy/PSS膜的掺杂离子含量在降解前后并未发生明显变化,而小尺寸对阴离子掺杂的PPy/SO4膜降解后,其S/NTotal值为0,原来的掺杂离子全部脱掺杂。通过比较掺杂不同尺寸对阴离子聚吡咯膜在降解前后Nδ+/NTotal和-N=/NTotal的值,也可得知PPy/SO4膜在碱性环境中比PPy/PSS膜降解更加严重。
表2 不同聚吡咯降解前后的Nδ+/N, -N=/N和S/N比率
| Sample | Nδ+/N | -N=/N | S/N |
| 新合成PPy/SO4 | 0.23 | — | 0.19 |
| 降解后PPy/SO4 | 0.03 | 0.23 | 0 |
| 新合成PPy/PSS | 0.29 | — | 0.44 |
| 降解后PPy/PSS | 0.17 | 0.08 | 0.44 |
在碱性溶液中,亲核的OH-可以与聚吡咯膜中的掺杂阴离子发生交换而侵入膜结构内部:PPy/A- + OH-= PPy/OH- + A- [11-12]。交换后的聚吡咯PPy/OH-膜非常不稳定,很容易被氧化生成带羰基的吡咯环,即发生了过氧化 [13]。但是,当掺杂对阴离子的尺寸很大时,其位阻效应也十分大,掺杂阴离子不容易从聚吡咯膜内脱出,很难与OH-进行交换,因此,亲核基团仅能进攻聚吡咯的表层结构而无法侵入膜内部,故具有很好的环境稳定性,如图5和图6所示。实验所得的FTIR和XPS分析数据结果也很好的证明了这一点。
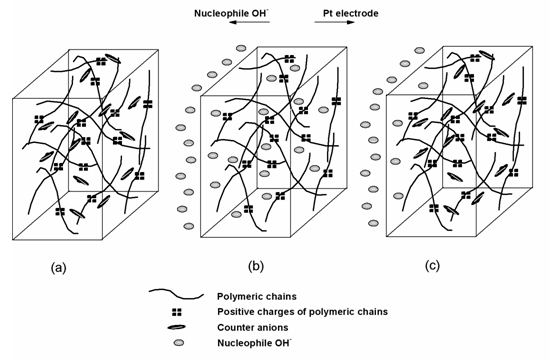
图5 不同聚吡咯膜降解过程结构变化示意图:(a)新合成聚吡咯膜;(b)掺杂小尺寸对阴离子聚吡咯膜处于碱性溶液中;(c)掺杂大尺寸对阴离子聚吡咯膜处于碱性溶液中
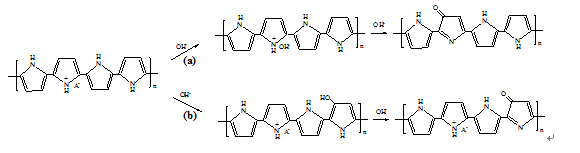
图6 不同聚吡咯膜降解过程反应机理:(a)掺杂小尺寸对阴离子聚吡咯膜;(b)掺杂大尺寸对阴离子聚吡咯膜
4 结论
聚吡咯膜中掺杂阴离子的尺寸越大,阴离子交换性越差,亲核的OH-难以与聚吡咯膜中的掺杂阴离子发生交换而侵入膜结构内部,聚吡咯抗腐蚀的性能越好,即使在碱性水溶液中浸泡后,仍能保持良好的电化学活性和电导性。
参考文献
[1] 朱道本, 王佛松. 有机固体 [M]. 上海: 科学技术出版社, 1999: 115-129
[2] 王国建, 刘琳. 特种与功能高分子材料 [M]. 北京: 中国石化出版社, 2004: 92-136
[3] 吴其晔, 冯莺. 高分子材料概论 [M]. 北京: 机械工业出版社, 2004: 233-241
[4] 孙酣经. 功能高分子材料及应用 [M]. 北京: 化学工业出版社, 1990: 54-94
[5] 肖纪美, 曹楚南. 材料腐蚀学原理 [M]. 北京: 化学工业出版社, 2002: 12-15
[6] G. Inzelt, M. Pineri, J.W. Schultze, M.A. Vorotyntsev. Electron and proton conducting polymers: recent developments and prospects [J]. Electrochim Acta 2000;45:2403-2421
[7] Z. Gao, M. Zi, B. Chen. The influence of overoxidation treatment on the permeability of polypyrrole films [J]. J Electroanal Chem 1994;373:141-148
[8] Q. Pei, R. Qian. Protonation and deprotonation of polypyrrole chain in aqueous solutions [J]. Synth Met 1991;45:35-48
[9] K.G. Neoh, T.T. Young, E.T. Kang, K.L. Tan. Structural and mechanical degradation of polypyrrole films due to aqueous media and heat treatment and the subsequent redoping characteristics [J]. J Appl Polym Sci 1997;64:519-526
[10] S. Li, Y.B. Qiu, X.P. Guo. Influence of doping anions on the ion exchange behavior of polypyrrole [J]. J Appl Polym Sci 2009;114:2307-2314
[11] Y. Li, R. Qian. Stability of conducting polymers from the electrochemical point of view [J]. Synth Met 1993;53:149-154
[12] Y. Li, R. Qian. On the nature of redox processes in the cyclic voltarnmetry of polypyrrole nitrate in aqueous solutions [J]. J Electroanal Chem 1993;362:267-272
[13] Y. Li, R. Qian. Electrochemical overoxidation of conducting polypyrrole nitrate film in aqueous solutions [J]. Electrochim Acta 2000;45:1727-1731

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62313558-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414




