摘要
采用电化学测试方法研究了不同Cl-浓度下,304不锈钢在两种模拟混凝土孔隙液中的点蚀行为,确定了304不锈钢的临界Cl-浓度;采用SEM观察了304不锈钢表面钝化膜在临界Cl-浓度前后的状态。结果表明,通过动电位极化和恒电位阻抗方法确定了304不锈钢的临界Cl-浓度,且数值基本一致,并SEM观测结果相一致;而开路电位下的阻抗测试并不能确定临界Cl-浓度。
关键词: 304不锈钢 ; 模拟混凝土孔隙液 ; 临界Cl-浓度 ; 点蚀
Cl-对碳钢的腐蚀已被广泛认为是导致钢筋混凝土结构过早破坏的主要原因之一。针对这一问题,相关学者提出了许多改善钢筋混凝土质量的策略和措施,一些研究者已经开始研究不锈钢钢筋在模拟混凝土孔溶液中的腐蚀行为。Freire等[1,2]研究了碱性溶液 (NaOH+KOH) 中AISI 304和316不锈钢上钝化膜的电化学行为和化学成分,结果表明,溶液pH和Cl-浓度对两种不锈钢的膜组成和腐蚀行为有重要影响。Moser等[3]研究了几种高强度不锈钢在模拟混凝土溶液中的耐蚀性,表明这些材料在含有Cl-的碱性溶液中均表现出较高的耐蚀性。
不锈钢的临界点蚀条件一直是腐蚀研究的热点。Frankel[4]总结了影响金属点蚀的关键因素,包括合金成分、环境、电位和温度等,列出了几种不锈钢允许的最高温度和氯化物浓度,以避免在氯化物中出现点蚀。对这些临界条件的研究有助于阐明点蚀形成和扩展机理,许多经典理论都是基于对临界点蚀条件的深入研究。Cl-作为最危险的点蚀影响因素之一,一直是研究人员关注的重点。Leckie和Uhlig[5]在1966年首次报道了电化学方法研究不锈钢的临界点蚀电位和Cl-活性的对数之间的线性关系。其它研究者也基于动电位极化曲线讨论了Cl-浓度对各种不锈钢的影响,包括AISI304,AISI 316L,LDX 2003,DSS 2205[6-8]。临界点蚀Cl-浓度 (CPCC) 是评价各种不锈钢在盐溶液中点蚀敏感性的较为直接的指标。2000年,Yang和Luo[9]通过在不同氯化物浓度的硼酸盐缓冲溶液中施加恒定电位,研究了氯化物对阳极电流密度的影响;并在此基础上,研究了不同充氢电流密度下的304不锈钢腐蚀的临界Cl-浓度。每一种不锈钢都有一个CPCC值,它可以像临界点蚀温度 (CPT) 那样用电化学方法测量[10],采用简便的电化学方法测定不锈钢的CPCC是十分必要和有意义的。本文采用动电位极化、电化学阻抗法和SEM等,研究了304不锈钢在不同模拟溶液下的临界Cl-浓度。
1 实验方法
采用的实验材料为304不锈钢,其化学成分 (质量分数,%) 如下:C 0.046、Si 0.57、Mn 1.22、P 0.046、S 0.005、Ni 8.01、Cr 18.06、Fe余量。模拟混凝土孔隙溶液为饱和Ca(OH)2溶液和HCO3-/CO32-溶液。溶液的初始pH是通过pH计直接测量得到,饱和Ca(OH)2溶液的pH为12.56;HCO3-/CO32-溶液由0.015 mol/L NaHCO3和0.005 mol/L Na2CO3组成,pH为10.07,选择这种溶液组成是为了模拟混凝土孔隙液碳化初期对304 SS点蚀行为的影响[11]。实验中所有使用的化学药品都为分析纯试剂。在整个实验过程中,溶液温度控制在 (23±2) °C。
将304不锈钢机械加工成尺寸为10 mm×10 mm×2 mm的试样,4个侧面用1500#的SiC砂纸打磨后再在60 ℃的硝酸钝化液中预钝化1 h,用铜导线焊接后,再用环氧树脂封在PVC管内以保证暴露于溶液中的工作电极面积为1 cm2。在进行电化学测试之前,先后用SiC砂纸依次湿磨至2000#,用酒精脱脂,在水中清洗,然后在冷空气中干燥。
在Zennium E电化学工作站上进行动电位极化测试、开路电位下阻抗测试和恒电位阻抗谱测试。采用三电极体系,铂片作为对电极,饱和甘汞电极 (SCE) 作为参比电极,工作电极 (WE) 是304不锈钢试样。动电位极化测量是在30 min的 OCP测试后获得的。扫描电位范围为-1.0~+1.0 VSCE,扫描速率为0.5 mV/s。
304不锈钢在两种模拟混凝土孔隙液中的开路电位下的电化学阻抗测试是在30 min的OCP测试后测得。交流电位幅度为10 mV,频率范围为105~10-2 Hz,并且通过Zsimpwin软件进行数据分析。
在饱和Ca(OH)2溶液中,将试样在+450 mVSCE的阳极电位极化1 h后测量电化学阻抗,在HCO3-/CO32-溶液中则将试样在+600 mVSCE的阳极电位极化1 h后测量电化学阻抗。交流电位幅度为10 mV,频率范围为105~10-2 Hz,并且通过Zsimpwin软件进行数据分析。所有电化学测试均在室温 (23±2) ℃下进行,并至少重复3次以确保实验的可重复性。
304不锈钢在除去表面钝化膜后,在两种不同测试溶液中的临界Cl-浓度前后分别对试样进行恒电位极化1 h,最后使用JSM-6700F扫描电子显微镜 (SEM) 对表面形貌进行观察。
2 结果与讨论
2.1 动电位极化曲线分析
304不锈钢在具有不同Cl-含量的饱和Ca(OH)2溶液和HCO3-/CO32-碱性溶液中的动电位极化曲线如图1所示。在饱和Ca(OH)2溶液中,添加各个浓度的Cl-之后,所有样品的腐蚀电位基本都是集中在-500 mVSCE。当Cl-浓度从0增加到0.2 mol/L时,从腐蚀电位到+400 mVSCE时,钝化电流密度先增大并出现一个峰值,然后出现二次钝化区。在这个Cl-浓度范围内,只观察到钝化行为,材料表面形成的钝化层保护钢材免受侵蚀[8],点蚀未发生,这表明并未达到临界Cl-点蚀浓度。当电位上升到较高水平时,电流迅速增加,这是由于析氧反应引起的[12]。304不锈钢在析氧前保持了良好的钝性,随着氯化物浓度的增加,钝化区宽度显著降低。结果表明,样品的点蚀敏感性明显提高。当Cl-浓度从0.2 mol/L提高到1 mol/L时,直至钝化膜的发生破裂,样品表面开始出现点蚀。当溶液中添加的Cl-浓度大于0.2 mol/L时,就可能出现点蚀。不锈钢表面的点蚀电位是最广泛报道的临界条件之一,超过点蚀电位会形成稳定的点蚀[6],随着Cl-浓度的提高,点蚀发生所需要的时间与电位变低[13]。在饱和Ca(OH)2溶液中,在钝化区出现了一些明显的电流波动,这是由于在稳定点蚀之前发生了亚稳态点蚀[14,15]。

图1 304不锈钢在含氯化物饱和Ca(OH)2溶液和HCO3-/CO32-碱性溶液中的极化曲线及临界Cl-浓度
在HCO3-/CO32-碱性溶液中,各个Cl-浓度下的腐蚀电位都集中在-300 mVSCE。当Cl-浓度从0增加到0.05 mol/L,从腐蚀电位到+400 mVSCE时,304不锈钢依然出现过钝化溶解和二次钝化区,直至氧析出的发生未发现点蚀。当Cl-浓度从0.05 mol/L提高到2 mol/L时,钝化电流密度一直增加,直至钝化膜发生破裂,点蚀坑出现。HCO3-/CO32-碱性溶液中的样品在Cl-浓度达到0.05 mol/L后,可能出现点蚀。而且随着Cl-浓度的升高,点蚀发生所需要电位变低,在Cl-浓度达到2 mol/L时,点蚀电位达到最低的+200 mVSCE。
304不锈钢钢筋在没有到达临界Cl-浓度的模拟混凝土孔隙液中会直接进入钝化状态,钝化区范围比较大,如果没有发生击破,一直到氧析出时,电流密度才明显升高[16]。当到达临界Cl-浓度时,钝化区范围变窄,在远低于氧析出电位处,电流值会突变增加,钝化膜破裂,点蚀电位明显负移[17]。
从图1c中不同Cl-浓度下的点蚀电位看出,在饱和Ca(OH)2溶液中,Cl-浓度在0.2 mol/L及以下时,可以看到样品未出现点蚀电位,而在0.3 mol/L时,出现了点蚀电位;同样的,在HCO3-/CO32-碱性溶液中,Cl-浓度在0.05 mol/L及以下时,样品并不能出现点蚀坑,直到增加到0.1 mol/L时,才会出现点蚀电位。综上所述,在饱和Ca(OH)2溶液中样品的点蚀发生临界Cl-浓度为0.2~0.3 mol/L,而在HCO3-/CO32-碱性溶液中样品的点蚀发生临界Cl-浓度为0.05~0.1 mol/L。
2.2 开路电位下阻抗分析
为了研究Cl-对模拟混凝土孔隙液中304不锈钢钝化膜结构性能的影响,在饱和Ca(OH)2溶液和HCO3-/CO32-碱性溶液中进行开路电位下的EIS测试,结果如图2所示。所有的阻抗曲线呈半圆弧状,表明304不锈钢在不同Cl-浓度下的两种模拟混凝土孔隙液中的成膜机制相同,Cl-含量的变化对阻抗弧形状的变化产生明显的影响。从图中可以看出,随着饱和Ca(OH)2溶液中Cl-浓度的不断增加,直到0.1 mol/L,容抗弧的半径逐渐减小;Cl-浓度从0.1到0.3 mol/L时,容抗弧的半径基本不变;然而当Cl-浓度逐渐从0.3 mol/L增加到0.7 mol/L时,容抗弧半径又逐渐增大;此后,在测试浓度范围内随着Cl-浓度的增加,容抗弧又基本保持不变。在HCO3-/CO32-碱性溶液中,随着浓度的不断增加,容抗弧半径逐渐减小;当Cl-浓度高于1 mol/L后,容抗弧半径又增大。经过以上分析可知,开路电位下的EIS不适合测试304不锈钢的临界Cl-浓度,这是由于点蚀的萌生和扩展是一个非常漫长的过程,短暂的开路电位测试之后的阻抗测试不能得到点蚀发生的临界Cl-浓度。此外,开路电位未达到304不锈钢的保护电位,所以继续采用恒电位下的阻抗来快速评价。
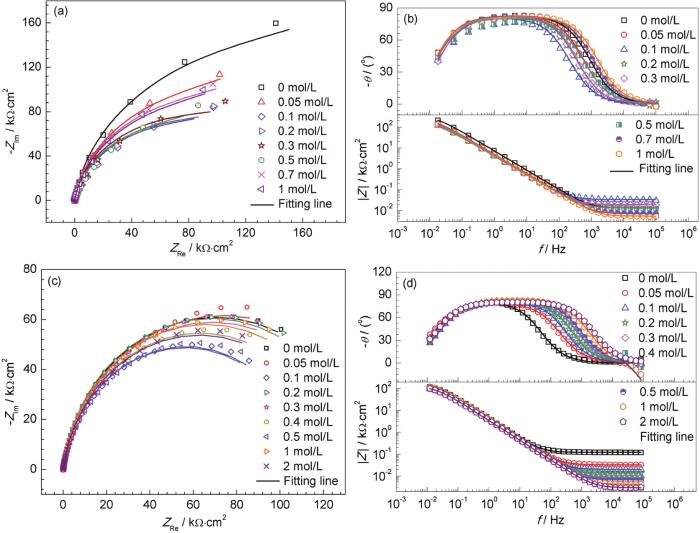
图2 304不锈钢在含不同Cl-浓度的饱和Ca(OH)2溶液和HCO3-/CO32-碱性溶液中的开路电位下EIS图
2.3 恒电位下阻抗分析
根据动电位极化曲线确定不锈钢的钝化区间,选择合适的钝化电位。在饱和Ca(OH)2溶液中,304 不锈钢在阳极电位+450 mVSCE下极化1 h后的EIS测试结果如图3a所示。在HCO3-/CO32-碱性溶液中,304不锈钢在阳极电位+600 mVSCE下极化1 h后的EIS测试结果如图3c所示。Nyquist图均由一段容抗弧组成,随着Cl-浓度的增加,容抗弧的半径有所改变,阻抗谱的高频区表征的是电解液和电极表面电阻的信息,低频区对应的是腐蚀过程中电化学反应的电荷转移电阻的大小。
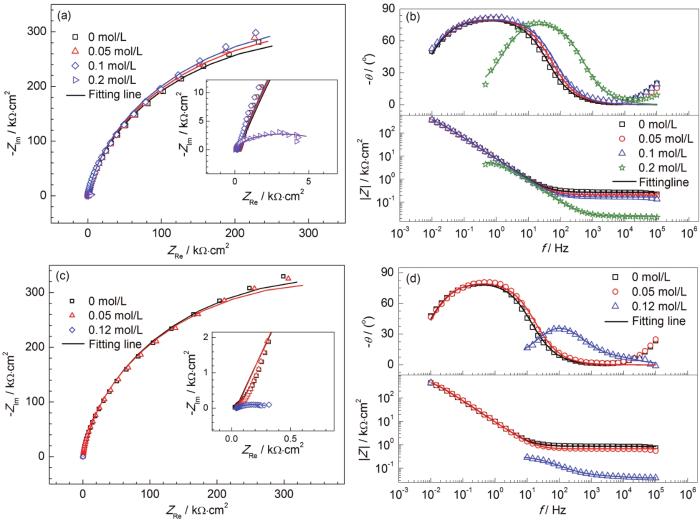
图3 304 不锈钢在含不同Cl-浓度的饱和Ca(OH)2和HCO3-/CO32-碱性溶液中的恒电位下EIS图
在饱和Ca(OH)2溶液中,304不锈钢的Nyquist图呈现出的是一段圆弧,容抗弧的半径不同,0、0.05和0.1 mol/L的Cl-浓度下的样品差距不大,对应的时间常数基本相同,此时不锈钢处于钝化状态[18]。由于容抗弧半径的大小直接反映了金属电极表面电荷转移电阻的大小,电阻越大,腐蚀速率越小。当Cl-浓度达到0.2 mol/L时,容抗弧发生了明显变化,半径远远小于其他的浓度。此时界面电阻值较小,样品的腐蚀速率加快。这表明钝化膜的破裂以及点蚀的发生,即已经超过发生点蚀的临界Cl-浓度;Bode图中,0.2 mol/L Cl-浓度下样品的阻抗模值最低,而且其出现了不同的时间常数,阻抗数值不再向低频区移动,说明腐蚀已经发生。
在HCO3-/CO32-碱性溶液中,0和0.05 mol/L的Cl-浓度下的样品的容抗弧半径相差不大,处于钝化状态;当Cl-浓度达到0.12 mol/L时,容抗弧半径急剧减小,同样说明此时Cl-浓度超过临界值以及点蚀的发生。而在Bode图中,0和0.05 mol/L Cl-浓度下,304不锈钢没有点蚀发生,而且其阻抗模值也比0.12 mol/L Cl-浓度下的样品高。阻抗值或容抗半径的显著下降是点蚀的标志[19]。
在这两种模拟溶液中,均出现了低频区阻抗数据的缺失。这是因为腐蚀已经发生,且速率很快,仪器未能输出结果,所以阻抗结果未能呈现出低频区的数据。综上所述,304不锈钢在饱和Ca(OH)2溶液中的点蚀发生临界点蚀Cl-浓度是在0.1~0.2 mol/L,而HCO3-/CO32-碱性溶液中的点蚀发生临界点蚀Cl-浓度是0.05~0.12 mol/L。
用于模拟EIS结果的等效电路图如图4所示,根据该模型提取的参数如表1所示。可以看出,在比较低的Cl-浓度下,304不锈钢表面为完整钝化膜,可以采用如图4a中的简单等效电路拟合。当溶液中的Cl-浓度超过临界值时,钝化膜表面会形成稳定的点蚀坑,其等效电路与低于临界Cl-浓度时的电路不同。此时可以将表面分为两个可区分的部分,即钝化表面和点蚀区域。在钝化表面处,所提出的电路类似于低于临界Cl-浓度时的电路。然而,在表面存在稳定点蚀的情况下,增加了一个与钝化表面平行的物理单元 (点蚀)。同时采用CPEpit、Rpit和Ri 3个元件对稳态点蚀进行拟合,它们分别代表了表面与坑内溶液界面形成的双电层结构、与点蚀坑有关的电荷转移电阻和点蚀坑内溶液电阻。在这些模型中,引入了频率相关的恒定相位元件 (CPE) 而不是纯电容 (C),以解释界面上存在的不均匀性[20],CPE用于更准确地分析双电层的阻抗行为。
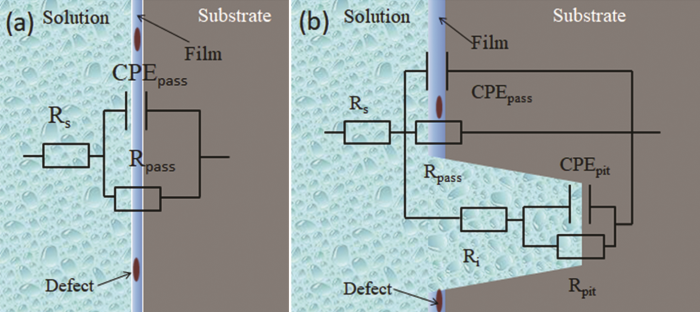
图4 低于临界Cl-浓度和高于临界Cl-浓度的等效电路模型
表1 304 不锈钢在不同模拟混凝土孔隙液中的EIS拟合参数
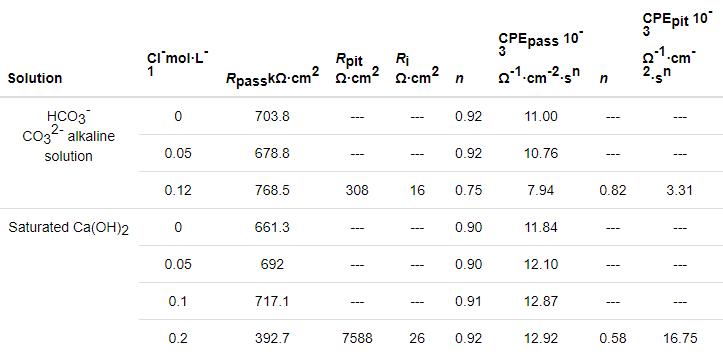
从表1可以看出,在饱和Ca(OH)2溶液中,当低于临界Cl-浓度时,随着Cl-浓度增加,Rpass的增大可能是由于离子通过钝化膜的扩散减少,这表明钝化膜受高碱性环境的保护。而在HCO3-/CO32-碱性溶液中,则出现相反的结果,Rpass的减小可能是由于离子通过钝化膜的扩散增加,这表明钝化膜上的缺陷增加。此外,n值的变化也表明了Cl-对钝化层均匀性产生了影响[21]。
临界Cl-浓度可以认为是Rtotal急剧下降时的氯离子浓度。当Cl-浓度低于临界Cl-浓度时,Rtotal的值与Rpass相同。而当Cl-浓度高于临界Cl-浓度时,Rtotal的计算公式如下:

式中,Rtotal是总电阻,Rpit是电荷转移电阻,Ri是点蚀坑内的溶液电阻,Rpass是膜电阻。
图5显示了在两种模拟混凝土孔隙液中304不锈钢钝化膜上的Rtotal值 (根据表1中的数据计算) 随Cl-浓度的变化。可以看出,对于饱和Ca(OH)2溶液,Rtotal的急剧下降发生在0.1~0.2 mol/L之间,对于HCO3-/CO32-碱性溶液,这种急剧下降在0.05~0.12 mol/L之间。综合恒电位阻抗法和动电位极化法的结果,可以看出恒电位阻抗法与动电位极化法的结果密切相关,说明恒电位阻抗法可以作为不锈钢临界Cl-浓度的测定方法。
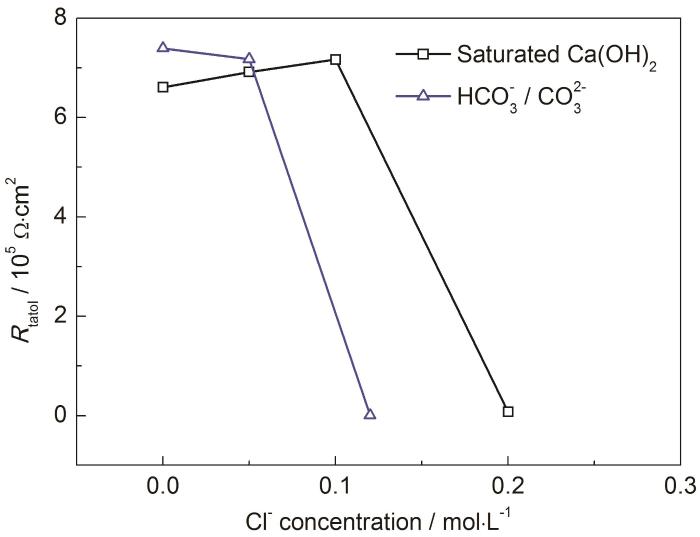
图5 在不同模拟混凝土孔隙液中304不锈钢的Rtotal值随Cl-浓度的变化曲线
2.4 腐蚀形貌的SEM观察结果
分别对在含0.1和0.2 mol/L NaCl的饱和Ca(OH)2溶液中的304不锈钢进行恒电位极化测试之后,在SEM下观察试样的表面形貌。同样,对304不锈钢在含0.05和0.12 mol/L NaCl的HCO3-/CO32-碱性溶液中进行1 h的恒电位极化测试,分析试样的表面微观形貌,结果如图6所示。可以明显的观察到,含有不同Cl-浓度的两种溶液中,在尚未达到临界Cl-浓度之前,304不锈钢试样表面没有任何明显的点蚀坑;当溶液中Cl-浓度超过临界值时,试样的表面出现了非常明显的点蚀坑。SEM观察结果进一步证实了恒电位下阻抗谱所得出的结论。

图6 在不同模拟混凝土孔隙液中304 不锈钢恒电位极化后的SEM像
3 结论
(1) 304不锈钢在不同的模拟混凝土孔隙液中进行动电位极化测试结果表明,在饱和Ca(OH)2溶液中,点蚀发生的临界Cl-浓度在0.2~0.3 mol/L之间,而在HCO3-/CO32-碱性溶液中是0.05~0.1 mol/L之间。
(2) 在两种不同的模拟混凝土孔隙液中的恒电位阻抗谱结果表明,304不锈钢在饱和Ca(OH)2溶液中,点蚀发生的临界Cl-浓度是0.1~0.2 mol/L之间,而在HCO3-/CO32-碱性溶液中的点蚀发生的临界Cl-浓度是在0.05~0.12 mol/L之间。与动电位极化所得的临界Cl-浓度相对一致,SEM的测试结果同样证明了这一结论。
(3) 304不锈钢的开路电位下和恒电位下的阻抗测试结果表明,恒电位下的阻抗测试可以作为判定304不锈钢临界Cl-浓度的方法,而开路电位下的阻抗测试不适合。
参考文献
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414





