海洋钢结构保护中广泛应用牺牲阳极阴极保护法。被保护体在阴极保护初期需要的电流密度远大于整个保护周期[1,2],而保护初期的时间占整个保护周期的时间较少,所以在采用普通牺牲阳极进行保护时,造成了资源浪费和被保护体承载过大的问题。有人提出采用镁铝型复合阳极来解决保护初期需求高电流密度而后期需求较低电流密度的矛盾[1],但Mg存在不宜加工和易燃的问题。近年来已出现关于高活性铝基牺牲阳极的研究报道,即在普通铝合金牺牲阳极基础上,添加合金元素作为活化点,促进阳极的溶解,从而避免阳极表面钝化,提供更负的电位。
文献[3]对元素周期表中的各种元素对铝合金牺牲阳极在海水中综合性能的影响进行了研究,结果表明,Zn、In、Ga、Mg、Sn、Bi、Ti、Ba等元素可使铝阳极电位负移,从而对其表面的活化溶解具有促进作用,这些元素的原子能够部分地取代铝晶体中晶格上的Al原子,成为铝氧化膜的缺陷部分,促使铝合金基体的活化溶解。与此同时,这些高活化合金元素能够使铝合金基体的稳定性提高,从而细化和均匀合金内部组织结构。之后许多学者[4,5,6,7,8,9,10,11,12,13,14,15,16,17,18]研究发现In、Ga、Sn、Mg等元素可以使阳极活化,也有学者对其活化机理进行了研究。但都是对单一活化元素进行研究,没有考虑到活化元素之间的相互作用。因此,有必要设计一种新的活性阳极,对比各元素对阳极性能的影响,得出阳极性能优异的配方,为复合阳极的研究提供设计参数。
1 实验方法
参照国家标准GB-T17848-1999加速试验法,采用天然海水,阳极试样尺寸为Φ25 mm×45 mm,其工作面积为14 cm2。称重。通电流前连续3 h测量其开路电位。使用恒电流仪按照表1控制恒定电流。
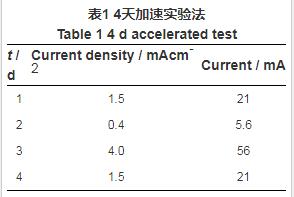
实验过程中测量极化电位,观察牺牲阳极形貌。测试结束后,断掉电流,测量其开路电位,连续1 h。将试样浸泡在68%的浓硝酸中5~10 min除去表面腐蚀产物,再用蒸馏水冲洗干净,然后放入烘箱内 (105±2) ℃下烘烤30 min,恒重,铜电量计同样操作。
按照下式计算实际电化学容量:
![]()
式中,Q为牺牲阳极试样实际电容量,(A?h)/kg;k为系数,k=843.3(A?h)/kg;M1和M2为实验前后铜电量计阴极铜片质量,g;m1和m2为实验前后阳极试样质量,g。
理论电容量计算方法:
Q=A⋅X+B⋅Y+C⋅Z+⋯⋯
式中,Q0为牺牲阳极的理论电容量,(A?h)/kg;A,B、C分别为合金元素的质量分数,%;X,Y和Z分别为合金元素的理论电容量,(A·h)/kg。
牺牲阳极电流效率:
![]()
极化曲线测试和电化学阻抗测试均采用IM6e电化学工作站,以铂片作为对电极,饱和甘汞 (SCE) 作为参比电极,实验介质为天然海水。将试样加工为直径为1 cm的牺牲阳极为工作电极,实验前用环氧树脂涂封,金相砂纸打磨后经无水乙醇除油。极化曲线采用恒电位法,电位扫描范围-200~300 mV (vs OCP),扫描速率为0.5 mV/s。电化学阻抗测试在开路电位进行,采用振幅为10 mV的正弦微扰信号,频率范围为105~10-2 Hz,自高频向低频扫描。
实验用钢板放置在全浸区,钢板上固定的监测探头采用无液界全固态Ag/AgX参比电极,实验前与饱和甘汞电极进行校正。使用全自动数据采集器采集阳极发出电流、工作电位和钢板不同位置的保护电位,设定采集时间间隔为5 min。实验过程中记录海水温度。钢板为边长1 m的正方形,监测探头分别安装在钢板中心、最远角以及两者之间连线的中间位置。
采用阴阳极面积比分别为50∶1,100∶1,200∶1和300∶1四种情况。实验周期分别为18,18,6和6 d。实际电化学容量 ((A?h)/kg) 根据电流时间积分除以消耗量来计算。
2 结果与讨论
2.1 铝合金活性阳极配方筛选
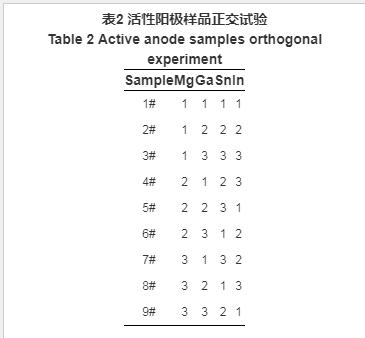
采用四因素三水平拉丁正交试验优化合金成分。正交试验成分设计如表2。Mg质量分数 (%) 对应的三水平分别为0.5,1.0和1.5;Ga质量分数分别为0.04,0.05,0.06;Sn质量分数分别为0.075,0.1和0.125;In质量分数分别为0.01,0.02和0.03,其余为Al。各个元素含量范围的选取是在前期大量实验基础上完成的,超出范围就表现为完全失控。确定一系列配方之后按照常规冶炼方法制作,炼制成型后检测其真实含量是否与配方有偏差,合格成品留用。采用4 d加速实验测定上述9组牺牲阳极的开路电位、闭路电位和电化学容量,计算电流效率,结果见表3。
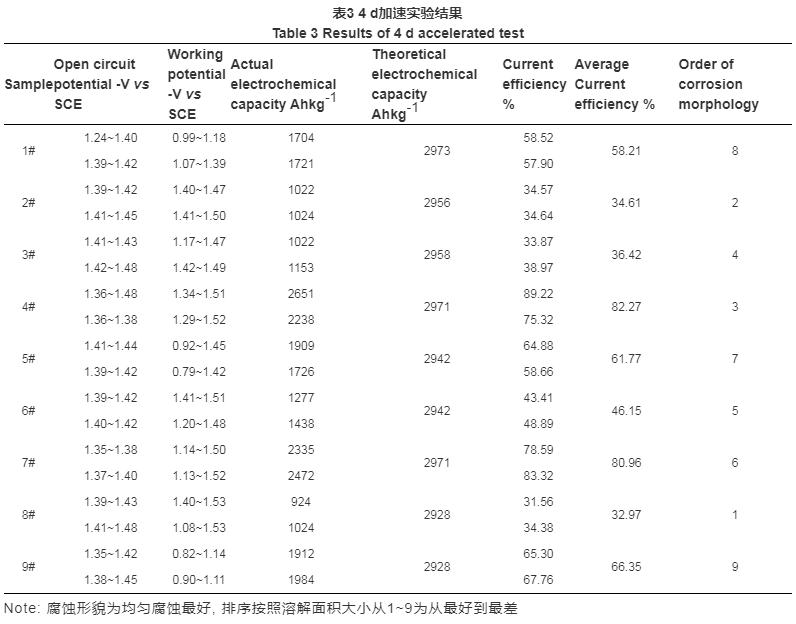
由表3可以看出,开路电位达到了-1.20 (V vs SCE) 以下,除9#外,各组实验阳极的工作电位都较负,符合活性阳极的基本要求。其中4#、7#电流效率最好,达到80%。8#、2#腐蚀溶解均匀,腐蚀形貌最佳。图1是9组样品4 d加速实验后的溶解形貌。

图1 9组牺牲阳极腐蚀形貌
从图1中看出,大部分阳极腐蚀均匀,腐蚀产物易脱落,形貌较好,其中8#、2#阳极溶解形貌最好,只有1#不易溶解。
分别以电流效率和溶解形貌为目标值进行正交试验的单因素分析。图2是以电流效率为目标值的单因素趋势图,图3是以溶解形貌为目标值的单因素趋势图。由图2可知,电流效率随Mg含量和Sn含量升高,先升高再降低;随Ga含量和In含量升高,先降低再升高。由图可以得到最佳配方水平为:2Mg-1Ga-2Sn-1In。
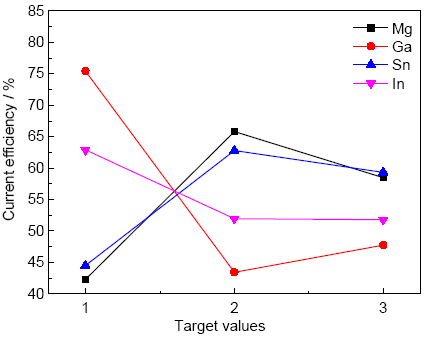
图2 以电流效率为目标值的单因素趋势图
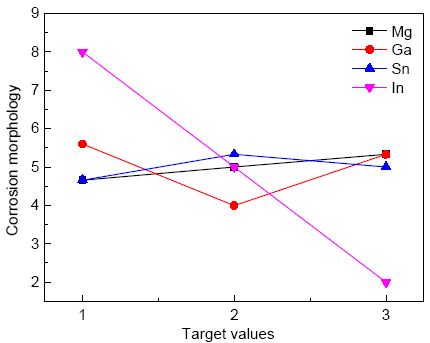
图3 以腐蚀形貌为目标值的单因素趋势图
由图3可知,牺牲阳极腐蚀形貌随着Mg含量的升高而变坏,随着Ga含量的升高先变好后变坏,随着Sn含量的升高先变坏后变好,随着In含量的升高逐渐变好。由图可以得到最佳配方水平为:1Mg-2Ga-1Sn-3In。
可以看出,分别以电流效率和溶解形貌为目标值获得的最佳配方是有差别的。牺牲阳极的使用过程中,既要求有高的电流效率也要求均匀的溶解形貌,两者缺一不可。在阳极溶解性能良好的情况下,稍低的电流效率也是允许的。权衡两者,在最佳配方研究的基础上设计了实海实验用配方。按照4 d加速实验的测试方法,对这3种阳极试样进行电化学性能测试,得到4 d加速实验结果 (见表4) 和腐蚀形貌 (见图4)。
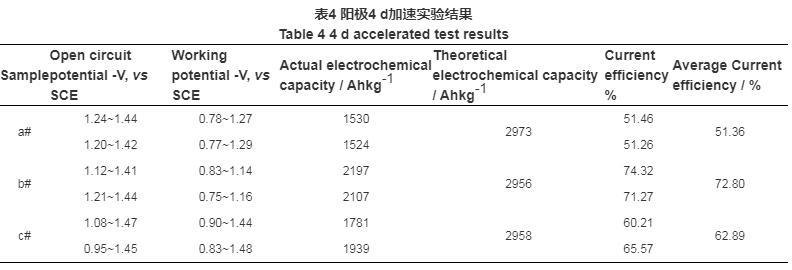

图4 优选阳极腐蚀形貌
由表4和图4可以看出,经过筛选所取得的3种配方的阳极开路电位和工作电位均符合高活化阳极的要求,阳极腐蚀均匀。
对实海实验用阳极c#进行了极化曲线和电化学阻抗测定,分别考察在天然海水中,自腐蚀浸泡0,4 和8 h的阳极性能,得到极化曲线图和Nyquist谱图见图5和6。
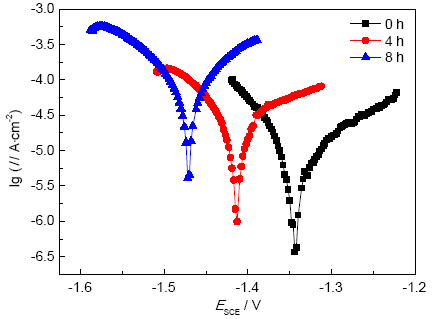
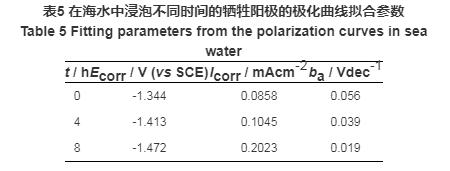
图5 活性阳极在海水中的极化曲线
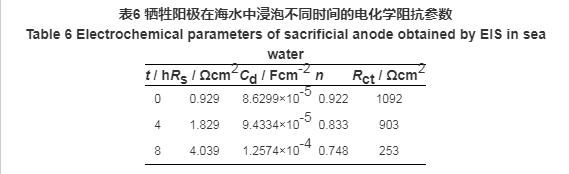
图6 活性阳极在海水中的Nyquist图谱
从极化曲线中可以看出随着浸泡时间的增长,电位出现了小幅度的负移,阳极保证了较负电位;同时,阳极始终处于活性溶解状态,表明阳极易溶解,无钝化现象。腐蚀电位与腐蚀电流密度增大,这说明阳极发挥了良好的活性。从表5数据可以看出,随着浸泡阳极Tafel斜率减小,活化溶解趋势增加。
从Nyquist阻抗谱图可以发现,电化学阻抗图谱表现为典型的单一容抗弧特征,表6是根据典型电化学溶解机制对应的单一容抗弧,即三元件等效电路图拟合结果。由图和数据可知,随着浸泡时间的增加,高-中频容抗弧随之减小,说明阳极表面的腐蚀溶解是不断加强的,Rct随之减小,表明阳极活性增大,这正是活性牺牲阳极需要的性质。溶液电阻Rs差距较大,可能的原因是阳极溶解产物没有及时脱落,部分保留在阳极表面。
2.2 活性阳极实海电化学性能
采用阴阳极面积比为300∶1、200∶1、100∶1、50∶1,考察活性阳极的电化学性能。其中,阴阳极面积比为300∶1、200∶1时,因为阳极体积较小,活性高,实验时间较短,实验时间为6 d,其它为18 d。海洋环境中的温度在22~28 ℃。
电极电位是表示保护状态的重要参数之一,实验得到4组实验的电极电位,见图7。
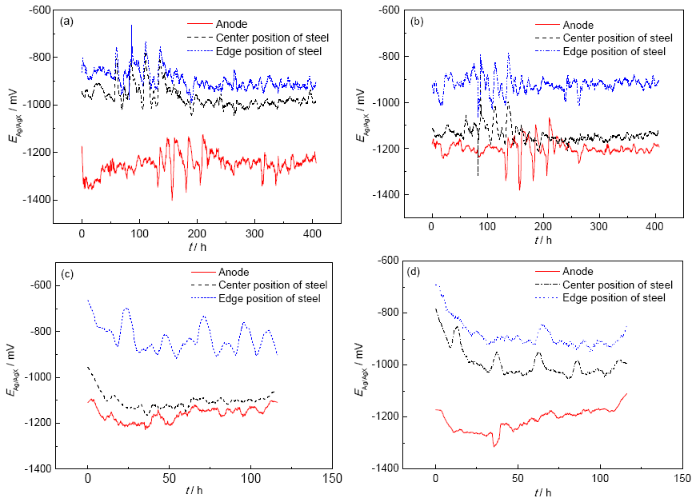
图7 活性阳极工作电位随时间变化曲线
从钢板上的2、3位置的电位随时间变化 (为平滑后的曲线) 可以看出,近阳极区,也就是钢板中心2电位最负,远阳极区3电位稍正;由图7可知,最远端的电位也较负,说明钢板达到了有效地的保护。阳极电位前期处在一个较负电位,随着极化推进,阳极电位正移,最后稳定。钢板中心和边缘的电位随着阴阳极面积比的增大而正移。表7中列入活性阳极电位在初始阶段和末尾阶段数值。
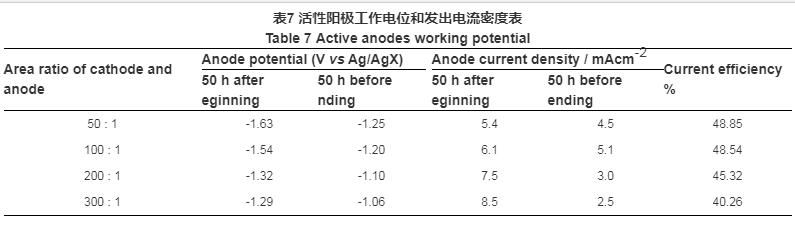
由表7可知,不同阴阳极面积比的活性阳极的工作电位在短暂的阳极极化后,都达到了高活化阳极要求的工作电位,初始极化能力较好。其中阴阳极面积比为50∶1时的初期电位为-1.63 (V vs Ag/AgX,下同),阴阳极面积比为100∶1时的初期电位为-1.54 V,阴阳极面积比为200∶1时的初期电位为-1.32 V,阴阳极面积比为300∶1时的初期电位为-1.29 V。随着活性阳极的不断消耗,电位逐渐正移。在这一过程中,牺牲阳极存在着强烈的阳极极化,然后处在一个较平稳的电位,随着阴阳极面积比由小到大,依次为-1.25,-1.20,-1.10和-1.06 V,均较负。
由表7中可以看出,阳极电位随阴阳极面积比的增大而负移。根据Crennell (McCoy) 公式可知,阳极表面积增大时,接水电阻减小,同时强极化时,驱动电位高,均造成阳极发出电流较大,可以快速形成石灰质垢层,进而降低了对保护电流的需求。综上可知,对于相同阳极材料来说,随着阳极暴露面积的增大,阳极初始发出电流增大,钢板能够受到的保护也越好。
阳极的发出电流密度表征其工作状态,而阳极的电流效率是其重要的电化学性能。在应用中,阳极初始阶段发出的电流尤为重要。4种情况初始和终了电流密度数据,见表7后两列。
由表7可知,4组活性阳极初期电流密度均较大,随着阴阳极面积比的增大,阳极电流密度从5.4 mA/cm2增加到8.5 mA/cm2。随着时间的推移,活性阳极发出电流逐步减小,这是由于该实验所用阳极量足够大,被保护体达到完全保护,表面形成钙镁沉积层,阴极保护回路阻抗大幅度增大,所需保护电流减小的原因,最后处在一个较平稳的数值。初始大的电流形成了较好的石灰质垢层,使得末期电流减小。
由表7可知,随着阴阳极面积比的增大,活性阳极的电化学效率呈下降趋势。实海实验所得的电化学效率与实验室所得数据相比有所下降,说明大电流放电电流效率减小,且自放电过程与恒电流强制放电过程电流效率有所不同,而且实际海洋环境潮汐海流的影响,加速了阳极腐蚀产物的剥离。
考察活性阳极的阳极腐蚀形貌,可以从表观评价阳极性能,得到4种情况下腐蚀形貌,见图8。

图8 活性阳极实海实验后腐蚀形貌
由图8可知,活性阳极实验后,腐蚀形貌良好,腐蚀较为均匀,牺牲阳极表面均未呈现钝化迹象,属于活化溶解过程;阴阳极面积比较大 (200∶1,300∶1) 时,由于初期发出电流大,表面更均匀,未见堆积现象;阴阳极面积比较小 (50∶1, 100∶1) 时,实验周期长,消耗的更多,整体来看是在横截面方向溶解,但是均存在“肌瘤”,可能是腐蚀产物没有全部快速脱落造成的。
总之,4种情况下,活性阳极在初期都处在一个较负的电位,均负于-1.29 V (vs Ag/AgX/seawater),随着阴阳极面积比的增大,活性阳极的电流密度也随之变大,阳极电位随之正移,活性阳极的电流效率呈下降趋势,均大于40%。实验后,腐蚀形貌良好,腐蚀较为均匀。
3 结论
经过正交试验筛选,分别以腐蚀形貌和电流效率为参考标准,得到腐蚀形貌最优活性牺牲阳极和电流效率最优活性牺牲阳极。
(1) 由单因素分析可知,牺牲阳极腐蚀形貌随着Mg含量的升高而变坏,随着Ga含量升高先变好后变坏,随着Sn含量的升高先变坏又变好,随着In含量的升高逐渐变好。电流效率随Mg含量和Sn含量升高,先升高再降低;随Ga含量和In含量升高,先降低再升高。
(2) 综合考虑腐蚀形貌和电流效率,正交试验得出用于实海实验的铝合金活性牺牲阳极,其电位为-1.45 V (vs SCE),电流效率大于60%。经过电化学实验发现,其能保持长时间的活性,维持活化溶解,满足复合活性阳极所需的性能要求,完全适合作为复合阳极的活性阳极部分使用。
(3) 在实海实验中,阴阳极面积比为50∶1、100∶1、200∶1、300∶1时,活性牺牲阳极表现出较负的电极电位,均负于-1.10 V (vs Ag/AgX/seawater),随着阴阳极面积比的增大,活性阳极电位正移,电流密度变大。阳极腐蚀形貌良好,腐蚀较为均匀,除极端阴阳极面积比300∶1之外,电流效率均在45%以上。
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62313558-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414





