前言
《皇帝内经素问》说:“心者,君主之官,神明出焉”。心脏主血脉和神志,其重要意义不言而喻。然而,随着工作节奏的加快、生活压力的增加、日常运动的减少和社会老龄化的凸显,冠心病、动脉粥样硬化、主动脉瓣狭窄和主动脉瓣反流等心脏疾病的占比日益增加,也愈发年轻化。等心脏病变,人的心情大多如此:花落水流红,闲愁万种,无语怨东风!
随着科技的进步,外科开胸手术首见疗效,用于心脏病治疗。但是其创伤较大,加之患者年龄和体质的限制,常常有并发症多、恢复难和致死率高等不足。本着敬畏生命和技术革新的宗旨,历经多年努力,以冠状动脉支架、主动脉瓣瓣膜(如图1)为核心的介入治疗手术方兴未艾,逐渐取代外科开胸手术,成为治疗冠心病、主动脉瓣狭窄的“微创”选择。
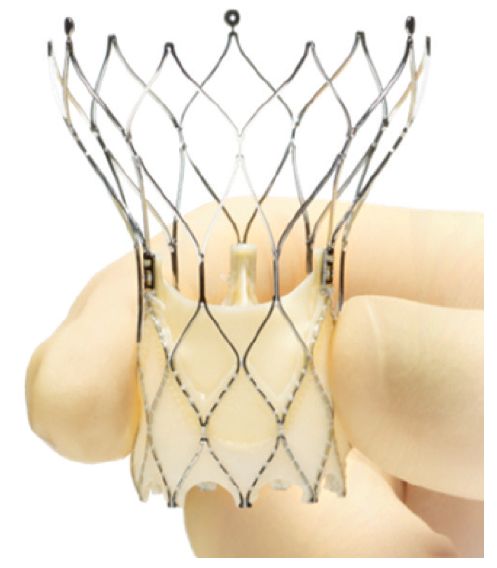
图1 主动脉瓣瓣膜
(金属支架+瓣叶)[1]
众所周知,水桶哪块板子短,哪里就容易漏水,这就是水桶的短板效应。金属材料的腐蚀也是如此,哪里容易和介质发生化学或者电化学反应,哪里就容易萌生腐蚀。支架的腐蚀不仅会造成表面损伤,诱发支架的疲劳断裂,还会导致局部镍(Ni)离子析出,产生生物毒性等危害身体健康的不良反应。
那么,植入心脏的金属支架的腐蚀是如何发生、控制和预防的呢?
1. 支架的选材和制造
以钙化性主动脉瓣狭窄为例,其显著影响心脏主动脉瓣的血流速度和通量,严重时危及生命。
主动脉瓣瓣膜支架不仅要有优异的力学性能,如撑开病变(如钙化狭窄)的血管,承受血管脉动引起的疲劳载荷(要求承受10年不少于3.8亿次脉动疲劳载荷),而且还要有良好的生物相容性,如组织排异性小,耐腐蚀性好,金属离子毒性小等。因此,支架材料经历了从奥氏体不锈钢、钴铬合金到钛镍合金(Nitinol)的演变。
特定成分的Nitinol经过适当的热处理,会产生早期支架材料所不具有的神奇性能——形状记忆效应和超弹性。形状记忆效应是高温定形的Nitinol经过低温塑性变形装入鞘管,输送到病变血管后经受血液加热升温,“记忆”恢复其高温形状的功能。超弹性是Nitinol中存在一种特殊的相变(应力诱发马氏体),使其最大可逆应变可达8%的神奇特性,而一般的金属材料其最大可逆应变不超过0.2%。形状记忆效应有利于将大直径的支架装入小直径的鞘管,超弹性既有利于支架在装载和释放过程中不发生塑性变形,也有利于实现脉动载荷下3.8亿次的应变疲劳寿命。
陶艺是将黏土制胚、烧结、打磨和上釉而成的工艺,考验制作者的审美和匠心。支架的制造也是如此!一枚小小的支架,需要先将Nitinol管材进行激光切割,然后机械研磨、热处理、喷砂,再进行酸洗、电解抛光等处理。成形之后,还需要进行外观、尺寸、力学和化学性能的品质检查,最后灭菌、抗钙化、消毒等,才能满足植入人体的条件。
像对待生命一样,对待每一个支架产品,这是每一个研发、制造、品质人员的使命和职责!
2. Nitinol合金支架的腐蚀问题
一般而言,电解抛光可以进一步降低支架表面粗糙度,提高表面光洁度,增加表面耐腐蚀能力和生物友好性。然而,腐蚀是一个吉布斯自由能降低的过程,就如倾斜的围墙,在条件具备的时候总能訇然坍塌,让人措手不及。
“君子不立于危墙之下”是孟子的智慧,其关键不是墙不能存在,也不是君子不能站在墙下?若如是,何来广厦万间,举家幸福。其核心在于“危”!这也是材料腐蚀科学与技术最核心的着力点。
成分、组织和处理工艺对金属材料的腐蚀和寿命有重要的影响[2]。增加材料在特定介质中的化学或者电化学稳定性,使其在规定的寿命周期内发生可预期、可控制和可接受的腐蚀,是腐蚀科学与技术的使命。虽然目标是明确的,手段是多样的,但是道路往往是曲折的,需要不断努力。
血浆是Nitinol支架植入体内后的主要腐蚀介质,其含有水、无机盐、纤维蛋白原、白蛋白、球蛋白、酶、激素、各种营养物质、代谢产物等,是一种复杂的生理电解质。
纵观Nitinol支架的腐蚀研究成果和临床反馈,重点考虑三种腐蚀形式:点蚀、电偶腐蚀和腐蚀疲劳。
2.1 点蚀
点蚀可以促进支架疲劳断裂的发生,也增加了Ni离子的氧化和离子释放,可能诱发组织炎性反应和癌变。
1999年报道的Nitinol主动脉支架的严重腐蚀引起了医疗行业对腐蚀的警觉,图2显示出严重的点蚀形貌。失效分析发现:表面氧化膜厚约0.2~0.3um,阳极极化点蚀击穿电位约280mV(SCE,下同)[3]。
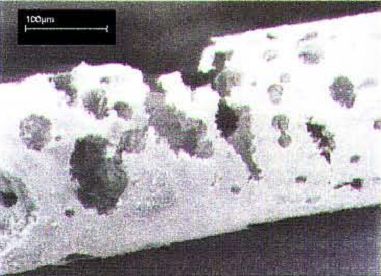
图2 Nitinol主动脉支架体内服役5个月的点蚀形貌[3]
经过电解抛光的Nitinol支架表面会形成一层薄而致密的TiO2,其增加了与血液接触的表层材料的电化学稳定性,保护基体材料免受腐蚀;也作为一种理化反应、物质传输的屏障,有效地避免了Ni的氧化和离子释放。如果TiO2中存在一定量的Ni原子,会导致其耐腐蚀性下降,Ni离子释放增加。
Nitinol支架中的夹杂物不仅促进疲劳裂纹的萌生,也会促进点蚀的萌生,且夹杂物的尺寸对点蚀萌生影响大于数量;热处理过程中产生的粗大析出相和带状偏析也会增加Nitinol支架材料的点蚀敏感性;电解抛光工艺对支架耐点蚀性能至关重要,但是当前还处于技术保密阶段。
Nitinol支架的点蚀评价主要采用循环动电位极化的方法,ASTM F2129指出点蚀评价是一种敏感性评价,建议测试溶液为PBS模拟生理溶液,每批样本量为7个,安全点蚀击穿电位大于+600mV,不安全点蚀击穿电位小于+300mV,介于+300~+600mV时需要增加样本进一步评价。
令人欣喜的是,对经过电解抛光的Nitinol支架进行循环动电位极化点蚀敏感性测试,当扫描电位高达+800mV时也不发生击穿。研究还发现Nitinol支架在Hank's模拟生理溶液中点蚀击穿电位约为316L不锈钢的3倍,且显示出持续的、瞬间的再钝化能力。
2.2 电偶腐蚀
支架在植入体内的过程中,需要借助显影设备CT。为了提高支架的显影性和定位性,常常在支架的挂耳位置增加显影性更好的贵金属,如铂Pt,金Au,钽Ta等。
显影点和支架之间会存在一定的电位差,在血浆中容易形成腐蚀电池,此时贵金属显影点为阴极,附近的支架材料为阳极,促使附近支架材料的活性溶解,产生电偶腐蚀和Ni离子溶出,甚至发生断裂的风险。
在Hank's模拟血浆中,Ta与Nitinol的腐蚀电位比较接近,而Au和Pt比Nitinol电位更正,有诱发电偶腐蚀的风险。因此,支架设计时需要在显影点和基材之间添加绝缘层,或者用绝缘材料包裹贵金属,这样可以有效地控制电偶腐蚀的发生。
2.3 腐蚀疲劳
腐蚀介质常常降低材料的疲劳极限,即腐蚀介质对疲劳有明显的促进作用,Nitinol支架也不例外。准确的讲,支架在血浆中的疲劳应该是腐蚀疲劳。
美国食品药品监督管理局FDA、欧盟统一安全认证CE、中国食品药品监督管理局CFDA和EN ISO 5840-3标准(心血管植入物-人工心脏瓣膜-第3部分:心脏瓣膜替代品经导管植入技术)均明确提出:血管内支架要有承受10年(心率72次/min)或3.8亿次脉动疲劳载荷而不发生断裂失效的能力。
Nitinol材料在空气、去离子水和Hank's模拟血浆中的疲劳裂纹扩展速率测试(37℃,R=0.1,f=10Hz)结果如图3所示:Paris公式的幂常数为3.0、2.8、3.1,结果相对接近[4]。EN ISO 5840-3也指出Nitinol支架的疲劳裂纹扩展速率对环境相对不敏感。
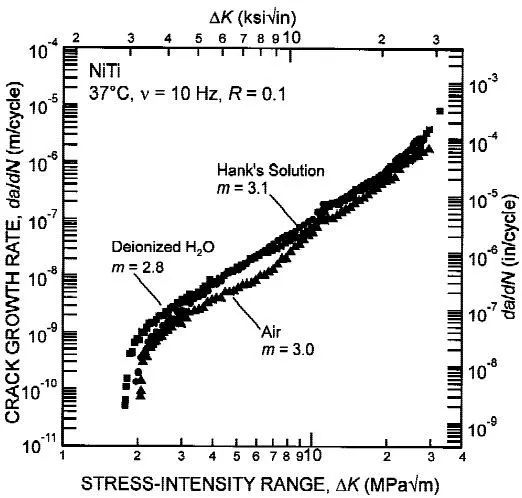
图3 Nitinol在空气、去离子水和Hank's溶液中的疲劳裂纹扩展测试[4]
然而,大多数支架的杆宽和壁厚约为几百微米,稳态腐蚀疲劳扩展区往往不超过断口面积的一半,所以其腐蚀疲劳寿命主要取决于裂纹的萌生。目前,切割、研磨、喷砂和扩径定形等表面机械损伤,酸洗、电解抛光等表面化学损伤(如点蚀坑)会增加局部表面应力集中,促进腐蚀疲劳裂纹萌生,且往往引起过早的疲劳断裂。因此,企业在制造和品检过程中会对支架的表面损伤进行严格的控制。
3. Nitinol支架腐蚀的控制
支架腐蚀的控制不能采用常规的阴极保护、牺牲阳极和添加缓蚀剂等措施,目前采用的耐腐蚀选料和表面处理(特别是电解抛光)配合的方法效果很好。
耐腐蚀支架选材经历了从奥氏体不锈钢、钴铬合金到Nitinol的发展,其耐腐蚀性能显著提升。TiO2表面膜的耐腐蚀性能远远优于Cr2O3。夹杂物尺寸对点蚀萌生的影响大于夹杂物数量,因此需要在订制管材时严格要求。
在425~450℃进行长时间的热处理,会形成粗大析出相和较严重的带状偏析,这也会增加Nitinol支架的点腐蚀敏感性。良好的电解抛光是提高Nitinol支架耐点蚀的重要工艺,经过有效的电解抛光,Nitinol支架表面形成薄而致密的TiO2膜,几乎不含有Ni,其在37℃的Hank's溶液中击穿电位可达+650mV,甚至达到+900mV,远大于316L不锈钢的+400mV。
需要注意的是:
工艺研发过程中,不应该片面追求通过提高电解抛光电位来提高表面光洁度,还应重视耐腐蚀的性能。因为过高的抛光电位会增加表面膜的缺陷,导致腐蚀的发生。
4. 腐蚀的利用
人们往往对金属腐蚀现象嗤之以鼻,但是金属的腐蚀难道真的一无是处?答案是否定的!
除了长期放置在体内的心脏支架(如主动脉瓣瓣膜支架)之外,有些支架(如冠状动脉支架)在完成血管矫正塑形(血管在几个月或者一年后恢复了正常的生理活性功能)后,其物理支撑作用的使命已完成,可以去除,但是外科手术目前难以做到,且较大创伤显而易见。那么有什么妙招可以去除支架呢?
腐蚀便是一个聪慧的手段。目前,很多冠状动脉支架使用可降解的镁锌合金,通过在血浆中发生均匀腐蚀而溶解,产生的离子被人体吸收作为微量元素,产生的微小碎块被巨噬细胞吞掉然后代谢,从而达到可降解去除的目的。这样看来,腐蚀并不总是一副邪恶的面孔!
5. 小结
支架是多种心脏病的有效治疗手段,通过微创伤介入治疗,带给了无数家庭“心”的希望。在每一枚承载希望的支架中,腐蚀仍然是需要长期关注的问题,它时而邪恶万分,时而温暖无限,有效利用其规律,分而治之很关键。
虽然支架可救命,但是保养身体、延缓老化更重要。“法于阴阳,和于术数,食饮有节,起居有常,不妄作劳”是《皇帝内经》记载的养生智慧,让我们一起行动起来吧!
参考文献
[1] https://citoday.com/images/articles/2017-04/0417_aortic_fig4.png
[2]王光辉。 异种金属焊接接头的应力腐蚀开裂和寿命评估[J]全面腐蚀控制。 2017 , 31 (5) :24-31.
[3] Dieter Stoeckel, Alan Pelton, Tom Duerig. Self-expanding nitinol stents: material and design considerations[J]European Radiology, 2004, 14 (2): pp 292–301.
[4] AL Mckelvey, RO Ritchie. Fatigue-crack propagation in Nitinol, a shape-memory and superelastic endovascular stent material[J]Journal of Biomedical Materials Research, 2015 , 47 (3) :301-308.
作者简介:王光辉,男,1987年生,硕士,陕西西安人,致力于介入医疗器械、核电主设备用金属材料的优化与老化机理研究、失效分析和寿命评估,上海市腐蚀科学技术学会会员。
E-mail:wanggh2010sh@163.com
更多关于材料方面、材料腐蚀控制、材料科普等方面的国内外最新动态,我们网站会不断更新。希望大家一直关注中国腐蚀与防护网http://www.ecorr.org
责任编辑:王元
《中国腐蚀与防护网电子期刊》征订启事
投稿联系:编辑部
电话:010-62313558-806
邮箱:fsfhzy666@163.com
中国腐蚀与防护网官方 QQ群:140808414
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62313558-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414





