孙海静,刘莉,李瑛*,王福会
中国科学院金属研究所金属腐蚀与防护国家重点实验室,沈阳,中国,110016,
liying@imr.ac.cn,辽宁省沈阳市沈河区文萃路62号
作者简介
孙海静,女,博士研究生,汉族,1985年7月出生,山东省潍坊市人。
2007年7月毕业于湖南大学化学化工学院应用化学系,同年9月考入中国科学院金属研究所攻读硕士学位,并于2010年3月转博。师从于腐蚀与防护国家重点实验室的李瑛研究员和刘莉副研究员,主要从事“深海环境下低合金钢的腐蚀行为及其相关防护措施”的研究工作。

孙海静
摘 要:本文采用静态挂片失重、电容-电位曲线和电化学阻抗谱(EIS)等方法研究了一种低合金高强度钢(HSLA钢)在深海静水压环境下的腐蚀行为。结果表明,在不同的浸泡阶段静水压力对该材料腐蚀行为的影响分别为:浸泡1-5天时,静水压力通过增加Cl-在材料表面的吸附量加速其腐蚀;浸泡5-10天时,由于高静水压下完整覆盖的产物膜表现出更好的阻挡作用,导致其腐蚀速度反而略低于常压;浸泡10天之后,高压和常压下材料表面均被产物膜完全覆盖,静水压力则通过加速侵蚀性粒子的传输,再次加速材料的腐蚀。
关键词:深海;静水压力;低合金高强度钢;电化学阻抗谱
1 引言
随着海洋资源的开发和利用,海水中金属的腐蚀问题得到了人们的广泛关注。然而目前的研究工作大多集中在海洋大气和浅海环境,深海环境中金属的腐蚀行为缺乏系统研究,成为亟待深入探讨的课题。深海是指200米以下的海洋环境。深海环境对材料的可靠性要求远远高于陆地和浅海,任何可能的腐蚀破坏现象在深海环境中都可能导致严重的工程事故,其损失远远超过腐蚀研究的投资。
从20世纪60年代起,一些发达国家就开展了材料的深海环境腐蚀试验[1-5],结果表明:随着水深的增加,材料的腐蚀类型和腐蚀速度均发生了较大的变化。但深海是一个复杂的腐蚀环境,随着海水深度的增加,静水压力、溶解氧、温度和流速等一系列因素都会发生较大程度的改变,而这些因素对材料腐蚀的影响很难区分[1,5]。Beccaria等[6-9]研究了静水压力对纯铝和纯镍在NaCl溶液中腐蚀行为的影响,发现随着静水压力的增大,纯铝和纯镍的腐蚀速率增加,同时静水压力使材料的点蚀敏感性上升。近来,张涛等人[10]研究了Ni-Cr-Mo-V钢的腐蚀行为,发现在高静水压下该钢的耐蚀性降低,且腐蚀形态更加均匀。总之,静水压力是深海环境中最重要的特征因素之一,它显着地影响了材料的腐蚀。
HSLA钢在深海工程中有着广泛的应用,是制造结构件的主要金属材料[1,11],然而静水压力对其腐蚀行为的影响尚不明确。本文在实验室中通过自行设计的深海环境模拟装置模拟了水下350米(相当于35 atm的静水压力)处的海洋环境,采用静态挂片失重、电容-电位曲线及电化学阻抗谱等方法系统研究了上述静水压下一种HSLA钢在3.5% NaCl溶液中的腐蚀行为。
2 实验材料及方法
2.1 样品准备
所用HSLA钢的主要成分为C 0.076,Si 0.29,Mn 0.54,Cr 0.6,Ni 4.67,Mo 0.46,V 0.065,Fe余量。静态挂片样品的尺寸为35 × 15 × 3 mm3,用水磨砂纸磨至1000#,经蒸馏水清洗、酒精除油、吹干后放入干燥器中待用。电化学样品的尺寸为10 × 10 × 10 mm3,试样背面点焊引出铜导线,再用环氧树脂将试样包封在聚四氟乙烯管中,露出试样表面积为1 cm2,用水磨砂纸打磨至2000#,2.5号抛光膏抛光,经蒸馏水清洗、酒精除油、吹干后放入干燥器中待用。
2.2 失重实验
静态挂片平行试样的数量为三个。实验结束后,按照GB/T16545-1996《金属和合金的腐蚀 腐蚀试样上腐蚀产物的清除》去除腐蚀产物,经蒸馏水清洗、酒精除油、吹干并冷却后,用电子天平(Sartorius公司,精度为0.0001 g)称重以计算其腐蚀速度。
2.3 产物膜成分形貌分析
采用金相显微镜、XL30FEG 型扫描电子显微镜(SEM/EDAX)对材料的微观形貌进行观察,而腐蚀产物的成分则通过X-ray衍射仪(XRD)和红外吸收光谱仪(IR)获得。#p#分页标题#e#
2.4 电化学测试
所有电化学测量均采用EG&G公司的PAR2273恒电位仪测试系统。用传统三电极体系,其中辅助电极为铂电极,参比电极为高压专用的固态Ag/AgCl参比电极(ESCE=-0.056 V),不同静水压下该参比电极的电位变化在±5 mV以内。电容-电位测量选用的固定频率为18 Hz,正弦波信号的振幅为10 mV,电位步长为5 mV。电化学阻抗谱的测量频率范围为100 kHz ~ 10 mHz,激励信号为5 mV.采用ZsimpWin软件对所测得的EIS数据进行处理,运用非线性最小二乘法进行拟合。上述所有测试均在室温下进行。
2.5 实验装置
实验所用的深海环境模拟装置结构如图1所示,该装置通过氮气加压提供所需的静水压力。由于通入氮气后装置内的氧气分压没有改变,由亨利定律可知,氮气的加入仅仅改变了总压力,对溶液中的氧含量没有影响。
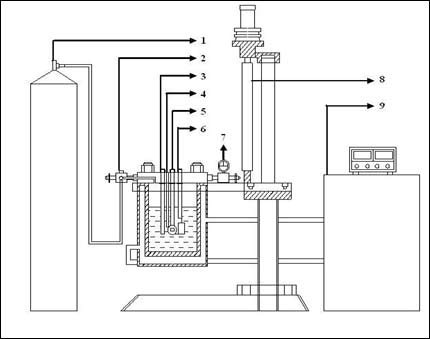
Figure 1. Schematic diagram of deep ocean simulation device: (1-nitrogen, 2-valve, 3-solid reference electrode, 4-thermocouple, 5-working electrode, 6-counter electrode, 7-pressure meter, 8-automatic elevator, 9-temperature controller)
3 实验结果与讨论
3.1 显微结构
实验所用HSLA钢的金相组织如图2所示,为板条状马氏体,其间散布着一些夹杂物,EDAX分析表明夹杂物可能由MnS和Al2O3构成。

Figure 2. The metallographic structure of the specimen
3.2 腐蚀动力学结果
该钢在1 atm和35 atm下腐蚀速度随时间的变化曲线如图3所示。结果表明,两种环境下它的腐蚀速度都随浸泡时间的延长降低而后趋于稳定;在不同的浸泡阶段静水压力对其腐蚀行为产生了不同的影响:浸泡1-5天时,高静水压下材料的腐蚀速度大于常压;浸泡5-10天时,高静水压下腐蚀速度反而略低于常压;10天之后,高静水压下腐蚀速度再次高于常压。为进一步阐明静水压力的作用机制,分别对材料在上述三个阶段的腐蚀行为进行了更为细致的观察分析。
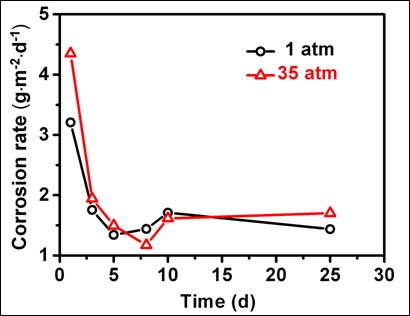
Figure 3. The corrosion rate of the steel as a function of immersion time at different pressures
3.3 浸泡1-5天的腐蚀行为特征
图4为1 atm和35 atm下该钢在3.5% NaCl溶液中浸泡30min后的腐蚀形貌。可见,表面均出现了活性金属的点蚀,比较腐蚀点的覆盖面积发现高静水压下腐蚀更加严重。对初始萌生点进行微观形貌观察如图5所示,发现两种环境下腐蚀均从一点萌生,向周围扩展。EDAX分析证明萌生点都发生在可能由MnS和Al2O3组成的夹杂物处。
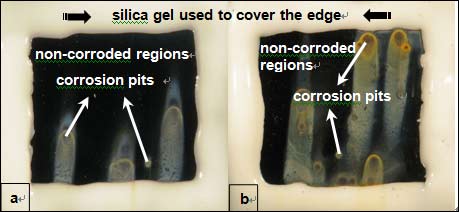
Figure 4. Macroscopic corrosion morphology of the steel after immersion for 30 min in 3.5% NaCl at (a) 1 atm and (b) 35 atm
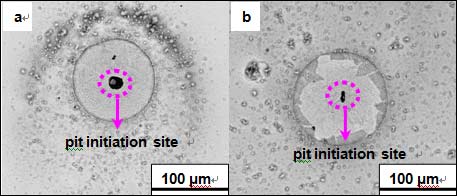
Figure 5. The morphology of the initial pits of the steel after immersion for 30 min in 3.5% NaCl at (a) 1 atm and (b) 35 atm

Figure 6. Macroscopic surface appearances of the steel after immersion in 3.5% NaCl: for 5 d (a) 1 atm and (b) 35 atm; for 10 d (c) 1 atm and (d) 35 atm; for 25 d (e) 1 atm and (f) 35 atm
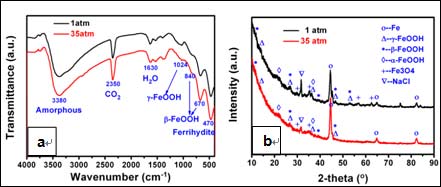
Figure 7. IR (a) and XRD (b) spectra of corrosion products after immersion for 1 d in 3.5% NaCl at different pressures
1 atm和35 atm下浸泡5天的腐蚀形貌见图6 (a和b)。可见,两种环境下材料发生的都是不均匀的全面腐蚀,表面均未被产物膜完全覆盖,但是高静水压下产物膜的生长速度比常压下快,覆盖面积大。
对腐蚀产物进行肉眼观察发现,两种环境下样品表面的腐蚀产物均由外部疏松的沉积黄锈和内部的黑褐色锈构成。上述腐蚀产物的XRD和IR分析结果如图7所示。结果表明,1 atm和35 atm下产物膜成分一致,内部由致密的黑褐色锈Fe3O4和β-FeOOH组成,外部由疏松的黄色锈γ-FeOOH和α-FeOOH构成。这进一步说明静水压力并没有改变材料的腐蚀历程,而是提高了其腐蚀速度。
腐蚀是材料和环境相互作用的结果。两种环境下,材料一致,且阳极均发生活性溶解反应,即Fe=Fe2++2e-;所处环境中的侵蚀性粒子主要有O2和Cl-,其中O2浓度一致,且阴极均发生氧的去极化反应,即O2+2H2O+4e-=4OH-。因此静水压力可能通过影响侵蚀性Cl-的行为来提高材料的腐蚀速度。而Cl-是特性吸附离子,即能与金属形成配位化学键吸附在其表面。我们通过电容-电位曲线的测量得到了金属表面电荷电位。
定义金属表面电荷Ψc为自腐蚀电位Ecorr与零电荷电位Eq=0的相对差值,即Ψc=Ecorr-Eq=0。当Ψc为正值时,金属表面带正电荷,优先吸附阴离子;反之,当Ψc为负值时,金属表面带负电荷,优先吸附阳离子。且︱Ψc︱越大,则离子吸附量也越大[12]。根据电容-电位曲线(图8),将表面电荷测量结果列于表1.结果显示,两种环境下Ψc均为正值,且高静水压下Ψc值大于常压。因此,静水压力更利于Cl-的吸附,从而加速了金属的活性溶解。#p#分页标题#e#
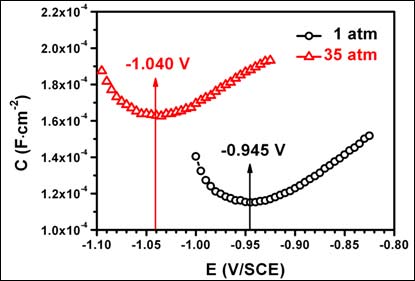
Figure 8. Capacitance vs. potential curves of the steel in 3.5% NaCl at different pressures
Table 1. Values of the surface charge parameters of HSLA steel at different pressures
| HP | Ecorr (mV/SCE) | Eq=0 (mV/SCE) | φc (mV/SCE) |
| 1 atm | -512 | -945 | 433 |
| 35 atm | -534 | -1040 | 506 |
3.4 浸泡5-10天的腐蚀行为特征
由腐蚀动力学结果可知,浸泡5-10天时高静水压下该钢的腐蚀速度反而略低于常压,即此时静水压力的作用出现了所谓的逆转现象。
1 atm和35 atm下浸泡10天的腐蚀形貌观察见图6 (c和d)。此时,常压下材料表面仍未被产物膜完全覆盖,但高静水压下腐蚀产物膜已完全覆盖样品表面。同样的,浸泡于两种环境下10天时材料表面的腐蚀产物均由内外两层组成,且XRD和IR结果表明其成分基本一致,内层由具有阻挡作用的黑褐色锈Fe3O4和 β-FeOOH组成,外部由疏松的黄色锈γ-FeOOH和α-FeOOH组成。
为了进一步阐明静水压力对该材料在这一浸泡阶段腐蚀历程的影响,我们对其电化学阻抗谱进行测试,结果见图9.根据这一阶段腐蚀产物的宏观形貌及电化学阻抗谱图形状选择合适的等效电路如图10所示,得到相应的拟合结果见表2.随着腐蚀的进行,材料表面逐渐形成具有一定保护作用的腐蚀产物膜。从表2结果可见,高静水压下的产物膜电阻Rf要明显大于常压,说明此时高静水压下材料表面形成的产物膜具有更高的阻挡和保护作用,从而降低了材料的腐蚀速度,这一结果与该阶段的形貌观察相吻合。
浸泡第二阶段,虽然高压和常压下形成的产物膜成分一致,但高静水压下产物膜完全覆盖样品表面,而常压下只有部分覆盖,高静水压下完整覆盖的产物膜具有更好的阻挡作用,所以最终导致高静水压下材料的腐蚀速度略低于常压。
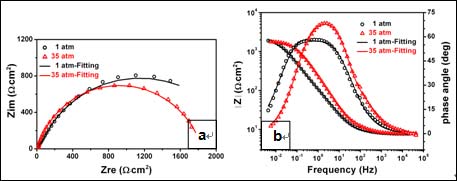
Figure 9. Impedances diagrams of the steel after immersion in 3.5% NaCl for 10 d at different pressures: (a) the Nyquist and (b) Bode diagrams
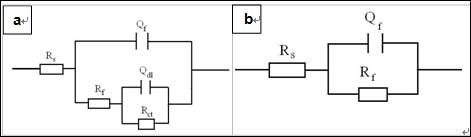
Figure 10. Equivalent circuit for EIS data of the steel in Figure 9 at (a) 1 atm and (b) 35 atm (Rs-the solution resistance, Qdl-the double layer capacitance, Rt-the charge transfer resistance, Qf-the capacitance of the corrosion products and Rf-the resistance of the corrosion products)
Table 2. Parameters extracted from the EIS data of the steel after immersion for 10 d in 3.5% NaCl at different pressures
| hydrostatic pressure | 1 atm | 35 atm |
| Rs (Ω·cm2) | 11.05 | 11.21 |
| Qf (F·cm-2) | 1.68E-3 | 6.84E-4 |
| n1 | 0.7427 | 0.8124 |
| Rf (Ω·cm2) | 1202 | 2592 |
| Qdl (F·cm-2) | 6.97E-4 | - |
| n2 | 1 | - |
| Rct (Ω·cm2) | 1996 | - |
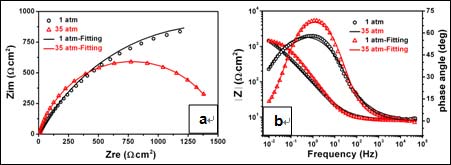
Figure 11. Impedances diagrams of the steel after immersion in 3.5% NaCl for 25 d at different pressures: (a) the Nyquist and (b) Bode diagrams
Table 3. Parameters extracted from the EIS data of the steel after immersion for 25 d in 3.5% NaCl at different pressures
| hydrostatic pressure | 1 atm | 35 atm |
| Rs (Ω·cm2) | 11.35 | 11.34 |
| Qf (F·cm-2) | 2.24E-3 | 1.20E-3 |
| n1 | 0.7002 | 0.8346 |
| Rf (Ω·cm2) | 3704 | 2145 |
3.5 浸泡10天后的腐蚀行为特征
腐蚀动力学结果表明,浸泡10天后高静水压下材料的腐蚀速度再次高于常压。浸泡10天后材料表面形貌如图6 (e和f),此时高压和常压下腐蚀产物膜均已全面覆盖。成分分析结果同样表明两种条件下样品表面腐蚀产物膜成分一致。
这一阶段的EIS结果如图11所示,随着浸泡时间的延长,两种环境下腐蚀产物膜均已完全覆盖样品表面,且阻抗谱都呈现一个容抗弧特征,因此我们用图10 (b)所示的等效电路进行拟合得到相应的参数值见表3.结果显示,高静水压下腐蚀产物的膜电阻远小于常压,说明此时材料在高压下形成的腐蚀产物膜的阻挡作用要明显弱于常压,也就是说在高静水压下溶液本体中侵蚀性粒子如Cl-更容易穿过这层产物膜传输到金属表面,从而起到加速材料腐蚀的作用。综上表明有完整的腐蚀产物膜覆盖后,静水压力则是通过加速侵蚀性粒子的传输,降低产物膜的阻挡作用,从而加速了材料的腐蚀。
4 结论
本文以静水压力作为研究重点,利用深海环境模拟装置对海洋用结构材料HSLA钢在3.5% NaCl溶液中的腐蚀行为进行研究,发现静水压力是影响这种材料在海水中腐蚀行为的重要因素,高静水压下腐蚀历程不变,而速度加快。#p#分页标题#e#
(1)在不同的浸泡阶段静水压力对该钢腐蚀行为的影响分别为:浸泡1-5天时,高静水压下材料的腐蚀速度高于常压;浸泡5-10天时,高静水压下腐蚀速度反而略低于常压;10天之后,高静水压下腐蚀速度再次明显高于长常压。
(2)在整个浸泡阶段,高压和常压下产物膜成分均一致。
(3)静水压力首先通过增加Cl-在钢表面吸附量加速了裸钢的腐蚀;材料表面生成完整产物膜后,静水压力则通过加速侵蚀性粒子的传输,降低产物膜的阻挡作用,再次加速材料的腐蚀。
References(参考文献)
[1]M. Schumacher. Seawater Corrosion Handbook [M]. Noyes Data, New Jersey, 1979.
[2]I. Ulanovskii, V. Egorova. Metal corrosion at different depths in the sea [J]. Protection of Metals, 1978, 14: 137-139.
[3]J. Heiser, P. Soo. Corrosion of barrier materials in the seawater environments [J]. Technology report, 1995, 2(4): 171-194.
[4]S. Sawant, A. Wagh. Corrosion behaviour of metals and alloys the waters of the Arabian Sea [J]. Corrosion Prevent Control, 1990, 37: 154-157.
[5]R.Venkatesan, M.Venkatasamy, T. Bhaskaran, E. Dwarakadasa. Corrosion of ferrous alloys in deep sea environments [J]. British Corrosion Journal, 2002, 37: 257-266.
[6]A.M. Beccaria, P. Fiordiponti, D. Mattongno. The effect of hydrostatic pressure on the corrosion of nickel in slightly alkaline solutions containing Cl- ions [J]. Corrosion Science, 1989, 29: 403-413.
[7]A.M. Beccaria, G. Poggi, D. Gingaud, P. Castello. In?uence of hydrostatic pressure on passivating power of corrosion layers formed on 6061 T6 aluminum alloy in sea water [J]. British Corrosion Journal, 1994, 29: 65-69.
[8]A.M. Beccaria, G. Poggi, M. Arfelli, D. Mattongno. The effect of salt concentration on nickel corrosion behavior in slightly alkaline solutions at different hydrostatic pressures [J]. Corrosion Science, 1993, 34: 989-1005.
[9]A.M. Beccaria, G. Poggi. In?uence of hydrostatic pressure on pitting of aluminum in sea water [J]. British Corrosion Journal, 1985, 20: 183-186.
[10]Yange Yang, Tao Zhang, Yawei Shao, Guozhe Meng, Fuihui Wang. Effect of hydrostatic pressure on the corrosion behaviour of Ni-Cr-Mo-V high strength steel [J]. Corrosion Science, 2010, 52: 2697-2706.
[11]Lathe G, Rajeswari S. Suitability of High Ni-Cr-Mo Alloys as Construction Materials in Seawater [J]. Corrosion Science, 1997, 44(1): 22-28.
[12]A. Popova, E. Sokolova, S. Raicheva, M. Christov. AC and DC study of the temperature effect on mild steel corrosion in acid media in the presence of benzimidazole derivatives [J]. Corrosion Science, 2003, 45: 33-58.

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62313558-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414




