张俊喜1,蒋俊1 ,原徐杰1,鲁进亮1,钱胜杰1 ,王昆2 ,屈文俊2
1上海电力学院,上海,中国,200090
2同济大学土木工程学院,上海,中国,200090
Email: zhangjunxi@shiep.edu.cn
个人简介
张俊喜,博士,教授,现为中国腐蚀与防护学会腐蚀电化学及测试方法专业委员会委员、水环境专业委员会委员和青年工作委员会委员,中国仪表功能材料学会理事,上海市新材料协会理事,国家科技进步奖评审专家,上海市科委高级专家库专家。1994年-2000年于浙江大学化学系研究生学习,师从曹楚南院士。2000年毕业后在上海电力学院从事教学、科研工作。主要从事金属腐蚀与防护、化学电源、新型材料制备、表面改性处理等领域的研究工作。作为负责人正在承担和完成了国家自然科学基金项目、教育部科技重点项目、国家航天基金项目、上海市基础重点项目、上海市教委科技重点项目等项目。在国内外发表研究论文六十余篇,被SCI、EI收录四十余篇。申请专利11项。承担了材料化学专业的《材料化学与物理》、《材料制备与加工》以及《科学研究训练》等课程的教学。

张俊喜
摘要:本文采用电化学测试方法研究了两种醇胺类缓蚀剂在模拟混凝土孔隙液中加入2000ppmNaCl的溶液中对钢筋的缓释效果。结果表明:在模拟溶液中,缓蚀剂能有效抑制钢筋的腐蚀,随着缓蚀剂浓度的增加,缓释效果逐步增大。所选用的两种醇胺类缓蚀剂均具有很好的缓释效果,当缓蚀剂浓度为0.08mol/L时,正丙醇胺的缓释效率为93.01%,二乙醇胺的缓释效率为93.24%通过自行设计的装置研究了缓蚀剂在混凝土中的迁移行为,结果表明:在2A/m2恒电流密度形成的电场作用下,醇胺缓蚀剂通过35mm厚的混凝土速率明显高于未通电的情况,说明电场作用对醇胺缓蚀剂的迁移扩散过程起到了促进作用。通过缓蚀剂辅助再碱化模拟实验发现,用1mol/L正丙醇胺溶液做电解质溶液,再碱化结束后在相同的弛豫时间内相对于碳酸钠溶液,其腐蚀电位正移,腐蚀电流密度更小,这表明缓蚀剂辅助再碱化技术可以提高再碱化的修复效果,能有效抑制钢筋混凝土中钢筋的腐蚀。
资助信息:国家自然科学基金(No. 50771602,50678127)资助项目
关键字:钢筋混凝土;电化学再碱化;缓蚀剂;物料传递
1. 前言
长期服役的钢筋混凝土发生碳化后,钢筋周围的pH下降,钢筋钝化膜稳定存在的条件被破坏,钝化膜溶解钢筋发生腐蚀。针对这种情况,目前电化学再碱化技术成为钢筋混凝土修复技术的研究热门之一。电化学再碱化方法可以使已碳化的混凝土pH值恢复,从而减缓钢筋的继续锈蚀[1-8]]。与其它常用的钢筋混凝土修补方法相比,电化学再碱化技术具有环境友好、方便、不破坏混凝土原有外貌等优点。然而电化学再碱化修复过程的研究也发现了较多问题,初步研究表明[9,10],尽管钢筋周围的混凝土在再碱化后碱性得以提高,但再碱化过程使得钢筋表面处于高度活性状态,钢筋很难进入再钝化状态,难以降低钢筋的腐蚀速度。因此,仅仅恢复钢筋混凝土的碱性环境是不足的,还需使钢筋进入被保护状态,降低钢筋的腐蚀速度。缓蚀剂应用于钢筋混凝土的保护已有大量的研究[11-15],早期研究主要是在混凝土浇筑过程中加入缓蚀剂,通过溶解在钢筋表面孔隙液中的缓蚀剂提高钢筋的耐蚀性能,起到保护作用[16,17],但是该方法主要针对新建设的混凝土结构,对已建成混凝土结构则无能为力。在对钢筋混凝土构筑物进行修复时,如何使缓蚀剂通过保护层到达钢筋表面是一个关键的问题。近年来,有关于应用外加电场使阳离子型缓蚀剂进入混凝土实现钢筋防腐蚀的研究[18,19],受到了本领域研究者的关注。在此基础上,可以设想在对碳化混凝土再碱化修复的同时,引入阳离子型缓蚀剂,使之在再碱化修复的同时,通过电渗和电迁移引入到钢筋表面,则可以在实现再碱化的同时起到保护钢筋的双重效果。
本文就是在这样的设想下开展研究,主要研究了缓蚀剂在浓度梯度以及外加电场的作用下通过混凝土保护层的传质行为,实验研究了在模拟碱性体系中缓蚀剂对钢筋的缓蚀行为,最后通过模拟实验研究了缓蚀剂对人工碳化的钢筋混凝土的缓蚀效果。
2 实验方法
2.1 试剂与仪器
正丙醇胺(分析纯,上海凌峰化学试剂有限公司产品),二乙醇胺(分析纯,上海凌峰化学试剂有限公司产品),氢氧化钠(分析纯,国药集团化学试剂有限公司),氧化钙(分析纯,国药集团化学试剂有限公司),氯化钠(分析纯,浙江三鹰化学试剂有限公司产品)。
采用1020A型TOC分析仪测定清水端有机碳浓度以及分析缓蚀剂浓度,采用PAR2273电化学工作站进行电化学测试。所采用的参比电极、辅助电极分别为饱和甘汞电极、铂电极。电化学交流阻抗谱(EIS)测量采用的激励信号为正弦波,振幅为10mV,扫描频率范围为100 kHz~10 mHz,用ZSimpWin软件拟合测试数据。动电位极化曲线测试的扫描速率为1mV/s,扫描范围为-150 mV~+ 150 mV( 相对于开路电位),实验数据由Powersuite软件采集和分析。
2.2 醇胺类缓蚀剂在混凝土中的迁移
采用425级普通硅酸盐水泥,混凝土浇注成Φ60mm*35mm的模型,其配合比为水泥:水:砂:石= 1:0.65:2.25:3.68。经标准养护,人工碳化后按照图1进行组装。
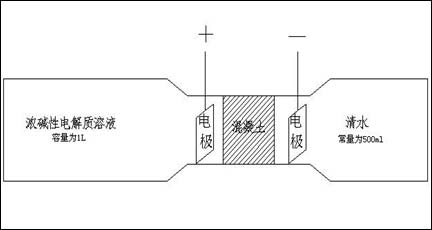
图1 物料传递装置模拟图
碱性电解质溶液端浓度为1mol/L 的正丙醇胺溶液及1mol/L 的二乙醇胺溶液各两组,清水端为0.5mol/L的硫酸铵溶液,硫酸铵作为支持电解质。其中每组包含通电与不通电两个装置,通电装置在2A/m2的固定电流密度下分别每隔3天对装置清水端取样10mL分析有机碳浓度,直至300天实验结束。
2.3 缓蚀性能评价
参照ASTM G31-72《Standard Practice for Laboratory Immersion Corrosion Testing of Metals》进行实验。实验温度为室温(25℃),实验材料为建筑用的公称直径为d=10mm的Q235螺纹钢筋,试验前将钢筋加工成Φl0mm×10mm 的圆柱形试样,在背面焊接导线,并用环氧树脂将焊点及非工作面包封,露出工作面积为0.785cm2。研究用溶液为含2000ppmNaCl+0.01M NaOH的饱和氢氧化钙溶液。将处理好的钢筋电极放入含有不同醇胺缓蚀剂浓度的溶液中,浸泡24h后,进行电化学测试,计算各自的缓蚀率及腐蚀电流。
2.4 模拟体系缓蚀效果的研究
将已完全碳化的钢筋混凝土试件置于有机电解液中,以碳化混凝土样品中钢筋作为阴极连接直流电源负极,在混凝土外以不锈钢网作为阳极与直流电源正极连接。试验时,调整直流电源电压,控制电流密度为2A/m2。电流密度指单位钢筋表面积上的电流值大小。
本研究中参比电极均相对于饱和甘汞电极(SCE)。
3 结果与讨论
3.1缓蚀剂在碳化混凝土中的传质行为
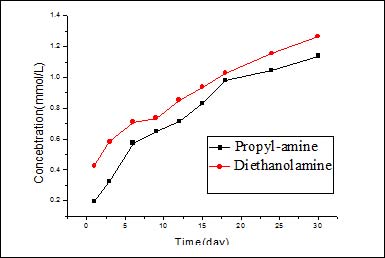
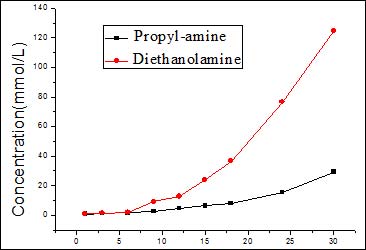
图2 不通电(上)与通电(下)情况下清液端正丙醇胺与二乙醇胺浓度随时间变化情况#p#副标题#e#
图2是在通电与未通电情况下清液端正丙醇胺和二乙醇胺浓度随时间的变化情况。从图中可以看出,随着时间的变化,清液端正丙醇胺和二乙醇胺浓度逐步增加,而且通电清液端浓度明显高于未通电清液端,这表明缓蚀剂能在浓度梯度和外加电场的作用下通过混凝土的保护层到达钢筋表面,外加电场对阳离子型缓蚀剂的迁移有明显的加速作用。无论是通电还是未通电,二乙醇胺通过混凝土块的速率均大于正丙醇胺。在未通电的情况下,缓蚀剂在混凝土中的传质主要是通过物质的扩散过程完成[20]。而扩散过程的驱动力为浓度梯度,实验中这两种缓蚀剂的浓液端初始浓度均为1mol/L,清夜端的浓度均为0mol/L,故它们的驱动力大小一致。但是在混凝土中,缓蚀剂在传质过程中还会与混凝土中一些颗粒发生作用,被混凝土中颗粒物吸附在孔隙中,缓蚀剂滞留在混凝土内影响了缓蚀剂的传质过程。二乙醇胺分子结构中的双羟基使得二乙醇胺相对于正丙醇胺更能溶于水中,即相对于正丙醇胺二乙醇胺受混凝土颗粒的作用更小,故未通电时二乙醇胺的传质速率大于正丙醇胺。在通电的情况下,缓蚀剂的迁移除了在浓度梯度作用下的扩散外,还有在电场作用下离子的电迁移以及电渗析[21]。故在电场作用下,缓蚀剂的迁移受到浓度梯度以及电场梯度的共同作用。在常温下,通过实验测得的1mol/L二乙醇胺和1mol/L正丙醇胺的电导率分别为0.387*103μS/cm、1.687*103μS/cm,二乙醇胺的电导率大大低于正丙醇胺的电导率,即二乙醇胺溶液的电阻大于正丙醇胺溶液。则在相同的电流大小,相同的混凝土厚度,二乙醇胺的电场梯度大于正丙醇胺,故二乙醇胺所受到的电场作用更大,这就是为什么在电场作用下二乙醇胺的迁移速率明显大于正丙醇胺。
3.2 缓蚀效果分析
已有的研究表明[22-24],在碱性环境下醇胺类物质对钢筋腐蚀有较好的缓释作用。图3a、3b是钢筋在模拟混凝土孔隙液中不同缓蚀剂浓度下的极化曲线。从图中可以看出,随着缓蚀剂浓度的增加,钢筋的腐蚀电位逐渐正移,腐蚀电流密度减小,这表明缓蚀剂的加入抑制了钢筋的阳极溶解过程。
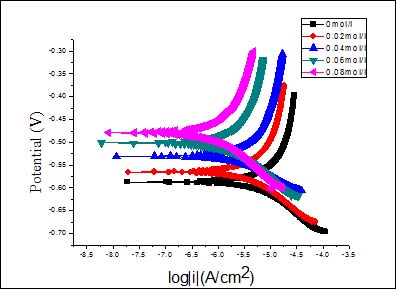
图3a 不同正丙醇胺浓度下钢筋的极化曲线
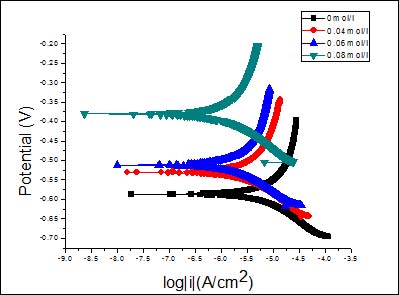
图3b 不同二乙醇胺浓度下钢筋的极化曲线
表1 钢筋在不同正丙醇胺浓度下的腐蚀电位以及腐蚀电流密度
| 正丙醇胺(mol/L) | 0 | 0.02 | 0.04 | 0.06 | 0.08 |
| Ecorr(mV) | -613.048 | -574.556 | -542.915 | -510.114 | -484.626 |
| Icorr(μA) | 14.80 | 5.243 | 3.780 | 2.194 | 1.046 |
| IE% | 64.57% | 74.46% | 85.18% | 92.93% |
表2 钢筋在不同二乙醇胺浓度下的腐蚀电位以及腐蚀电流密度
| 二乙醇胺(mol/L) | 0 | 0.04 | 0.06 | 0.08 |
| Ecorr(mV) | -613.048 | -536.997 | -463.598 | -380.993 |
| Icorr(μA) | 14.80 | 3.113 | 1.934 | 1.169 |
| IE% | 78.97% | 86.93% | 92.10% |
表1、表2是通过Powersuite测试软件对极化曲线拟合所得出的钢筋在不同缓蚀剂浓度下腐蚀电位、腐蚀电流密度。以及通过式⑴所求得的缓释效率。
 (1)
(1)
I’corr:不同缓蚀剂浓度下钢筋的腐蚀电流密度;Icorr:空白溶液中钢筋的腐蚀电流密度
从表中可以看出,在碱性环境下正丙醇胺和二乙醇胺对钢筋都有很好的缓释效果,当缓蚀剂浓度为0.08mol/l时,缓蚀剂对钢筋的缓释效率都达到了90%以上。
图4a、4b为钢筋在不同浓度正丙醇胺和二乙醇胺下浸泡24h的Nyquist图。从图4a、4b中可以看出,随着缓蚀剂浓度的增加,容抗弧逐渐增大。这表明随着缓蚀剂浓度的增加,缓释效果越来越好。

图4a 不同正丙醇胺浓度下钢筋的阻抗谱图
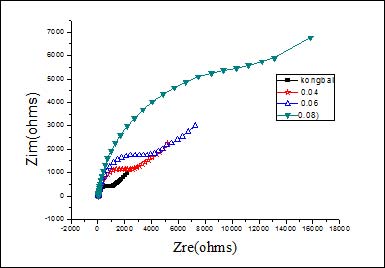
图4b 不同二乙醇胺浓度下钢筋的阻抗谱图
图4a、4b显示阻抗谱中呈现双容抗弧,故阻抗采用R(Q(R(QR)))等效电路拟合。
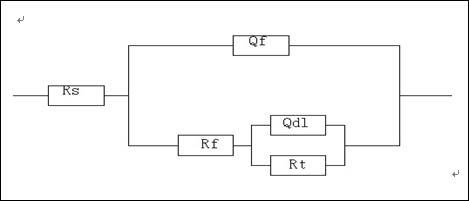
图5 等效电路图#p#副标题#e#
表3、4为不同浓度正丙醇胺和二乙醇胺含2000ppmNaCl的饱和氢氧化钙溶液中Q235电极的阻抗拟合参数。其中,Rs表示溶液电阻,Qf表示表面层电容,Rf表示表面层电阻,Qdl表示界面双电层电容,Rct表示电荷传递电阻。随着缓蚀剂浓度的增加,电荷转移电阻(Rct)变大,双电层电容(Cdl)降低,这表明随着缓蚀剂浓度的增加,双电层电容较大的水分子被正丙醇胺或二乙醇胺取代,正丙醇胺分子或二乙醇胺在钢筋表面形成保护膜,抑制了其腐蚀[25]。对电路拟合后计算其缓蚀效率,其计算公式如下:
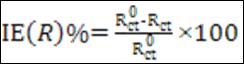 (2)
(2)
式中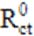 、Rct分别为加与不加缓蚀剂时的电荷转移电阻。从表中可以看出,随着浓度的增加,缓蚀效率逐渐增加。当缓蚀剂浓度为0.08mol/l时,正丙醇胺缓蚀剂的缓释效果为93.01%,二乙醇胺的缓释效果为93.24%,这与极化曲线获得的结果一致。
、Rct分别为加与不加缓蚀剂时的电荷转移电阻。从表中可以看出,随着浓度的增加,缓蚀效率逐渐增加。当缓蚀剂浓度为0.08mol/l时,正丙醇胺缓蚀剂的缓释效果为93.01%,二乙醇胺的缓释效果为93.24%,这与极化曲线获得的结果一致。
表3 钢筋在不同正丙醇胺浓度下的等效电路拟合参数
| C(mol/L) | 0 | 0.02 | 0.04 | 0.06 | 0.08 |
| Rs(Ω•cm2) | 26.76 | 25.98 | 42.33 | 41.5 | 38.18 |
| Qcp(F •cm2) | 0.000103 | 9.213E-5 | 9.76E-5 | 0.0001061 | 9.369E-5 |
| n1 | 0.8915 | 0.8 | 0.8827 | 0.8811 | 0.8382 |
| Rcp(Ω•cm2) | 605.7 | 1542 | 1924 | 2729 | 8647 |
| Qdl(F •cm2) | 0.002124 | 0.001872 | 0.001064 | 0.0005752 | 0.0005392 |
| n2 | 0.4243 | 0.4347 | 0.479 | 0.6083 | 0.8 |
| Rct(Ω•cm2) | 8774 | 2.567E4 | 4.521E4 | 1.177E5 | 1.255E5 |
| IE% | 0 | 65.82% | 80.59% | 92.55% | 93.01% |
| C(mol/L) | 0 | 0.04 | 0.06 | 0.08 |
| Rs(Ω•cm2) | 26.76 | 30.34 | 29.9 | 28.77 |
| Qcp(F •cm2) | 0.000103 | 8.449E-5 | 0.0001065 | 0.0001111 |
| n1 | 0.8915 | 0.8796 | 0.8 | 0.8 |
| Rcp(Ω•cm2) | 605.7 | 1953 | 2513 | 6763 |
| Qdl(F •cm2) | 0.002124 | 0.001223 | 0.0008273 | 0.0005079 |
| n2 | 0.4243 | 0.5709 | 0.8 | 0.8 |
| Rct(Ω•cm2) | 8774 | 7.572E4 | 1.256E5 | 1.297E5 |
| IE% | 0 | 88.41 | 93.01 | 93.24 |
3.3 吸附行为研究
有机缓释剂分子在金属表面的覆盖度(θ)可以通过缓蚀剂的缓释效率来表示[25]即:
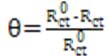 (3)
(3)
表5给出了钢筋电极在模拟溶液中,不同缓蚀剂浓度下的覆盖度。将θ带入等温吸附方程拟合,结果表明,实验所获得的结果符合Langmuir等温吸附方程。
根据Langmuir等温吸附方程有:
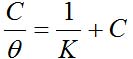 (4)
(4)
其中,C为缓蚀剂浓度,K为Langmuir吸附平衡常数。将Cθ-1-C作图(图6),从图中可以看出,Cθ-1-C呈较好的线性关系,正丙醇胺和二乙醇胺的线性相关系数R分别为:0.99462,0.99835,其斜率分别为:0.910,1.014。这说明正丙醇胺,二乙醇胺分子在钢筋表面的吸附符合Langmuir等温吸附模型,每个分子大约占据1.0个吸附点,是单分子吸附。通过拟合曲线所获得的截距而计算得到的Langmuir吸附平衡常数K分别为:83.333和232.558L/mol。
K与吸附吉布斯自由能ΔG0的关系式为:
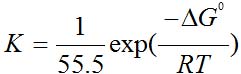 (5)
(5)
其中,55.5为溶剂水的浓度(mol/L),R为摩尔气体常数,T为热力学温度(K),计算ΔG0分别为:-20.920kJ/mol,-23.464kJ/mol,ΔG0<0说明缓蚀剂在钢筋表面的吸附过程是一种自发行为。通常情况下,当ΔG0在-20kJ/mol左右时,表示带电荷的缓蚀剂分子和带电荷的金属之间的静电作用,为物理吸附,因此正丙醇胺和二乙醇胺在钢筋表面的吸附为物理吸附。
3.4 模拟再碱化的效果分析
表5 在不同浓度缓蚀剂的模拟孔隙液中钢筋表面缓蚀剂覆盖度
| 浓度(mol/L) | 0.02 | 0.04 | 0.06 | 0.08 |
| 正丙醇胺(θ) | 0.6582 | 0.8059 | 0.9255 | 0.9301 |
| 二乙醇胺(θ) | 0.8841 | 0.9301 | 0.9324 |
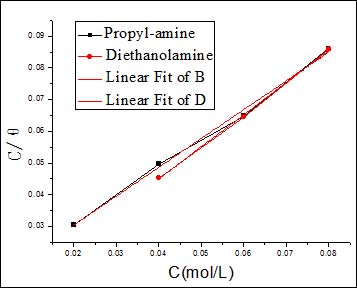
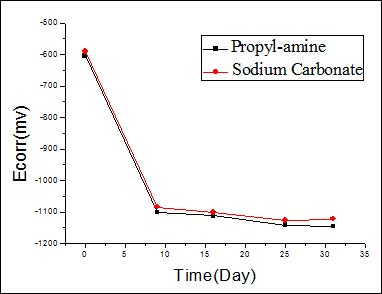
图7a 再碱化过程中钢筋的Ecorr随时间的变化趋势
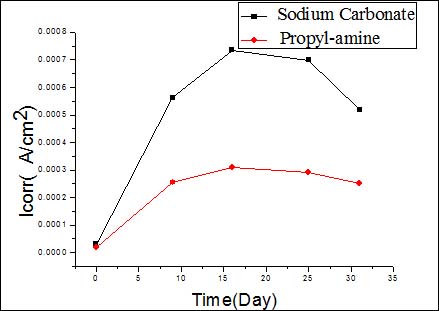
图7b 再碱化过程中Icorr随时间的变化趋势#p#副标题#e#
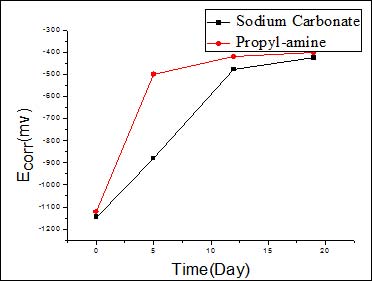
图8a弛豫过程中Ecorr随时间的变化趋势
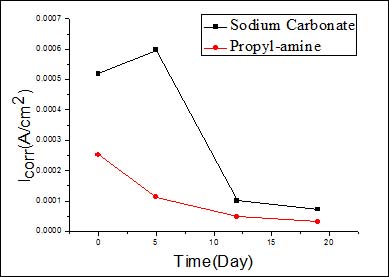
图8b弛豫过程中Icorr随时间的变化趋势
从图7a,7b中可以看出在再碱化过程中,腐蚀电位变得更负,接近析氢电位,而腐蚀电流也增加,但有缓蚀剂存在时,样品的腐蚀电流增加幅度远小于仅在碳酸钠电解质中的腐蚀电流。从图8a,8b中可以看出,随着弛豫时间的延长,腐蚀电位正移,腐蚀电流减小,但有缓蚀剂存在情况下,钢筋在弛豫过程中腐蚀电位正移幅度更大,腐蚀电流小于无缓蚀剂的情况。以上分析表明,短期内缓蚀剂的加入确实起到缓蚀作用,对改善钢筋状态起到有益的作用。
4. 结论
⑴ 在通电与未通电的情况下,缓蚀剂均能通过3.5cm厚的混凝土块到达清液端,在外加电场的作用下缓蚀剂的迁移速率明显大于未加电场,外加电场对缓蚀剂的迁移有明显的促进作用;
⑵ 在碱性环境下,正丙醇胺与二乙醇胺对钢筋均有很好的缓释效果,当缓蚀剂浓度为0.08mol/l时,正丙醇胺缓蚀剂的缓释效率为93.01%,二乙醇胺的缓释效率为93.24%;
⑶ 在等温等压下,正丙醇胺与二乙醇胺都能自发的吸附在钢筋表面,其ΔG0分别为:-20.920kJ/mol,-23.464kJ/mol,为物理吸附。
⑷ 缓蚀剂的加入确实起到缓蚀作用,对改善钢筋状态起有益的作用。
致 谢
感谢国家自然科学基金(50771602,50678127)对本课题的资助。
References(参考文献)
[1] Anon,Electrochemical realkalisation of reinforced concrete, Quality Concrete,2002,41: 3-4
[2] Mohankumar G, Concrete repair by electrodeposition, Indian Concrete J, 2005,79 (8):57
[3] Yeih,Chang Weichung,Jiang Jhy, A study on the efficiency of electrochemical realkalisation of carbonated concrete,Construction and Building Materials, 2005,19 (7):516-520
[4] M.Castellote, I.Llorente, C.Andrade,Influence of the composition of the binder and the carbonation on the zeta potential values of hardened cementitious materials,Cement and Concrete Research, 2006,36 (10): 1915-1920
[5] J.Mietz, Electrochemical realkalisation for rehabilitation of reinforced concrete structures, Mater Corrosion, 1995,46(9): 527-533
[6] Bewley, Dave,Realkalisation of reinforced concrete structures, Concrete (London), 2005,39(3): 25-29
[7] Penhall Derek. Electrolytic treatment of concrete to restore its corrosion resistance,Civil engineering, 1994,2(11):17-21
[8] J.M.Miranda, J.A.Gonzalez, A.Cobo, E.Otero, Several questions about electrochemical rehabilitation methods for reinforced concrete structures, Corrosion Science, 2006,48(8):2172-2179
[9] J.A.Gonzalez, A.Cobo, M.N.Gonzalez, E.Otero, On the effectiveness of realkalisation as a rehabilitation method for corroded reinforced concrete structures, Mater Corrosion, 2000,51(2): 97-103
[10] Zhang Junxi, Yang Ji, Zhang Lingsong, Xiong Yan, Qu Wunjun, Yan Licheng. Electrode Process of Rebar in Ca(OH) 2 Solution during Realkalization of Carbonated Concrete , Corrosion &Protection, 2008, 29(9): 507-511(Ch)
张俊喜,杨吉,张铃松,熊焱,屈文俊,颜立成,碳化混凝土再碱化过程中钢筋在Ca(OH)2溶液中的电极过程,腐蚀与防护,2008,29(9):507-511
[11] C.K.Nmai, S.A.Farrington, G.Bobroski,Organic-based corrosion inhibiting admixture for reinforced concrete ,Concrete International, American Concrete Institute, 1992,14(4), 45-51
[12] C.K.Nmai, P.D.Krauss,Comparative evaluation of corrosion inhibiting chemical admixtures for reinforced concrete, V.M.Malhotra(Nice, France, ACI International, May,1994) p.245
[13] T.A.Soylev, C.M.Nally, M.G.Richardson, The effect of a new generation surface-applied organic inhibitor on concrete properties,Cement & Concrete Composites,2007(29): 357-364
[14] C.L.Page, V.T. Ngala, M.M. Page, Corrosion inhibitors in concrete repair systems,Magazine of Concrete Research,2000, 52(1): 25-37
[15] L.B.Mechmech, L.Dhouibi, M.B.Ouezdou, E.Triki, F.Zucchi, Investigation of the early effectiveness of an amino-alcohol based corrosion inhibitor using simulated pore solutions and mortar specimens,Cement &Concrete Composites,2008, 30:167-173
[16] C.K.Nmai, S.A.Farrington, G.Bobroski,Organic-based corrosion inhibiting admixture for reinforced concrete ,Concrete International, American Concrete Institute, 1992,14(4): 45-51
[17] C.K.Nmai, P.D.Krauss,Comparative evaluation of corrosion inhibiting chemical admixtures for reinforced concrete, V.M.Malhotra(Nice, France, ACI International, May,1994) p.245
[18] Sawada S, Kubo J, Page C L, Page M M. Electrochemical injection of organic corrosion inhibitors into carbonated cementitious materials: Part 1 Effects on pore solution chemistry , Corrosion Science, 2007(49): 1186-1204
[19] S.Sawada, J.Kubo, C.L.Page, M.M.Page, Electrochemical injection of organic corrosion inhibitors into carbonated cementitious materials: Part 2 Mathematical modeling, Corrosion Science, 2007(49): 1205-1227
[20] Buenfeld, N.R., Glass, G.K., Hassanein, A.M. and Zhang, Jian-Zhong, Chloride Transport in Concrete Subjected to Electric Field, Journal of Materials in Civil Engineering, 1998,10(4):220-
[21] Tongyan Pan, Tuan Anh Nguyen, Xianming Shi. Assessment of Electrical Injection of Corrosion Inhibitor for Corrosion Protection of Reinforced Concrete[J]. Journal of the Transportation Research Board, 2008,2044(6):51-60
[22] C.L.Page, V.T. Ngala, M.M. Page, Corrosion inhibitors in concrete repair systems,Magazine of Concrete Research, 2000,52(1):25-37
[23] L.B.Mechmech, L.Dhouibi, M.B.Ouezdou, E.Triki, F.Zucchi, Investigation of the early effectiveness of an amino-alcohol based corrosion inhibitor using simulated pore solutions and mortar specimens,Cement &Concrete Composites, 2008,30:167-173
[24] S.Sawada, C.L.Page, M.M. Page, Electrochemical injection of organic corrosion inhibitors into concrete, Corrosion Science, 2005(47):2063-2078
[25] Hong H G, Park W A. Study of adsorption kinetics and thermodynanics of ω-mercaptoalkylhydroquinone selfassembled monolayer on a gold electrode[J]. Electrochim. Acta.,2005,51(3):579-587

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62313558-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414




