硫酸盐还原菌诱导的碳钢腐蚀:生物膜中的电化学机制与途径
2026-04-29 15:06:19
作者:腐蚀与防护 来源:腐蚀与防护
分享至:
微生物腐蚀(MIC)是指微生物自身生命活动及其代谢产物直接或间接加速金属材料腐蚀过程的现象。统计数据显示,微生物引发的金属材料腐蚀约占金属总腐蚀的20%。其中,硫酸盐还原菌(SRB)是一类革兰氏阴性菌,可在厌氧条件下以环境中硫酸盐为末端电子受体,将其还原为硫化氢,广泛分布于土壤、海底沉积物、油田、工业设备等高硫酸盐缺氧环境中,被认为是最常见的厌氧微生物腐蚀相关微生物。
关于SRB诱导微生物腐蚀机制的研究表明,其对不同金属的腐蚀行为与机制存在差异。为解释SRB对碳钢的典型腐蚀机制,主要有酸性代谢产物腐蚀理论与经典阴极去极化理论(CDT)。微生物腐蚀与微生物燃料电池(MFC)密切相关。微生物燃料电池中的胞外电子传递(EET)过程,包括希瓦氏菌MR-1的直接电子传递(DET)、硫还原地杆菌的导电菌毛蛋白/纳米线介导的电子传递,以及核黄素、吩嗪介导的间接电子传递(MET),可用于探究SRB引发碳钢腐蚀的过程、EPS中胞外电子传递路径及电化学机制。当前,微生物腐蚀研究多关注腐蚀机制、腐蚀产物特征、影响腐蚀的环境条件及防腐措施。基于微生物燃料电池中的生物阴极,已总结出金属阳极与微生物间胞外电子传递的三类路径与方式。然而,由于对电子从胞外到胞内完整传递过程的关键组分缺乏清晰认知,例如参与长程电子传递的导电菌毛/纳米线主要组分仍存在争议,以及胞外电子到达外膜后如何转运并最终在细胞质中被利用尚不明确;同时,对影响腐蚀过程的EPS复杂环境考虑不足,SRB对碳钢腐蚀的认知仍存在诸多问题。
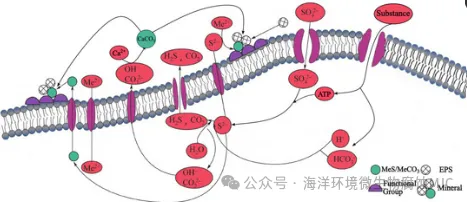
铁金属腐蚀必然伴随铁的阳极溶解。早期研究者推测,在厌氧无微生物环境中,水中的氢会作为电子受体,在金属表面形成“氢膜”,阻碍金属溶解,即“极化”现象。当环境中存在微生物时,阴极去极化理论认为,含氢化酶的SRB吸附于金属表面,利用氢化酶破坏金属表面的“氢膜”,产生电子将SO₄²⁻还原为H₂S并释放能量,以维持SRB生长。金属表面H₂的去除加速了铁的溶解,此过程称为“去极化”,SRB充当去极化剂。Fe²⁺与溶液中的OH⁻、S²⁻结合生成Fe(OH)₂与FeS,FeS在金属表面未被腐蚀层覆盖的裸露区域形成硫化铁(FeSₓ)络合物,构成FeSₓ/Fe电偶腐蚀对,腐蚀产物层的电子富集促进金属腐蚀,并将电子传递给SRB用于硫酸盐还原。H₂S是SRB的代谢产物之一,H₂S微溶于水形成HS⁻,其在水中的溶解比例影响金属腐蚀速率。腐蚀性H₂S会在金属表面造成局部低pH环境,在特定pH条件下,质子还原与铁氧化溶解耦合,加速金属腐蚀过程。徐等于2009年首次提出生物阴极催化还原理论(BCSR),从生物能学角度认为,金属表面附着具有腐蚀能力的生物膜,在生物膜中SRB分泌的多种生物活性酶作用下,阳极金属材料溶解释放的电子穿过细菌细胞壁,被阴极SRB细胞质中发生的硫酸盐还原过程消耗。完整的阴极反应发生在SRB细胞膜上,生物膜直接作为电子受体,“生物阴极”替代了传统“物理阴极”。铁的溶解与硫酸盐还原耦合反应的吉布斯自由能变(ΔG⁰′=-178 kJ/mol),低于标准条件下以乳酸为底物的硫酸盐还原(ΔG⁰′=-164 kJ/mol),热力学上更有利。徐等指出,阴极去极化理论仅适用于含氢化酶的SRB,而体内无氢化酶的SRB仍可腐蚀金属,因此阴极去极化理论仅是生物催化阴极硫酸盐还原理论的特例。生物膜是微生物、代谢产物、腐蚀产物、部分无机矿物与吸附有机物的混合物。其中,微生物代谢产物EPS占生物膜总有机物的50%~90%,被认为是决定生物膜理化与生物学特性的关键组分。EPS通常呈凝胶状三维网状结构,吸湿性强,可溶解于带电生物膜基质中,使微生物群落在界面或基材表面固定、聚集、镶嵌并不可逆吸附。EPS组分包括多糖、蛋白质、脂质、腐殖质、表面活性物质与大量胞外核酸(E-DNA)。不同微生物的EPS组成与比例各异,但均具有组分复杂、功能多样的特点,作为生物膜的重要组分,影响微生物金属腐蚀与胞外电子传递过程。EPS对微生物腐蚀的抑制作用主要体现在四方面:1) EPS引发不同微生物间的竞争,减少微生物附着,降低腐蚀速率;2) EPS在金属表面吸附形成的膜,将金属与腐蚀环境隔离;3) EPS改性金属材料表面性质,抑制细菌黏附;4) 生物矿化。基于生物矿化膜研发新型天然绿色缓蚀剂具有广阔应用前景。生物矿化可分为生物调控矿化与生物诱导矿化两类。生物调控矿化在生物生理活动等直接控制下,在细胞内或细胞表面特定位置合成,不受周围理化环境影响;生物诱导矿化则是生物通过自身生理代谢活动改变周围溶液环境的理化条件,使局部环境达到过饱和状态,诱导细胞外矿物矿化的过程。SRB利用EPS中的有机物诱导周围矿化离子形成固态矿化层,即为典型案例。SRB的EPS组分中存在大量羧基、磷酰基等电负性功能基团,可吸附并静电吸引Ca²⁺、Cd²⁺、Pb²⁺等金属阳离子,提供成核位点与早期生长模块。在异化还原过程中,有机物作为电子供体,SO₄²⁻被还原为H₂S,同时生成CO₃²⁻。当H₂S从液相逸出进入气相时,H₂S生成反应向释放更多气体方向进行,导致游离氢离子浓度降低、胞周微环境pH升高,促进Ca²⁺与CO₃²⁻结合。影响碳酸钙饱和指数的微生物代谢与环境条件称为“碱度”,碱度与EPS为碳酸盐成核提供模板,是微生物席系统中碳酸盐生物矿化的关键组分。当局部区域碳酸钙浓度过饱和(饱和指数SI>1)时,发生CaCO₃沉淀成核。当H₂S不以气体形式释放时,金属离子因EPS静电吸附聚集于细胞表面或细胞内,少量与胞内S²⁻结合生成沉淀后排出,大部分在细胞表面生成沉淀。金属-S²⁻沉淀后,在EPS与细胞表面功能基团作用下结晶成核形成纳米级矿化产物,进而聚集形成大颗粒矿物。但SRB在此过程中具体的调控诱导机制仍需进一步研究。马克斯等分别采用扫描电镜/能谱分析等技术,表征了浸泡在天然海水与灭菌海水中的AA5083铝合金表面改性的化学组成与结构,发现生物矿化过程中形成的含EPS富水合镁外层可提升铝镁合金的耐腐蚀性。单等利用贝莱斯芽孢杆菌诱导碳酸钙矿化,在X65钢表面制备生物矿化膜,其在模拟海上油田采出水中表现出更优的稳定性与耐腐蚀性。
图1 SRB诱导生物矿化过程示意图
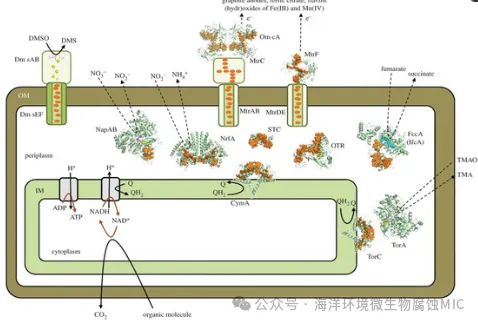
EPS在微生物腐蚀中具有双重作用,其促进作用主要体现在:1) 金属离子与EPS中功能基团反应,破坏金属表面氧化膜,加速腐蚀;2) EPS改变腐蚀产物的化学组成与形貌,即形成不均匀生物膜与氧浓差电池,促进金属腐蚀;3) EPS电化学反应加剧金属腐蚀,包括阳极溶解与阴极还原。金与关指出,EPS结合的Fe³⁺及其在不同生长阶段与EPS的相互作用,可影响阳极或阴极电化学反应。在生物膜形成过程中,EPS与Fe³⁺络合并吸附于铸铁表面,络合态Fe³⁺在生物膜与铸铁界面催化新的氧化还原反应。一方面,Fe³⁺-EPS络合膜改变金属材料表面活性,使金属离子更易从金属表面解离,加速阳极溶解;另一方面,EPS中的Fe³⁺不易扩散至本体溶液,高浓度Fe³⁺充当去极化剂引发阴极去极化,促进金属腐蚀。 胞外电子传递(EET)指微生物细胞外电极与细胞间的电子传递。根据电子传递路径,EET主要分为直接电子传递(DET)与间接电子传递(MET)两类。已鉴定的电子传递介体主要包括内源性吩嗪、核黄素、醌类、细胞色素、溶菌酶、黑色素等。 细胞与胞外固体电极间的电子传递必须穿过EPS层,且大部分EPS组分具有导电或半导电氧化还原特性,因此EPS影响胞外电子传递过程,包括直接电子传递与间接电子传递路径。1) EPS的多糖、蛋白质、DNA组分间存在显著的电学与电化学性质差异,使EPS基质在不同环境中表现出不同的电子传递能力;2) EPS帮助细胞附着于固体电极,缩短微生物与电极间的间隙距离,降低远离电极的生物膜细胞获取电子供体/受体的能量消耗;3) EPS对直接电子传递具有衰减作用。在EPS生长过程中,细胞表面大部分逐渐被EPS包裹,导致细胞外膜上的多个c型细胞色素无法与电极表面相互作用进行直接电子传递。1) EPS基质中直接存在c型细胞色素与核黄素。EPS中大量存在的羟基、羧基、酮基等功能基团与胞外DNA(E-DNA),可将核黄素、吩嗪等电子传递介体吸附或结合在基质中。肖等仅在提取EPS后检测到核黄素/MtrC结合的差分脉冲伏安峰,可能是由于EPS中多糖吸附或结合核黄素分子,物理“阻断”了电子传递介体与细菌外膜c型细胞色素的结合;而实际形成的EPS构成复合电子传递网络,增加了生物膜内部的电子传递路径,提升了EPS基质中的电子传递效率。2) EPS促进间接电子传递过程,EPS的存在使电子传递介体在细胞与电子供体/受体间维持高浓度水平,不易扩散。微生物腐蚀已成为金属材料研究的重要分支。徐等根据厌氧代谢类型与电子传递方式,将微生物腐蚀分为Ⅰ型与Ⅱ型两类。Ⅰ型微生物腐蚀指靠近金属表面的底层生物膜因缺乏碳源,直接以金属(如Fe⁰)为电子供体获取能量。由于金属阳极释放的电子无法像溶液中的离子一样自由“游动”,电子必须穿过铁表面的生物膜,再穿过细胞膜进入细胞质,还原胞内电子受体并释放能量。阴极去极化理论与生物催化阴极硫酸盐还原理论涉及的SRB金属腐蚀机制均属于Ⅰ型微生物腐蚀。Ⅱ型微生物腐蚀由微生物分泌的腐蚀性代谢产物(包括质子与未解离的有机酸)引发。这类氧化剂无需生物膜或生物催化参与,直接在胞外从金属阳极获取电子。生物膜可充当扩散屏障,维持局部高代谢产物浓度,引发严重的金属局部腐蚀。SRB代谢释放的H₂S腐蚀属于Ⅱ型微生物腐蚀。胞外电子传递概念源自微生物燃料电池。微生物燃料电池是指以生物膜为催化剂,将有机物氧化产生的化学能直接转化为生物电能的技术。当具有产电能力的微生物参与微生物燃料电池时,胞外电子传递方向为从细胞向外传输至胞外电极(如不溶性Fe(III)、Mn(III)、Mn(IV)等氧化物),即有机碳氧化释放的电子从细胞质传输至胞外金属氧化物阴极。当产电微生物细胞内缺乏有机碳源作为电子供体时,会引发胞外电子传递逆转,导致微生物腐蚀。徐等比较了不同碳含量培养基中碳源饥饿程度不同的普通脱硫弧菌引发的微生物腐蚀差异,发现ATCC 1249培养基与有机碳减少90%、99%的培养基中,在C1018碳钢片上生长的细菌,碳源饥饿但未完全饥饿时,生物膜引发的金属腐蚀最严重。克劳沃特等与黄等设计了以生物阴极替代氧阴极的微生物燃料电池。此时,电子从阳极释放进入胞外环境,到达覆盖生物阴极表面的生物膜,再穿过细胞壁进入阴极生物膜细胞,电子从阴极生物膜到阴极的传递方向与微生物腐蚀一致。因此,生物膜中的电子传递通常具有可逆性,微生物腐蚀中的电化学机制与电子传递方式与微生物燃料电池生物阴极相同,可基于微生物输出电子路径探究胞外电子如何通过生物膜输入胞内。微生物燃料电池中的胞外电子传递分为两类:直接电子传递(包括直接电子接触与细菌导电菌毛/纳米线)、间接电子传递(包括电子传递介体介导的电子穿梭)。奥奈达希瓦氏菌MR-1可通过胞外底物与细胞表面具有氧化还原活性的多血红素细胞色素接触,实现直接电子传递,还原胞外电子受体。原卟啉IX结构通过硫醚键与含-CXXCH-基序的肽链共价结合(X可为任意氨基酸),该基序提供组氨酸轴向配体,使卟啉环中心的铁离子以组氨酸/组氨酸轴向方式连接。多血红素细胞色素是奥奈达希瓦氏菌MR-1对胞外受体呼吸还原过程的基础,通过一系列涉及Fe³⁺/Fe²⁺氧化还原对的蛋白内电子传递步骤,支持快速电子传递。希瓦氏菌细胞质中首先发生有机底物的氧化,该过程释放的电子通过起源于内膜、跨越周质空间与外膜、延伸至胞外环境的氧化还原蛋白网络传递。内膜中存在的可溶性电子载体泛醇(QH₂)可结合并传递电子;QH₂由细胞质中泛醌(Q)还原生成,TorC与CymA两种多血红素细胞色素催化Q的再生。电子到达周质空间后,NO₃⁻、NO₂⁻、延胡索酸等末端电子受体可穿过外膜,分别被多血红素细胞色素NapAB、NrfA与FccA还原。对于石墨阳极、柠檬酸铁、Fe(III)与Mn(IV)的水合氧化物等电子受体,电子需穿过外膜进入胞外环境。该过程涉及Mtr/OmcA通路,MtrCAB通道由周质空间十聚体细胞色素(MtrA)、跨膜孔蛋白(MtrB)与周质空间十聚体细胞色素(MtrC)组成;MtrF、MtrD与MtrE组成MtrFDE复合物,整体结构与MtrCAB相同。电子从细胞周质空间依次经MtrA、MtrB,再从MtrB传递至MtrC或另一种外膜细胞色素OmcA,最终到达细胞周围环境。
图2 来自谢瓦内拉菌MR-1的多血红素细胞色素,以指示它们的细胞位置和作用
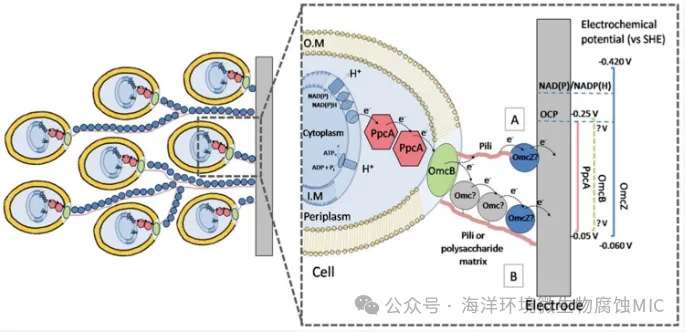
多血红素细胞色素的血红素紧密排列,大部分通过范德华力相互接触。电子在血红素铁离子中心15.5 Å范围内,通过Fe³⁺与Fe²⁺的相互转化发生单步隧穿。长程多步电子跳跃需氧化还原梯度驱动。氧化态Fe³⁺浓度随与阳极表面距离的增加而降低,电子从低电位Fe²⁺向高电位Fe³⁺传递的趋势构成生物膜中的氧化还原梯度。阳极释放的电子首先传递至血红素组分Fe³⁺,使其还原为Fe²⁺;Fe³⁺/Fe²⁺电位差驱动电子在后续多血红素细胞色素内部或之间跨越空间能垒直接跳跃,量子隧穿效应允许该过程发生,即电子沿血红素链从一个氧化还原中心跳跃至另一个,实现数十纳米距离的电子传递。硫还原地杆菌有机物氧化产生的电子首先经NADH脱氢酶传递至醌库,再从醌库传递至MacA蛋白,随后电子从呼吸链释放至细胞周质空间,传递至周质空间c型细胞色素过氧化物酶A(PpcA),该蛋白被认为与外膜中的OmcB相互作用。博南尼等讨论了硫还原地杆菌的两种胞外电子传递机制:类金属导电模型与电子跳跃(超交换)模型。类金属导电模型认为,电子沿生物膜基质中高密度排列的c型细胞色素传递;电子跳跃模型则认为,电子通过细胞色素内部或之间的氧化还原中心隧穿或跳跃传递。连接每个生物膜细胞与电极的导电菌毛,支持c型细胞色素在生物膜基质中有序排列,可在微生物燃料电池中产生高密度电流,实现向Fe(III)氧化物的长程电子传递。 硫还原地杆菌需要导电菌毛作为生物“菌毛”,将电子从细胞膜传递至胞外环境;王等指出,硫还原地杆菌外表面的c型细胞色素OmcS可组装成细丝,是该菌表达的最丰富导电细丝,参与微生物-电极交换与腐蚀中的长程胞外电子传递。刘等通过直接观察硫还原地杆菌细胞伸出的细丝,证实了上述结论。
图3 从内膜到电极的电子传输过程在硫还原拟杆菌生物膜中的示意图
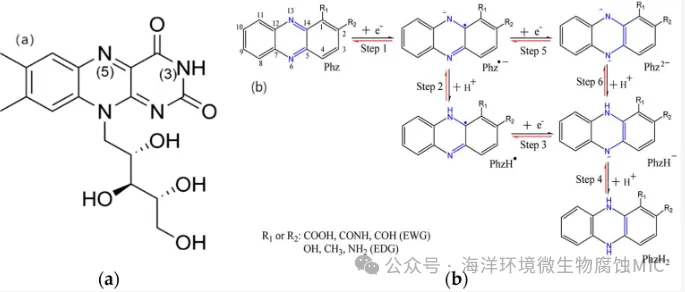
核黄素与吩嗪电子传递介体是细胞周围存在的具有氧化还原能力的可溶性电子载体。电子传递介体可逆地充当中间电子受体或供体,在EPS不同位置接收电子,再释放至下一个电子传递介体或末端电子受体,有效提升微生物胞外电子传递效率。核黄素类似物(如核黄素、黄素腺嘌呤二核苷酸(FAD)、黄素单核苷酸(FMN))是常见的电子传递介体。核黄素是FAD与FMN生物合成的前体,其结构中的异咯嗪环是决定黄素类化合物电子结合能力的主要组分。核黄素在氧化还原过程中可存在三种形式:氧化态核黄素(Flₒₓ)、自由基态核黄素(Flᵣₐd·⁻)、还原态核黄素(Flᵣₑd²⁻)。由于Flᵣₐd·⁻与Flᵣₑd²⁻的中点电位仅相差0.06 V,适合作为胞外电子载体,与细胞色素或金属发生单电子或双电子反应。马尔西利等采用电化学技术研究了两株希瓦氏菌以胞外电极为呼吸电子受体的电子传递过程,发现细胞主动分泌的核黄素发挥重要作用。吩嗪类是一类含氮杂环化合物,包括1-羧酸吩嗪(PCA)、绿脓菌素(PYO)、1-甲酰胺吩嗪(PCN)、1-羟基吩嗪(1-OHPHZ)等,PCA是PYO、PCN等的合成前体,取代基的性质与位置不同,导致多种吩嗪类化合物的理化性质差异显著。吩嗪存在三种氧化态:Phz、Phz·⁻、Phz²⁻,每种氧化态均对应相应的质子化形式。吩嗪类似物可作为电子载体接收与释放电子,发生可逆电子氧化还原过程。冯等将铜绿假单胞菌的PCA合成途径异源导入大肠杆菌,使PCA在大肠杆菌中成功表达,提升了大肠杆菌的产电能力与胞外电子传递效率。
图4 (a) 核黄素(维生素B2);(b) 氟嗪的电子转移过程
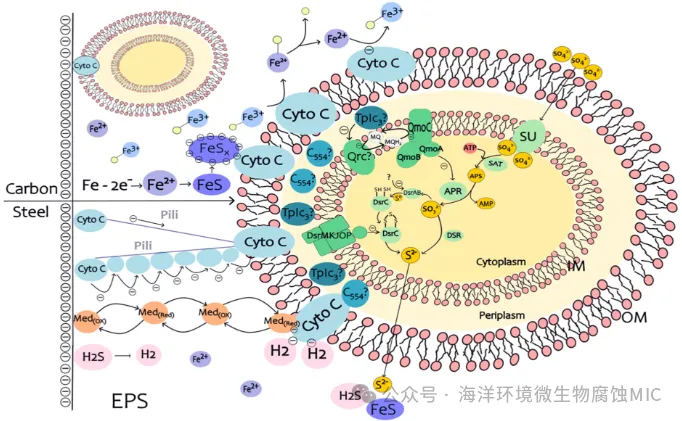
SRB的生命代谢过程优先以环境中的有机碳源为电子供体;当微生物富集繁殖在金属材料表面形成生物膜后,底层生物膜细胞无法直接从外界获取碳源以维持细胞生长所需能量。位于底层的SRB细胞会以金属为电子供体,直接利用生物阴极内的电子还原SO₄²⁻并进行厌氧呼吸,引发金属腐蚀。如图5所示,SRB诱导的微生物碳钢腐蚀过程中发生的电子传递,同样涉及上述微生物燃料电池中的胞外电子传递方式与机制。
图5 硫酸盐解离还原在硫酸盐还原菌诱导的微生物碳钢腐蚀中的完整过程示意图,其中电子从金属阳极传递到胞外聚合物;外膜、周质膜和内膜;然后到达细胞质。
王等指出,SRB细胞外膜上的c型细胞色素等电子穿梭蛋白,使细胞可直接利用胞外不溶性碳钢中的电子,并将其穿过细胞壁传递至胞内,引发碳钢腐蚀。谢拉尔等发现,当培养基中无有机碳源作为电子供体时,从油井分离的SRB生长的菌毛会将细胞与碳钢表面连接,将胞外阳极释放的电子传递至SRB内部用于硫酸盐还原。阿尔拉马等采用多种电化学测试方法证实,导电纳米线通过促进电子传递过程,显著加速SRB对C1020碳钢的腐蚀。张等与李等分别在培养基中添加核黄素与FAD两种电子介体,发现SRB加速了C1018碳钢与304不锈钢的金属腐蚀,出现更严重的点蚀坑与挂片失重。此外,考虑到EPS中的复杂组分,基质中的多糖、蛋白质、胞外DNA均具有一定导电性,可在微观层面形成网状结构,允许部分胞外电子传递过程中电子直接通过,或结合多种电子传递介体,影响电子传递效率。腐殖质也是EPS的重要组分,醌类腐殖酸可可逆还原为氢醌,作为电子传递介体参与SRB厌氧呼吸。H₂S与FeS是SRB在EPS中分泌的两类代谢腐蚀产物,可在碳钢表面发生还原反应生成富电子H₂,硫化铁(FeSₓ)得电子后传递至SRB细胞外膜上的电子传递链。Fe³⁺也可作为电子供体;EPS中存在羧基、酰胺基等多种氧化还原功能基团,会与Fe³⁺络合,当络合物与细胞外膜表面c型细胞色素距离极近(<2 nm)时,Fe³⁺通过电子隧穿还原为Fe²⁺;Fe²⁺可与EPS中的葡萄糖醛酸结合形成新络合物,该络合物不稳定易降解;游离Fe²⁺若迁移至外膜附近,可作为底物被c型细胞色素重新氧化,电子随后进入胞质用于硫酸盐异化还原。 SRB诱导的微生物腐蚀过程中,金属阳极的电子经直接/间接电子传递路径穿过EPS与外膜后,在细胞周质空间的传递需多种细胞色素或电子载体参与。Ⅰ型四聚体c₃细胞色素(TpIc₃)由cycA基因编码,是脱硫弧菌属周质空间中含量最丰富的c型细胞色素。凯勒等利用缺失TpIc₃的阿拉斯加脱硫弧菌G20突变体发现,当以胞内乳酸或丙酮酸为硫酸盐异化还原过程的电子供体时,乳酸氧化产物丙酮酸再氧化或丙酮酸直接氧化产生的电子,部分迁移至周质空间与TpIc₃结合,再传递至具有甲基萘醌(MQ)还原酶活性的跨膜复合物QrcABCD,生成甲基萘醌醇(MQH₂),还原另一种跨膜复合物QmoABC。穆拉利等探究了共生SRB的呼吸通路,其中厌氧甲烷氧化古菌ANME将甲烷氧化产生的电子传递给四类主要共生SRB类群。c₅₅₄细胞色素是SRB形成电子传递链的保守组分之一,存在于所有四类SRB分支中。位于周质空间的c₅₅₄细胞色素将电子传递至内膜中的醌库还原酶,生成甲基萘醌醇或泛醇。TpIc₃与c₅₅₄细胞色素是SRB细胞周质空间中参与电子传递的常见细胞色素,但二者是否参与胞外金属阳极产生的电子向胞内传递过程,以及该过程中还涉及哪些确定的细胞色素或电子载体,仍需进一步实验研究。在SRB厌氧条件下的硫酸盐呼吸中,异化硫酸盐还原(DSR)过程如图5所示:胞外SO₄²⁻通过细胞质膜上的硫酸盐摄取蛋白(SU)捕获摄入;在细胞质中与ATP中的磷酸基团结合,经ATP硫酸化酶(Sat)激活生成5'-腺苷磷酰硫酸(APS);随后经腺苷酰硫酸还原酶(Apr)催化,APS还原为SO₃²⁻并释放AMP;SO₃²⁻经亚硫酸盐还原酶(DSR)直接作用,或经亚硫酸盐还原酶、连三硫酸盐还原酶、硫代硫酸盐还原酶三种酶间接作用,还原为S²⁻,并以H₂S形式通过被动运输扩散出细胞膜。两种末端还原酶(APS还原酶AprAB与异化亚硫酸盐还原酶DsrAB)均为可溶性,因此不直接参与膜相关电子传递。关于AprAB与DsrAB电子供体的探究,皮雷斯等与曼德等首次描述了QmoABC复合物与DsrMKJOP复合物参与硫酸盐还原过程。AprAB是αβ异二聚体铁硫黄素酶,α亚基含催化位点,与FAD辅因子非共价结合;β亚基含两个[4Fe4S]金属簇,其中靠近FAD辅因子的β亚基内部[4Fe4S]为中心I,另一个更暴露于溶剂的中心II接收并传递来自电子供体的电子,经中心I传递至催化位点的FAD部分。AprAB中的底物扩散通过部分暴露于溶剂的催化位点到达包裹的FAD。在许多硫酸盐还原微生物中,qmoABC基因与aprBA基因相邻,作为sat-aprBA-qmoABC基因簇的一部分,强烈提示QmoABC参与AprAB的电子传递。拉莫斯等通过免疫沉淀与表面等离子共振实验证实,QmoABC复合物与AprAB之间存在直接相互作用。QmoABC复合物由两个胞质亚基(QmoAB)与一个细胞膜亚基(QmoC)组成,其中QmoA与QmoB均为可溶性铁硫黄素蛋白,QmoA与AprAB相互作用,QmoB功能尚不明确,可能具有其他生理伴侣作用。QmoC亚基属于膜细胞色素b家族,疏水C端结构域含六个跨膜螺旋,结合两个血红素b基序,负责与内膜中醌库的电子交换与传递。杜阿尔特等通过电化学测量研究了翻转与非翻转条件下的蛋白质-蛋白质电子传递,证实非翻转条件下,电子从醌库经QmoC与QmoA传递至AprAB的β亚基与α亚基,在催化位点FAD发生两次连续的单电子还原。DsrAB由α₂β₂四个亚基组成,每个αβ单元含两个铁氧还蛋白辅因子,仅一个具有催化活性。四个铁氧还蛋白辅因子轴向耦合[4Fe4S],并通过半胱氨酸残基固定。DsrC作为DsrAB的生理伴侣,其柔性羧基端臂含两个高度保守的半胱氨酸(CysA、CysB),具有氧化还原活性。膜结合复合物DsrMKJOP被认为与硫酸盐异化还原过程的电子供体相关,包含周质空间(三血红素c型细胞色素DsrJ与多铁氧化还原蛋白DsrO)、膜(二血红素b型细胞色素DsrM、DsrP)与细胞质(铁硫蛋白DsrK)多个亚基,分为面向周质空间的DsrJOP模块(可能参与周质空间与内膜中醌库的电子交换)与面向细胞质的DsrMK模块(参与内膜与细胞质间的电子交换)。根据帕雷等提出的经三个双电子步骤进行的六电子反应,DsrAB依次接收两个双电子,在活性中心生成[Sᴵᴵ]与[S⁰]。[S⁰]与DsrC中的CysA结合形成过硫化物,随后CysB取代形成分子内二硫键桥。DsrC三硫化物作为底物,接收来自DsrK亚基的两个电子被还原,最终释放硫化物。
针对特定条件下EPS对微生物腐蚀与胞外电子传递的影响、微生物燃料电池与微生物腐蚀中胞内外电子传递的方式、机制、路径存在的问题,以及影响腐蚀过程的实际环境因素,提出以下思考:
EPS中发生的生物诱导矿化可有效抑制金属腐蚀,为防腐与新型天然绿色缓蚀剂研发提供新思路。SRB诱导的生物矿化会在细胞表面形成MeS/MeCO₃矿物沉淀,但其自身生理代谢活动的变化如何具体诱导胞外矿化发生,仍需进一步实验探究。
当前微生物燃料电池中胞外电子传递研究较多,电子在15.5 Å范围内发生单步隧穿、在氧化还原梯度驱动下长程跳跃的传递机制,从量子力学角度拓展了生物能学层面电子传递的探究视野;而微生物腐蚀中胞外电子传递的方式、机制与路径的阐明,仅源于可逆过程的推断,缺乏实质性、更直接的实验证据。
SRB诱导碳钢腐蚀过程中,EPS层、外膜、周质空间、内膜中参与电子传递的细胞色素或其他电子载体的类型及作用,仍需进一步实验研究。基因突变、蛋白质组学分析、代谢组学等分子工具,在关键组分鉴定中可能发挥重要作用。
实际腐蚀环境通常更复杂,温度、pH、阴离子、共生菌等是否及如何影响SRB碳钢腐蚀过程,仍需进一步认知与探讨;SRB对其他金属材料(如不同浓度碳钢、其他合金等)在生物膜中发生的电化学机制与路径是否一致、腐蚀机制是否相同,有待验证。
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。