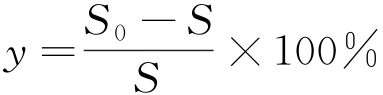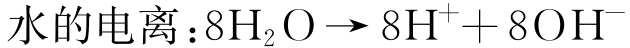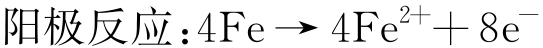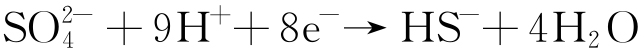自然水体中存在大量微生物,在工业生产中用水设备可能发生微生物腐蚀,引发设备点蚀穿孔等问题。在冷却水系统中,微生物黏附在换热管表面形成生物膜,导致热传递效率降低、管道堵塞[1],并造成能量损耗和经济损失[2]。选用耐蚀材料是控制微生物腐蚀的方法之一,但这会造成投入成本过大。另外,投加缓蚀剂和杀菌剂也是防治微生物腐蚀[3]的常用方法。
缓蚀剂可以抑制腐蚀电池阳极或阴极反应的进行,从而降低金属的腐蚀速率,其缓蚀效果与水中微生物种类相关,因此在投加时需考虑微生物因素[4]。杀菌剂通过将微生物杀灭,从源头上控制微生物腐蚀,但使用量较大,可能对环境造成不利影响,且长期使用单一种类杀菌剂,会使微生物产生耐药性,增大去除微生物的难度[5]。
ZnO纳米粒子对大肠杆菌[6]、金黄色葡萄球菌[7]及绿脓杆菌[8]等细菌普遍具有杀灭性,杀菌效果与细菌种类相关,如:10 mg·L-1 ZnO纳米粒子对枯草芽孢杆菌CB310菌株的抑制率可达到90%,而相同含量下对大肠杆菌DH5α菌株的抑制率仅为14%[9]。目前,有关纳米粒子杀菌性的研究对象多为致病菌,对腐蚀性细菌的杀菌性能研究不多。为此,作者采用微生物培养与检测、电化学测试及表面分析等方法研究了ZnO纳米粒子对硫酸盐还原菌(SRB)的抑菌性能及对304不锈钢的微生物腐蚀行为影响。
1. 试验
1.1 试验材料和介质
试验用ZnO纳米粒子平均粒径为25 nm,图1为用FEOL JEM 2100F型透射电子显微镜(TEM)表征的ZnO纳米粒子形貌。试验材料为304不锈钢,所用药品均购自阿拉丁工业公司。
试验溶液为模拟地表水(SCW),主要组成为:7.5 mmol·L-1 NaCl,2.0 mmol·L-1 NaHCO3,3.5 mmol·L-1 Na2SO4,0.25 mmol·L-1 MgSO4及0.5 mmol·L-1 CaCl2。将培养基中的SRB以1∶10(体积比)接种至经高压灭菌后的模拟地层水中,用石蜡密封维持溶液的厌氧环境。
1.2 细菌培养和计数
试验用菌种为SRB,取自池塘污泥,经提取并纯化后得到,微生物种群分析检测出该菌株为脱硫弧菌属。用于菌种培养和活化的液体培养基的组成为:0.2 g·L-1 MgSO4·7H2O,0.01 g·L-1 KH2PO4,0.2 g·L-1(NH4)2Fe(SO4)2,10.0 g·L-1 NaCl,4.0 m L·L-1乳酸钠,1.0 g·L-1酵母浸汁,0.1 g·L-1维生素C。调节培养基p H至7.0~7.2,保持菌种的培养温度为35 ℃。
溶液中SRB的数量测定采用稀释平板计数试验。将制备好的琼脂平板(含不同量ZnO纳米粒子)在35 ℃条件下进行培养,经48 h培养后对菌落计数,并通过式(1)计算抑菌率。
|
|
(1) |
式中:y为抑菌率,%;S0为对照样品平均菌落数;S为试样样品平均菌落数。
1.3 水中自由基的测定
水中羟基自由基(·OH)测定:以对苯二甲酸为荧光捕捉剂,使用RF-5301pc型荧光分光光度计获得水中·OH对应的三维激发-发射矩阵(EEM)荧光光谱。
超氧阴离子自由基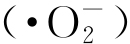 测定:采用羟氨氧化法[10],以模拟地表水代替纳米氧化锌悬浮液作为参比溶液。
测定:采用羟氨氧化法[10],以模拟地表水代替纳米氧化锌悬浮液作为参比溶液。
1.4 电化学测试
将304不锈钢电极在不同ZnO纳米粒子含量的模拟地表水(含菌和无菌)中浸泡7 d后进行电化学测试。测试在CHI660e型电化学工作站上完成并采用三电极体系。304不锈钢电极作为工作电极,饱和甘汞电极作为参比电极,铂电极作为辅助电极。电化学阻抗谱的测试频率范围为0.01 Hz~100 k Hz,幅值为5 m V。极化曲线测试的扫描速率为1 m V·s-1,温度为35 ℃。
1.5 金属表面形貌观察
将304不锈钢挂片置于含ZnO纳米粒子的有菌体系中浸泡7 d,取出后用2%戊二醛固定生物膜,采用扫描电镜(SEM)对挂片表面形貌进行观察,并采用扫描电镜附带的能谱分析仪(EDS)对其表面微区化学成分进行分析。
2. 结果与讨论
2.1 ZnO纳米粒子的抑菌性能
细菌在溶液中接触到材料后会在材料表面形成生物膜,细菌的附着被认为是微生物腐蚀的前兆[11]。不锈钢表面黏附的菌量与纳米粒子的抑菌性能相关。测定了水中不同含量ZnO纳米粒子对SRB的抑菌性能,如表1所示。结果表明,ZnO纳米粒子有一定的抑菌性,随ZnO纳米粒子含量增大,抑菌性能逐渐增强,当其质量浓度为100 mg·L-1时,抑菌率可达89.3%。
| ZnO纳米粒子质量浓度/(mg·L-1) | 10 | 20 | 50 | 100 |
|---|---|---|---|---|
| 抑菌率/% | 27.2 | 41.2 | 77.1 | 89.3 |
一般认为,纳米粒子在水中可以产生活性氧物质,活性氧物质(包括·OH、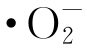 等)诱导细菌氧化应激是纳米粒子具有抗菌性的重要原因[12]。
等)诱导细菌氧化应激是纳米粒子具有抗菌性的重要原因[12]。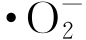 和·OH均具有很强的氧化性,可破坏细胞内的有机物,进而破坏微生物的结构并抑制其生理活性[13]。ZnO纳米粒子的抑菌性能与其在水溶液中催化产生的活性氧物质相关。当体系中存在ZnO纳米粒子时,可在体系中检测到
和·OH均具有很强的氧化性,可破坏细胞内的有机物,进而破坏微生物的结构并抑制其生理活性[13]。ZnO纳米粒子的抑菌性能与其在水溶液中催化产生的活性氧物质相关。当体系中存在ZnO纳米粒子时,可在体系中检测到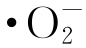 。表2为水中检测到的
。表2为水中检测到的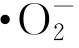 含量与ZnO纳米粒子含量的对应关系。可见,随着ZnO纳米粒子含量升高,水中
含量与ZnO纳米粒子含量的对应关系。可见,随着ZnO纳米粒子含量升高,水中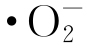 的含量也随之增大。图2为不同ZnO纳米粒子含量水溶液的荧光光谱。图2(b)、(c)、(d)中,荧光位置的出现表明水中产生了·OH(最高峰出现在激发波长Ex为320 nm、发射波长Em为430 nm处),且荧光强度随ZnO纳米粒子含量增大而增强,表明随ZnO纳米粒子含量增大,水中生成了更多的·OH。水中活性氧物质的产生主要有以下两方面原因:ZnO纳米粒子自身缺陷导致催化反应生成活性氧物质[14];在试验过程中,自然光导致纳米粒子光催化形成活性氧物质[15]。上述结果说明,添加ZnO纳米粒子可使水中生成强氧化性的活性氧物质
的含量也随之增大。图2为不同ZnO纳米粒子含量水溶液的荧光光谱。图2(b)、(c)、(d)中,荧光位置的出现表明水中产生了·OH(最高峰出现在激发波长Ex为320 nm、发射波长Em为430 nm处),且荧光强度随ZnO纳米粒子含量增大而增强,表明随ZnO纳米粒子含量增大,水中生成了更多的·OH。水中活性氧物质的产生主要有以下两方面原因:ZnO纳米粒子自身缺陷导致催化反应生成活性氧物质[14];在试验过程中,自然光导致纳米粒子光催化形成活性氧物质[15]。上述结果说明,添加ZnO纳米粒子可使水中生成强氧化性的活性氧物质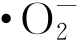 和·OH,从而对SRB产生了较强的抑制作用。
和·OH,从而对SRB产生了较强的抑制作用。
| ZnO质量浓度/(mg·L-1) | 20 | 50 | 100 |
|---|---|---|---|
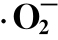 质量浓度/(mg·L-1) 质量浓度/(mg·L-1) |
0.152 | 0.178 | 0.208 |
2.2 ZnO纳米粒子对不锈钢微生物腐蚀行为的影响
在不同ZnO纳米粒子含量的模拟地层水中浸泡7 d后,对304不锈钢进行电化学阻抗谱测试,结果如图3所示,采用图4所示等效电路对电化学阻抗谱进行拟合,结果见表3。图中,Rs为溶液电阻,Rct为电荷转移电阻,Rf为不锈钢表面钝化膜电阻,Qdl和Qf分别为用于表示双电层电容和膜电容的常相角元件。
| ZnO质量浓度/(mg·L-1) | Rs/(Ω·cm2) | Ydl/( μS·cm-2·s-n) | ndl | Rct/(kΩ·cm2) | Yf/( μS·cm-2·s-n) | nf | Rf/(MΩ·cm2) | |
|---|---|---|---|---|---|---|---|---|
| 无菌 | 0 | 177.2 | 526.9 | 0.88 | 2.14 | 26.1 | 0.80 | 36.2 |
| 100 | 178.3 | 281.4 | 0.73 | 2.62 | 34.4 | 0.87 | 14.7 | |
| 有菌 | 0 | 91.1 | 397.0 | 0.88 | 0.90 | 460.9 | 0.78 | 0.050 |
| 10 | 86.4 | 194.3 | 0.78 | 0.17 | 314.9 | 0.92 | 0.252 | |
| 20 | 100.0 | 73.2 | 0.67 | 0.19 | 77.9 | 0.78 | 0.479 | |
| 50 | 66.3 | 197.2 | 0.99 | 0.23 | 61.6 | 0.73 | 0.668 | |
| 100 | 86.6 | 117.9 | 0.78 | 0.27 | 75.3 | 0.75 | 1.700 | |
由表3可见,在无菌模拟地层水中,304不锈钢的Rf与Rct值均较大,分别达到36.2 MΩ·cm2和2.14 kΩ·cm2。不锈钢是自钝化金属,在水中溶解氧的作用下可自发钝化[16],具有较好的耐蚀性。在无菌模拟地层水中加入100 mg·L-1 ZnO纳米粒子后,304不锈钢的阻抗值变化较小,说明在无菌溶液中ZnO纳米粒子对不锈钢耐蚀性能的影响较小。而在有菌模拟地层水中,304不锈钢的Rf与Rct均显著减小,分别为0.050 MΩ·cm2和0.90 kΩ·cm2,这表明当体系中存在SRB时,不锈钢表面不易形成钝化膜或形成的钝化膜保护性减弱,使不锈钢的耐蚀性能下降。在有菌模拟地层水中加入ZnO纳米粒子可使304不锈钢的Rf和总电阻(Rct+Rf)明显增大,表明ZnO纳米粒子抑制了SRB对不锈钢的侵蚀作用,但在该体系中304不锈钢的Rct小于其在不含ZnO纳米粒子的有菌体系中的Rct。在不含ZnO纳米粒子的有菌体系中,细菌黏附在不锈钢表面形成了较厚的生物膜,生物膜的存在使电荷转移过程受到阻碍[17],但同时SRB生物膜下不锈钢表面也难以形成钝化膜,因此在该体系中不锈钢具有较大的Rct值和较小的Rf值。随着体系中ZnO纳米粒子含量的增加,Rct与Rf均出现增大,不锈钢耐微生物腐蚀性能增强。
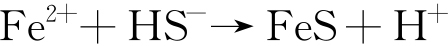
在不同ZnO纳米粒子含量的模拟地层水中浸泡7 d后对304不锈钢进行极化曲线测试,结果如图5所示。钝态电流密度Jp的大小可反映不锈钢的耐蚀性能,其值越小,钝化膜对不锈钢的保护性能越好,不锈钢的耐蚀性能越强[18]。由图5可见,在无菌模拟地层水中,304不锈钢具有较小的钝态电流密度,ZnO纳米粒子添加与否对极化曲线影响不大;在有菌模拟地层水中,304不锈钢的钝态电流密度显著增大,钝化膜的保护性能下降。这是由于SRB的代谢产物在金属表面积累使钝化膜受到破坏,不锈钢的耐蚀性降低。根据生物催化阴极还原理论[19],在SRB腐蚀体系中存在如下反应:
|
|
(2) |
|
|
(3) |
SRB细胞内发生的阴极反应:
|
|
(4) |
|
|
(5) |
腐蚀体系的阴极反应在SRB的细胞膜内进行,并生成HS-,Fe2+与HS-结合产生硫化物,使不锈钢的钝化膜受到破坏,加速了不锈钢的腐蚀。
表4为极化电位为0 V时304不锈钢的钝态电流密度,可见在无菌体系中ZnO纳米粒子对不锈钢耐蚀性影响不大,而在有菌体系中添加ZnO纳米粒子可抑制不锈钢的微生物腐蚀。在有菌体系中不锈钢电极的钝态电流密度为15.8 μA·cm-2,添加10 mg·L-1 ZnO纳米粒子后钝态电流密度降为5.78 μA·cm-2,随ZnO纳米粒子含量增大,钝态电流密度减小,这说明ZnO纳米粒子抑制了SRB的生命活动,降低微生物对不锈钢的腐蚀速率。
| ZnO质量浓度/(mg·L-1) | Jp/(肀A·cm-2) | |
|---|---|---|
| 无菌 | 0 | 0.193 |
| 100 | 0.222 | |
| 有菌 | 0 | 15.8 |
| 10 | 5.78 | |
| 20 | 3.35 | |
| 50 | 1.54 | |
| 100 | 1.19 | |
2.3 金属表面形貌
在不同ZnO纳米粒子含量的有菌体系中浸泡7 d后304不锈钢表面的SEM图和EDS谱如图6所示。由图6可见,在不含纳米粒子的含菌溶液中304不锈钢表面SRB数量较多,EDS结果显示表面C、O元素原子分数之和达到76.13%,这说明不锈钢表面被一层生物膜附着。生物膜是由微生物细胞以及包裹在微生物外由细胞自身分泌的胞外聚合物(EPS)构成的聚集体[20],SRB在EPS的黏聚下形成的生物膜较为致密。在含ZnO纳米粒子体系中,随ZnO纳米粒子含量增大,不锈钢表面附着的细菌量减少,且分布更为分散,这表明ZnO纳米粒子抑制了不锈钢表面生物膜的附着。在图6(b)的EDS谱中测得了Zn元素,其应该来自于ZnO纳米粒子。另外,ZnO纳米粒子与SRB的直接接触也可起到杀菌作用[21]。
3. 结论
(1)模拟地层水中ZnO纳米粒子对SRB具有抑菌作用,抑菌率随ZnO纳米粒子含量的增加而增大,当ZnO纳米粒子质量浓度为100 mg·L-1时,抑菌率达到89.3%。ZnO纳米粒子的抑菌机制主要是使水中催化生成强氧化性的活性氧物质·OH和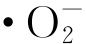 ,这些活性氧物质对SRB产生较强抑菌作用。
,这些活性氧物质对SRB产生较强抑菌作用。
(2)在含SRB的模拟地层水中,304不锈钢产生了微生物腐蚀,在模拟地层水中加入一定量的ZnO纳米粒子可以抑制SRB的活性,降低水中细菌代谢产物并减少不锈钢表面生物膜的附着,明显降低不锈钢的微生物腐蚀速率。加入50 mg·L-1 ZnO纳米粒子可以使304不锈钢在含菌模拟地层水中的钝态电流密度下降一个数量级以上。
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606
- 邮箱:fsfhzy666@163.com
- 腐蚀与防护网官方QQ群:140808414