摘要
采用极化曲线、电化学阻抗谱技术和SEM、EDS、XRD分析方法研究了X70管线钢在含硫酸盐还原菌 (SRB) 的大庆土壤模拟溶液中的微生物腐蚀行为。结果表明,SRB在大庆土壤环境模拟溶液中生长周期分为对数生长期、衰减期和死亡期3个阶段。SRB的新陈代谢对大庆土壤环境产生显著影响:pH值在SRB生长的前2 d降低,然后呈逐渐上升趋势。氧化还原电位在SRB对数生长期降低,在衰减期和死亡期呈增加趋势。溶液电导率在SRB的对数生长期时增加,在衰减期和死亡期呈整体减小趋势。在SRB对数生长期,游离的SRB利用其新陈代谢产物H将硫酸盐还原成硫化物,促进了点蚀的发生;在SRB衰减期,腐蚀产物成团簇状,膜层致密,减缓腐蚀;在SRB死亡期,生物膜脱落,腐蚀产物膜有明显裂纹出现,形成微观腐蚀电池,导致X70管线钢的腐蚀加剧。X70管线钢在SRB的大庆土壤中腐蚀产物为FeS和Fe3O4。
关键词: X70管线钢 ; 大庆土壤 ; 硫酸盐还原菌腐蚀 ; 生长周期 ; 环境参数
埋地钢质管道作为油气运输的大动脉,其可靠性和完整性直接影响着油气资源的输送安全[1]。在油气输送管线的失效事故中,有70%以上是腐蚀问题造成的,其中15%~30%的管线泄漏与微生物腐蚀有关[2]。土壤中微生物种类繁多且代谢活动旺盛,微生物的新陈代谢与管道表面电化学反应中的离子传输过程,共同构成了腐蚀的一个重要环节。微生物的代谢过程几乎可以在所有金属表面进行,导致金属阳极溶解和力学性能的损失[3,4],并生成影响腐蚀的生物膜层[5]。据报道,2006年微生物腐蚀致使美国阿拉斯加州的输油管道泄漏,美国的石油产量大幅降低[6]。硫酸盐还原菌 (SRB) 是导致金属发生微生物腐蚀的最主要的菌种。SRB在大多数情况下是典型的厌氧菌,它们的新陈代谢活动与金属一起导致H2S等强腐蚀性产物的形成[7]。土壤的低浓度氧环境特别适宜SRB的生长。宋博强等[8]研究表明,SRB对X70钢在近中性土壤中腐蚀速率的影响与其生长规律有关。Wu[9]等研究了X80钢在沈阳土壤中的微生物腐蚀行为,认为SRB的新陈代谢诱发了X80钢点蚀的萌发。Xu[10]等研究了A36钢在沈阳土壤中的缝隙腐蚀行为,结果表明:由于生物膜的保护,在早期阶段SRB代谢活动抑制了钢的腐蚀;后期生物膜脱落,A36钢的腐蚀加快。
大庆作为我国重要的石油工业基地,地下铺设大量的油气管道。大庆土壤为我国典型的苏打盐,有碱性、含水率高的特点[11],油田井口微生物含量极高。在众多的土壤微生物腐蚀研究成果中,关于我国大庆土壤中微生物对管线钢腐蚀行为影响的研究甚少。本工作通过电化学方法结合微观观察手段对X70钢在大庆土壤中微生物腐蚀行为进行表征,系统地研究大庆土壤中SRB生长周期对环境参数及X70钢腐蚀行为的影响,研究成果将为管线钢在我国大庆土壤中的微生物腐蚀与防护提供有效的数据支持。
1 实验方法
实验材料为X70管线钢,其化学成分 (质量分数,%) 为:C 0.045,Si 0.26,Mn 1.48,Nb 0.033,Ni 0.16,Cr 0.17,Cu 0.21,S 0.001,P 0.0017,Fe余量。线切割浸泡实验试样尺寸为40 mm×10 mm×2 mm,电化学试样尺寸为10 mm×10 mm×1 mm。电化学试样背面点焊引出铜导线,非工作表面用环氧树脂封装,留出有效面积1 cm2的正方形为工作面。实验前将试样用SiC水砂纸从80#逐级打磨到1500#,然后用丙酮去除油污,去离子水清洗后吹干待用。
根据中国腐蚀与防护网站数据,用分析纯和去离子水配置大庆土壤模拟溶液,其成分 (g/L) 为:NaHCO3 1.726,CaCl2 0.084,MgSO4·H2O 0.061,KNO3 0.086,Na2SO4 0.109,pH值为9.0。
实验所用的SRB菌种为土壤分离纯化后获得。所用培养基 (I) 成分为:0.5 g/L K2HPO4,0.5 g/L Na2SO4,1 g/L NH4Cl,0.1 g/L CaCl2,2 g/L MgSO4·7H2O,1 g/L酵母粉,3 mL乳酸钠;培养基 (II) 为:0.1 g/L抗坏血酸,0.1 g/L保险粉,0.1 g/L硫酸亚铁铵。用4% (质量分数) NaOH溶液调节培养基 (I) 的pH值至7.2。将土壤模拟溶液和培养基 (I) 放入立式压力蒸汽灭菌器当中,在121 ℃下灭菌15 min。培养基 (II) 通过圆筒式过滤器进行过滤,经由紫外线灭菌处理。在生物安全柜中进行接种操作,按照1∶1∶2的比例混合培养基I、II和土壤模拟溶液,再按照1∶100的比例接种SRB,即为有菌溶液。
采用光密度 (OD值) 法,测量SRB在大庆土壤模拟溶液当中的生长曲线。对含SRB的溶液进行提取上清液,连续测量14 d。用紫外分光光度计 (UV-2550型) 进行吸光度 (Abs) 测定,由于吸光度在0.15~1.0范围内与OD值近似相等,从而测得OD值,得到生长曲线。如果测得的OD值超出此范围,则把待测样品用液体培养基进行稀释5~10倍,直至达到此范围,最后的结果与稀释倍数相乘。
采用S220多参数测试仪测量SRB生长对溶液pH值和氧化还原电位的影响。通过DDS-307型电导率仪监测SRB生长对溶液导电性的影响。连续测量14 d。
将试样浸泡在含SRB的大庆土壤模拟溶液中,放置在生物培养箱中恒温培养至不同时间后取出,用5% (体积分数) 的戊二醛固定液固定2 h后,再用不同浓度的乙醇 (30%,50%,80%和100%) 逐级脱水,以最大限度的保持其生物膜的完整性。用SU-8010型扫描电镜 (SEM)、Q500MW型能量色散X射线光谱仪 (EDS)、D8 Advance型X射线多晶粉末衍射仪 (XRD) 观察浸泡不同时期后试样的腐蚀形貌及分析试样的腐蚀产物。
电化学实验采用三电极体系,工作电极为X70管线钢,辅助电极为Pt电极,参比电极为饱和甘汞电极 (SCE)。采用PARSTAT 2273型电化学工作站对浸泡至4,7,10和14 d的试样进行动电位极化曲线和电化学阻抗谱 (EIS) 测量。EIS谱的测量频率为105~10-2 Hz,交流激励信号为10 mV。动电位极化曲线的扫描速率为0.667 mV/s,扫描范围为-0.5 V(vs. OCP) 至0.2 V。本文中所有的电位均相对于饱和甘汞电极 (SCE)。
2 实验结果
2.1 SRB的生长曲线
图1为SRB在大庆土壤模拟溶液中的生长曲线。由图可知,SRB在大庆土壤模拟溶液中生长周期为14 d,大致分为3个阶段:0~4 d为对数生长期,在这个阶段溶液营养充足,SRB迅速繁殖,数量呈对数生长且活性增强,并在第4 d时达到最大值;5~10 d为衰减期,SRB的数量在这个阶段逐渐减少,此时由于营养物质被迅速消耗,SRB死亡数量大于繁殖数量,数量上整体呈下降趋势,其中4~7 d下降速度最快。11~14 d为死亡期,在这一阶段,SRB数量基本保持不变,表明此时已经没有新的SRB生成,SRB消失殆尽。
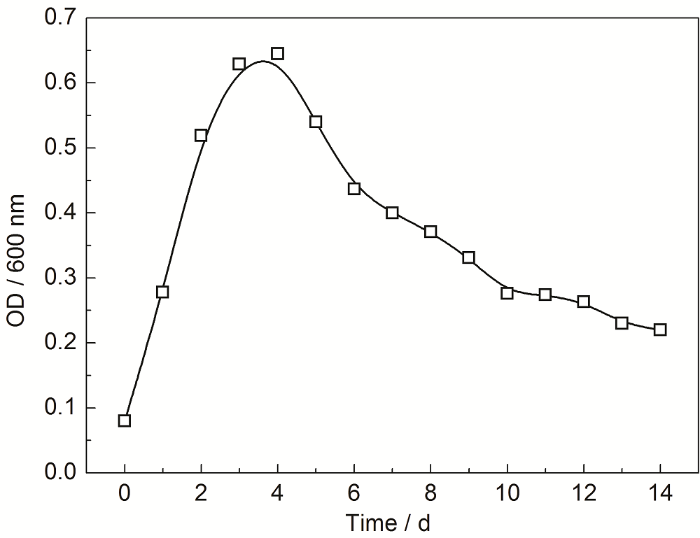
图1 SRB在大庆土壤模拟液中的生长曲线
2.2 SRB生长对环境参数的影响
图2为溶液pH值随SRB生长周期的变化。由图2可知,溶液的pH值在对数生长期第2 d时由9迅速降低至8.07,此后pH值随时间增加呈整体增高趋势,并最终达到8.96,表明SRB新陈代谢能导致pH值增加。
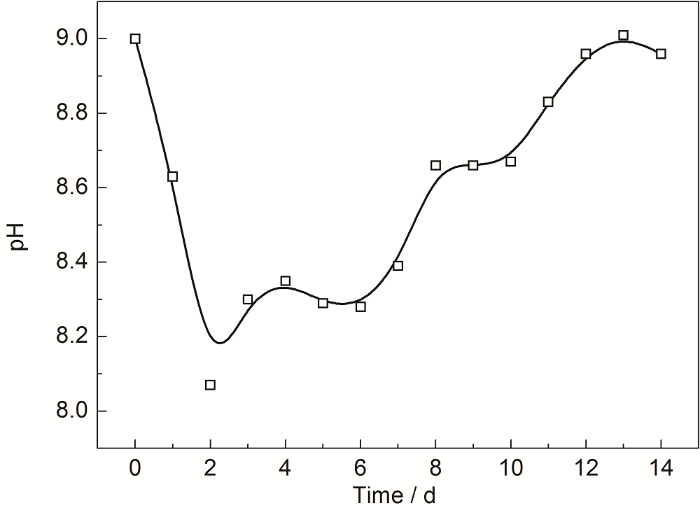
图2 溶液pH值随SRB生长过程的变化
图3为溶液的氧化还原电位Eh随SRB生长周期的变化。由图可知,在SRB的对数生长期Eh从-296 mV降低到-345 mV,然后随着SRB的衰亡,Eh略有增加,当SRB进入死亡期,Eh急剧增加至-201.3 mV。

图3 溶液氧化还原电位随SRB生长过程的变化曲线
图4为溶液的电导率在SRB生长周期内的变化。由图可知,在SRB对数生长期溶液电导率增加,并在第4 d时达到最高值为5030 μs/cm,随着SRB的衰减,电导率呈整体下降趋势,当SRB进入死亡期,电导率急剧下降,最终降到4440 μs/cm。值得注意的是,当SRB进入死亡期,电导率略有上升,这可能是由于金属表面生物膜脱落,不能对金属形成保护作用,此时溶液中侵蚀性离子加速对金属溶解造成的。
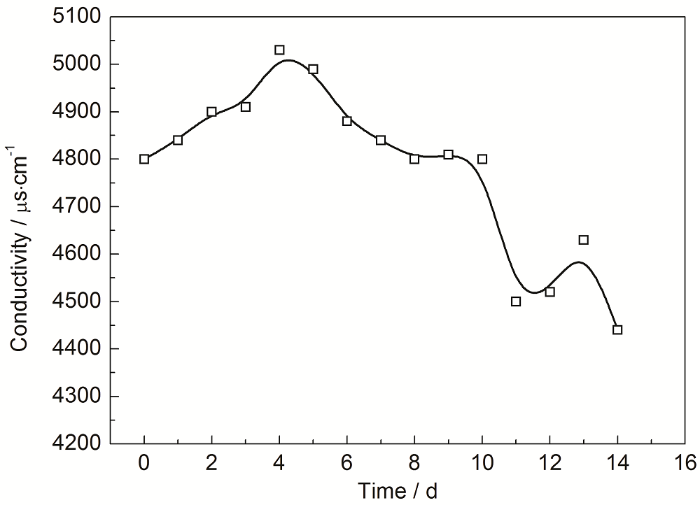
图4 溶液电导率随SRB生长过程的变化曲线
2.3 表面腐蚀产物形貌和成分分析
图5为X70钢在含SRB的大庆土壤模拟溶液中浸泡至4,7和14 d的SEM图像和EDS结果。从图5a1中可以看出,浸泡至第4 d时,X70钢表面覆盖有生物膜,且伴随有点蚀坑;浸泡至7 d时 (图5a2),生物膜和腐蚀产物团簇生长在钢基体表面。浸泡至14 d,钢基体表面的腐蚀产物膜增厚,并出现明显裂纹 (图5a3)。EDS能量谱结果表明:X70钢在含SRB的大庆土壤模拟溶液中浸泡4、7和14 d的腐蚀元素主要为C、O、Fe、P、S、Mn,同时含有Na、Mg、Ca等少量的无机离子。其中图 (5a2) 中腐蚀产物A点的P含量高于光滑表面B点,而S含量则低于B点;同样,图5a3中C点的P含量大于D点,而S含量小于D点。由此可知,团簇状腐蚀产物主要为磷化物,而硫化物主要分布在电极表面。
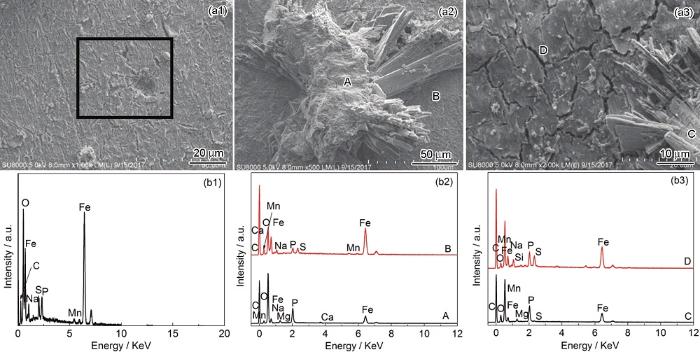
图5 X70钢在含SRB的大庆土壤模拟溶液中的SEM像和EDS结果
图6为X70钢在含SRB的大庆土壤模拟溶液中浸泡14 d的XRD结果。由图可知,腐蚀产物主要为FeS和Fe3O4,Fe3O4可能是样品取出后被空气氧化形成的。
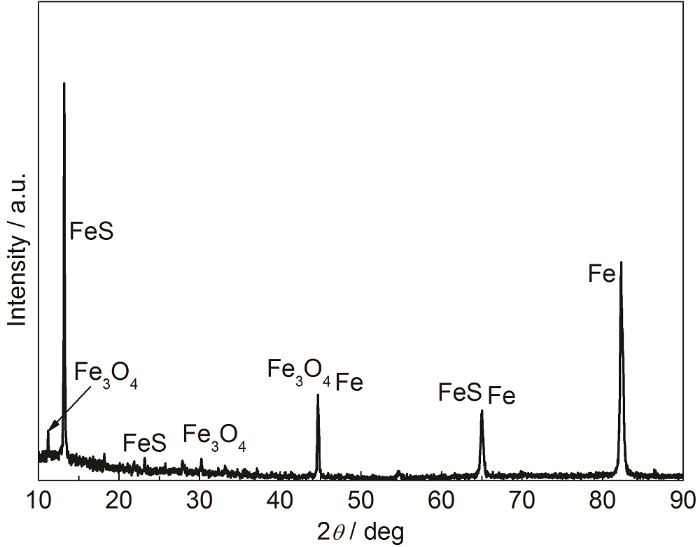
图6 X70钢在含SRB的大庆土壤模拟溶液中浸泡14 d的XRD谱
2.4 电化学实验
2.4.1 EIS谱
图7为X70钢在含SRB的大庆土壤模拟溶液中的EIS结果。从Nyquist图可以看出,在含SRB的大庆土壤模拟溶液中不同浸泡时间的X70钢电化学阻抗谱均呈现为单一容抗弧特性,表明腐蚀过程由电化学反应控制。容抗弧半径大小一般与金属耐蚀性有关,容抗弧半径越大表明耐蚀性越好。浸泡7 d的试样容抗弧半径最大,10和4 d次之,14 d的容抗弧半径最小。在Bode图中|Z|-lgf曲线可以看出,在浸泡7 d时系统中的电阻特性最大,此时电极表面可能形成了一层高阻抗低电容的隔绝层[12];而4,10和14 d的|Z|-lg f的曲线几乎重合。Bode图中相位角在浸泡第7 d时达到最大,最大相位角接近90°,说明此时微生物腐蚀产物膜完整。
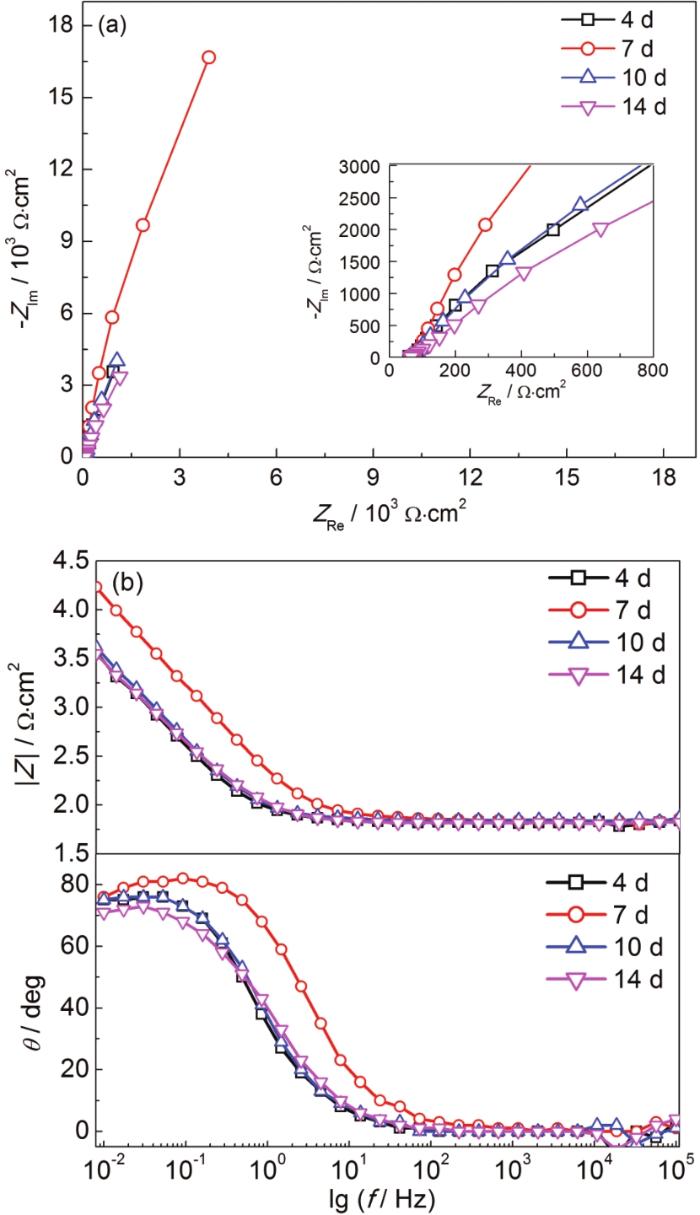
图7 X70钢在含SRB的大庆模拟溶液中浸泡不同时间的EIS图
采用ZsimpWin软件和图8中的等效电路图对EIS结果进行拟合,拟合结果见表1。其中,Rs为溶液介质电阻,Qdl为双电层电容,Rf是试样表面膜电阻,Rct是电荷转移电阻,CPE为双电层常相位角元件,其大小主要与电极表面双电层的介电性能相关,由两个参数 (常相系数Y0和弥散系数n) 决定[13],n的取值范围为0<n<1,表示弥散效应的程度。CPE1为膜电容,CPE2为双电层电容。
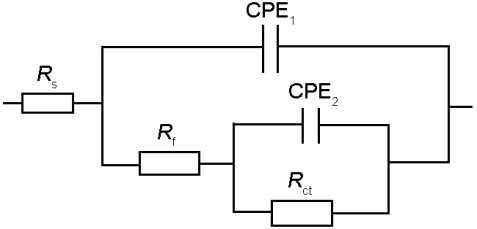
图8 X70钢在含SRB的大庆土壤模拟溶液中EIS等效电路图
表1 X70钢在含SRB的大庆土壤模拟溶液中EIS拟合结果
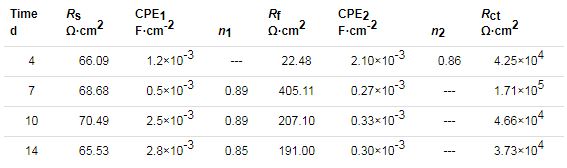
由表1可知,电荷转移电阻Rct为7 d>10 d>4 d>14 d,膜电阻Rf为7 d>10 d>14 d>4 d,7 d时的电荷转移电阻Rct和膜电阻Rf之和最大,14 d的电荷转移电阻Rct和膜电阻Rf之和最小,即第7 d时X70钢的耐蚀性最好,第14 d时最差。这表明X70钢在含SRB的大庆土壤模拟溶液中的耐蚀性呈先增大后减小。
2.4.2 极化曲线
X70钢在含SRB的大庆土壤模拟溶液中的极化曲线见图9。由图可知,各条极化曲线均表现出钝化行为,其中X70钢在含SRB的大庆土壤模拟溶液中浸泡7 d时的腐蚀电流密度最小,为1.776 A/cm2,说明此时耐蚀性最好。而其它时间的极化曲线差别不大,第14 d时的腐蚀电流密度较大,为4.203 A/cm2,说明此时耐蚀性最差。这与电化学阻抗结果相一致。文献[11]表明,X70钢在无菌的大庆土壤中的极化曲线均为活化,并没有出现钝化。而在本实验中,在SRB的作用下,X70钢发生了“钝化”行为,这是由于X70钢表面形成的生物膜在一定程度上阻碍了金属的阳极溶解反应。
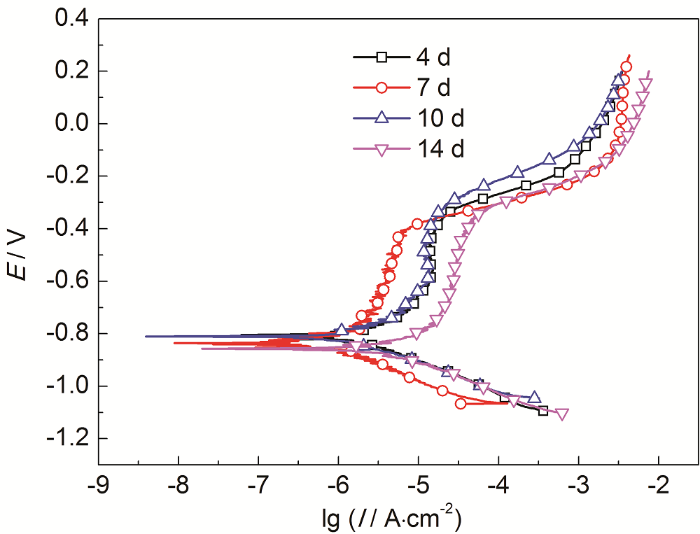
图9 X70钢在含SRB的大庆土壤模拟溶液中浸泡不同时间的极化曲线
3 分析与讨论
3.1 SRB生长对介质环境参数的影响
SRB新陈代谢过程中的产物能够改变腐蚀介质中的参数。SRB代谢活动对溶液中的pH值变化有表现为,对数生长期前2 d,SRB新陈代谢产生的H2S和小分子有机酸导致pH值的降低[14]。随后,SRB代谢产生的S2-水解产生的OH-的量增多,导致溶液中的pH值升高。具体反应如下[7]:
SO42+8H→S2+4H2O(1)
2H++S2→H2S(2)
S2+H2O→HS+OH(3)
SRB对溶液体系氧化还原电位Eh的影响是由代谢硫化物的性质决定的[15]。SRB处于对数生长期时,对体系中SO42-的还原能力增强,低价态的S2-数量开始增加,Eh迅速下降[16]。Eh的降低表明被还原出的S2-浓度增大是体系还原能力增强的直接原因[17]。在SRB衰减期和死亡期,SO42-被还原的程度降低。溶液中还原产物S2-发生水解且部分与Fe2+络合成Fe的硫化物,使溶液中的S2-量降低,导致Eh升高。具体反应为:
Fe→Fe2++2e(4)
Fe2++S2→FeS(5)
SRB对溶液电导率的影响表现为:当SRB处于对数生长期时,溶液的电导率升高,这是因为SRB的代谢速度加快能使溶液中离子浓度增加,电导率增大[18]。衰减期和死亡期时,溶液中的营养物质不断消耗,残余的SRB从其他无机化合物中获得能量[19],溶液中的无机化合物被消耗,导致电导率降低。
3.2 SRB生长对微观腐蚀形貌的影响
SEM 结果表明,第7 d时,钢基体表面形成了较致密的微生物腐蚀产物膜。在碱性环境下,SRB与胞外聚合物具有电负性[20],排斥本体溶液中侵蚀性阴离子到达管线钢表面[21],从而管线钢的腐蚀减缓。第14 d时,随着SRB的死亡,微生物膜的电负性消失[22],钢基体表面的腐蚀产物膜出现裂纹,无法阻碍腐蚀性介质接触基体表面,导致腐蚀的继续发生。
EDS能量谱表明,钢基体表面的腐蚀产物元素除了C、O、Fe、P、S外,还有Na、Mg、Ca等无机离子,表明基体表面包含胞外聚合物 (主要成分是核酸、脂类、多糖和蛋白质) 等有机物质[22]。胞外聚合物具有很强的络合能力,能够将多种无机金属离子固定下来[23]。另外,胞外聚合物具有很高的黏性,可以吸附无机矿化物,形成复杂的生物膜[24]。腐蚀产物中的P是因为培养基中的K2HPO4存在所形成的[25]。
3.3 SRB生长对X70钢的电化学行为的影响
EIS结果和极化曲线结果表明,X70钢在含SRB的大庆土壤模拟溶液中的腐蚀行为与SRB的新陈代谢过程有关。第4 d时,SRB处于对数生长期,溶液中的SRB数量最多,但是膜电阻Rf最小。说明此时大量的SRB浮游在溶液中,保护性生物膜尚未形成。SEM结果也证实了这一点。第7 d时,Rf与Rct均为最大值,腐蚀电流密度最小。此时SRB处于衰减期,虽然总体上SRB数量呈下降趋势,但是附着在钢表面的SRB数量增多,使钢表面形成致密的生物膜,增强了X70钢的耐蚀性。10和14 d时的Rf和Rct均为减小趋势且腐蚀电流密度为增大趋势,说明随SRB的衰亡及浸泡时间的增长,钢表面的生物膜不能在金属表面附着,SEM结果表明X70钢表面出现大量裂纹,腐蚀速率增加。
3.4 SRB新陈代谢对X70钢在大庆土壤模拟溶液中的腐蚀行为影响
在大庆土壤环境中,1~4 d时,在对数生长期时SRB菌簇主要游离于溶液中,利用新陈代谢产生的H将介质中的SO42-还原成S2-、H2S及有机酸参与阴极去极化过程[26],导致X70钢发生腐蚀 (反应 (1)、(2)和 (4)。4~10 d时,SRB处于衰减期,SRB从溶液中开始向电极表面附着,钢基体表面覆盖一层致密的微生物膜,抑制基体表面的腐蚀,致使腐蚀速率减小。当SRB进入死亡期,生物膜不能维持完整性,出现明显裂纹,腐蚀性介质直接接触基体表面,X70钢的腐蚀速率增大。此时膜层破损的区域电势较低成为阳极被加速腐蚀,而微生物腐蚀产物膜致密的区域电势较高作为阴极[27,28]。膜层破损的区域与有生物腐蚀产物膜覆盖的区域形成腐蚀原电池促进了腐蚀[28]。
4 结论
(1) SRB在大庆土壤模拟溶液中一个生长周期分为对数生长期 (1~4 d)、衰减期 (4~10 d)、死亡期(>10 d) 3个阶段。
(2) SRB的生长代谢影响了土壤当中的环境参数。pH值在SRB的对数生长期前2 d降低,然后呈整体上升趋势。Eh在对数生长期时降低,在衰减期和死亡期增加。电导率在SRB的对数生长期时增加,在衰减期和死亡期降低。
(3) 在SRB对数生长期,游离的SRB利用介质环境中H将硫酸盐还原成硫化物,促进了X70钢腐蚀的发生;SRB衰减期,致密的微生物膜附着在X70钢的表面,暂时减缓了腐蚀;SRB进入死亡期后,由于生物膜脱落,形成微观腐蚀电池,导致钢基体的腐蚀加剧。
参考文献
[1] Chen X, Li X G, Du C W, et al. Effect of cathodic protection on corrosion of pipeline steel under disbonded coating [J]. Corros. Sci., 2009, 51: 2242
[2] Chen G F, Xie Y J. Application of fault tree analysis in oil and gas pipelines leakage [J]. Contemp. Chem. Ind., 2014, (7): 1342
[2] (陈广芳, 谢禹钧. 事故树分析法在油气输送管道泄漏事故中的应用 [J]. 当代化工, 2014, (7): 1342)
[3] Biezma M V. The role of hydrogen in microbiologically influenced corrosion and stress corrosion cracking [J]. Int. J. Hydrogen Energy, 2001, 26: 515
[4] AlAbbas F M, Williamson C, Bhola S M, et al. Influence of sulfate reducing bacterial biofilm on corrosion behavior of low-alloy, high-strength steel (API-5L X80) [J]. Int. Biodeterior. Biodegrad., 2013, 78: 34
[5] Castaneda H, Benetton X D. SRB-biofilm influence in active corrosion sites formed at the steel-electrolyte interface when exposed to artificial seawater conditions [J]. Corros. Sci., 2008, 50: 1169
[6] Xu D K, Li Y C, Song F M, et al. Laboratory investigation of microbiologically influenced corrosion of C1018 carbon steel by nitrate reducing bacterium Bacillus licheniformis [J]. Corros. Sci., 2013, 77: 385
[7] Chen X, Wang G F, Gao F J, et al. Effects of sulphate-reducing bacteria on crevice corrosion in X70 pipeline steel under disbonded coatings [J]. Corros. Sci., 2015, 101: 1
[8] Song B Q, Chen X, Ma G Y, et al. Effect of SRB on corrosion behavior of X70 pipeline steel in near-neutral pH solution [J]. J. Chin. Soc. Corros. Prot., 2016, 36: 212
[8] (宋博强, 陈旭, 马贵阳等. SRB对X70管线钢在近中性pH溶液中腐蚀行为的影响 [J]. 中国腐蚀与防护学报, 2016, 36: 212)
[9] Wu T Q, Xu J, Yan M C, et al. Synergistic effect of sulfate-reducing bacteria and elastic stress on corrosion of X80 steel in soil solution [J]. Corros. Sci., 2014, 83: 38
[10] Xu J, Sun C, Yan M C, et al. Electrochemical behavior of steel A36 under disbonded coating in the presence of sulfate-reducing bacteria [J]. Mater. Chem. Phys., 2013, 142: 692
[11] Lu X R, Du C W, Li X G, et al. Corrosion behavior of X70 steel in Daqing soils [J]. Corros. Prot., 2008, 29: 503
[11] (鲁新如, 杜翠薇, 李晓刚等. X70钢在大庆两种土壤中的腐蚀行为 [J]. 腐蚀与防护, 2008, 29: 503)
[12] Wang S, Li X G, Huang Y Z, et al. Effect of ferrous ion on sulfate-reducing bacteria influenced corrosion of mild steel [J]. J. Aeronaut. Mater., 2012, 32(1): 51
[12] (汪崧, 李晓刚, 黄一中等. Fe2+对碳钢硫酸盐还原菌腐蚀行为的影响 [J]. 航空材料学报, 2012, 32(1): 51)
[13] Du N, Ye C, Tian W M, et al. 304 stainless steel pitting behavior by means of electrochemical impedance spectroscopy [J]. J. Mater. Eng., 2014, (6): 68
[13] (杜楠, 叶超, 田文明等. 304不锈钢点蚀行为的电化学阻抗谱研究 [J]. 材料工程, 2014, (6): 68)
[14] Kuang F, Wang J, Yan L, et al. Effects of sulfate-reducing bacteria on the corrosion behavior of carbon steel [J]. Electrochim. Acta, 2007, 52: 6084
[15] Li F S, An M Z, Liu G Z, et al. Roles of sulfur-containing metabolites by SRB in accelerating corrosion of carbon steel [J]. Chin. J. Inorg. Chem., 2009, 25: 13
[15] (李付绍, 安茂忠, 刘光洲等. 硫酸盐还原菌的含硫代谢产物在加速碳钢腐蚀中的作用 [J]. 无机化学学报, 2009, 25: 13)
[16] Li F S, An M Z, Liu G Z, et al. Effect of sulfate-reducing bacteria on the pitting corrosion behavior of 18-8 stainless steel [J]. Acta Metall. Sin., 2009, 45: 536
[16] (李付绍, 安茂忠, 刘光洲等. 硫酸盐还原菌对18-8不锈钢点蚀行为的影响 [J]. 金属学报, 2009, 45: 536)
[17] Zhu Y Y, Zheng C B, Li Y T, et al. The change in corrosion parameter with SRB growth in sea mud [J]. Marine Sci., 2006, 30(11): 37
[17] (朱永艳, 郑传波, 李言涛等. 海泥中硫酸盐还原菌数量变化对主要腐蚀环境因子的影响 [J]. 海洋科学, 2006, 30(11): 37)
[18] Chen X, Gao F J, Song W Q, et al. Effects of CO2 on SRB influenced corrosion behavior of X70 steel in near-neutral pH solution [J]. Corros. Sci. Prot. Technol., 2017, 29: 103
[18] (陈旭, 高凤娇, 宋武琦等. CO2对X70钢在近中性pH值溶液中硫酸盐还原菌腐蚀行为的影响 [J]. 腐蚀科学与防护技术, 2017, 29: 103)
[19] Usher K M, Kaksonen A H, Bouquet D, et al. The role of bacterial communities and carbon dioxide on the corrosion of steel [J]. Corros. Sci., 2015, 98: 354
[20] Wu T Q, Ding W C, Zeng D C, et al. Microbiologically induced corrosion of X80 pipeline steel in an acid soil solution: (I) Electrochemical analysis [J]. J. Chin. Soc. Corros. Prot., 2014, 34: 346
[20] (吴堂清, 丁万成, 曾德春等. 酸性土壤浸出液中X80钢微生物腐蚀研究: (Ⅰ) 电化学分析 [J]. 中国腐蚀与防护学报, 2014, 34: 346)
[21] Liu T, Zhang Y F, Chen X, et al. Effect of SRB on corrosion behavior of X70 steel in a simulated soil solution [J]. J. Chin. Soc. Corros. Prot., 2014, 34: 112
[21] (刘彤, 张艳飞, 陈旭等. SRB对X70钢在土壤模拟溶液中腐蚀行为的影响 [J]. 中国腐蚀与防护学报, 2014, 34: 112)
[22] Sun C, Xu J, Wang F H. Interaction of sulfate-reducing bacteria and carbon steel Q235 in biofilm [J]. Ind. Eng. Chem. Res., 2011, 50: 12797
[23] Braissant O, Decho A W, Dupraz C, et al. Exopolymeric substances of sulfate-reducing bacteria: Interactions with calcium at alkaline pH and implication for formation of carbonate minerals [J]. Geobiology, 2007, 5: 401
[24] Liu H W, Liu H F, Qin S, et al. Investigation of biomineralization induced by sulfate reducing bacteria in sewage gathering pipelines in oilfield [J]. Corros. Sci. Prot. Technol., 2015, 27: 7
[24] (刘宏伟, 刘宏芳, 秦双等. 集输管线硫酸盐还原菌诱导生物矿化作用调查 [J]. 腐蚀科学与防护技术, 2015, 27: 7)
[25] Alabbas F M, Williamson C, Bhola S M, et al. Influence of sulfate reducing bacterial biofilm on corrosion behavior of low-alloy, high-strength steel (API-5L X80) [J]. Int. Biodeterior. Biodegrad., 2013, 78: 34
[26] Zheng Q, Li J, Du Y L, et al. Influence of sulfate reducing bacteria on corrosion behavior of HSn70-1A alloy [J]. J. Chin. Soc. Corros. Prot., 2008, 28: 38
[26] (郑强, 李进, 杜一立等. 硫酸盐还原菌对HSn70-1A铜合金电化学腐蚀行为的影响 [J]. 中国腐蚀与防护学报, 2008, 28: 38)
[27] Song W Q. Microbial corrosion of 2205 duplex stainless steel in oilfield-produced water [J]. Int. J. Electrochem. Sci., 2018, 13: 675
[28] Zhou P, Qin S, Ye Q, et al. Monitoring and controlling growth of biofilm on carbon steel surface in oilfield sewage [J]. Mater. Prot., 2013, 46(11): 20
[28] (周平, 秦双, 叶琴等. 油田污水中碳钢表面生物膜的生长监测与控制 [J]. 材料保护, 2013, 46(11): 20)
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414





