摘要
以乌洛托品、溴己烷为主要原料,甲醇为溶剂,合成了一种乌洛托品季铵盐缓蚀剂,采用失重法研究了季铵盐缓蚀剂在15% (质量分数) HCl溶液中的缓蚀性能及复配性能,并采用量子化学计算对缓蚀剂机理进行分析,通过红外光谱、SEM对腐蚀后表面进行分析。结果表明,季铵盐缓蚀剂具有良好的缓蚀性能,在15%HCl、90 ℃下,加量0.5% (质量分数) 时,缓蚀率达98.41%,并且与聚乙二醇、KI、丙炔醇复配后协同增效效果较好;量子化学计算表明该季铵盐缓蚀剂分子活性主要分布在分子环上,与乌洛托品相比具有更小的能隙,在Fe表面也具有更大吸附能,因此乌洛托品季铵盐活性更高。表面分析实验进一步验证了该缓蚀剂分子在QT-800钢片表面形成一层吸附膜。
关键词: 合成 ; 乌洛托品 ; 缓蚀剂 ; 复配 ; 量子化学计算
Abstract
A new type of urotropine quaternary ammonium salt as corrosion inhibitor was synthesized through nucleophilic reaction with urotropine and bromohexane as raw materials, while methanol as solvent. Then, the corrosion inhibition effect of quaternary ammonium salt for QT-800 steel in 15% (mass fraction) HCl solution was assessed by mass loss measurements, IR spectrometer and SEM. The mechanism of corrosion inhibition was studied by quantum chemical density functional theory. The results indicated that the quaternary ammonium salt has good corrosion inhibition performance, when urotropine quaternary ammonium salt of 0.5% (mass fraction) was added into 15%HCl solution at 90 ℃, the inhibition efficiency for QT-800 steel could reach up to 98.41%. The complexes of the urotropine quaternary ammonium salt with polyethylene glycol, potassium iodide and propynol were prepared respectively, and they all showed good performance in corrosion inhibition. Quantum chemical parameters indicates that the chemical activity of the urotropine quaternary ammonium salt is mainly distributed on the molecular ring, which has a smaller energy gap than the urotropine, and a larger adsorption energy on the iron surface. Therefore, the reactivity of urotropine quaternary ammonium salt is higher than that of urotropine. The results of IR spectrum and SEM analysis reveal that the urotropine quaternary ammonium salt molecules could adsorb on the surface of QT-800 steel during the corrosion test in HCl solution.
Keywords: synthesis ; urotropine ; corrosion inhibitor ; complex ; quantum chemical calculation
缓蚀剂又称腐蚀抑制剂,少量地添加到腐蚀环境中时会在金属与介质的界面上阻滞腐蚀进行[1]。由于缓蚀剂的用量很少,基本上不改变介质环境的性质,不需要太多的辅助设备,操作简单方便、成本低、效果好,因此,使用缓蚀剂是一种适应性强、经济有效的金属防腐措施[2,3,4,5]。目前咪唑啉季铵盐、喹啉季铵盐、吡啶季铵盐、曼尼希碱类缓蚀剂在国内应用较为广泛,通常复配以金属盐、表面活性剂、丙炔醇等来提高缓蚀效果[6,7,8,9,10],这些缓蚀剂分子是由两种极性不同的基团构成,含有O、N、S等元素的极性基团可以吸附在金属表面改变其电荷状态和界面性质,含C、H的非极性基团在金属表面形成疏水性保护膜,从而减缓腐蚀速率[11,12]。
乌洛托品无毒、无异味,是一种常用的环境友好型缓蚀剂,但是其缓蚀效果并不明显,对金属材料还具有一定腐蚀作用[13,14],根据德尔宾反应可知在乌洛托品分子环上能够引入碳链,增强其缓蚀性能,有效抑制金属腐蚀。为此,本文以乌洛托品与溴己烷为原料合成了乌洛托品季铵盐,并对其复配性能进行研究。应用量子化学计算对缓蚀机理进一步分析,通过红外谱图、扫描电镜 (SEM) 对腐蚀后试片进行表征,通过实验与理论相结合的方式分析合成缓蚀剂性能。
1 实验方法
实验用乌洛托品、溴己烷、碳酸氢钠、甲醇、盐酸、OP-10、平平加 (O-20)、聚乙二醇 (400)、吐温-80、丙炔醇、碘化钾试剂均为分析纯。将合成缓蚀剂分别与OP-10、平平加 (O-20)、聚乙二醇 (400)、吐温-80、丙炔醇、碘化钾进行复配。固定盐酸15% (质量分数),腐蚀温度为90 ℃、腐蚀时间为4 h,考察助剂类型及用量对复配效果的影响,其中复配实验缓蚀剂加量均为0.5%。
实验中所使用试片为QT-800钢,规格50 mm×10 mm×3 mm,符合SY/T5405-1996的要求,在油管上取样做化学成分分析,成分 (质量分数,%) 为:C 0.15,Mn 0.77,P 0.013,S 0.002,Si 0.34,Cr 0.59,Ni 0.17,Cu 0.26,Mo≦0.23,Fe余量
在装有回流冷凝管的三口烧瓶中,加入适量无水甲醇溶剂,打开DF-101D集热式恒温加热磁力搅拌器并加热,称取28 g乌洛托品与适量碳酸氢钠催化剂加入甲醇溶剂中,然后用恒压滴液漏斗向甲醇中缓慢滴入49.5 g溴己烷[15]。滴加完毕后在50 ℃条件下反应7 h,冷却反应体系,待有白色固体析出时过滤即得固体粗产品,然后将产品在60 ℃条件下用无水甲醇溶液洗涤,过滤烘干即得产品。反应方程式如下:
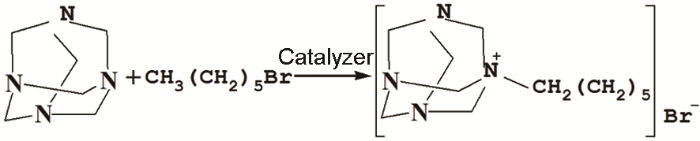
参照SY/T 5405-1996,用静态挂片失重法测定QT-800钢片在加有缓蚀剂的盐酸中的腐蚀速率。首先在反应釜中配制好腐蚀介质,加入不同量缓蚀剂或复配缓蚀剂,然后将钢片放入反应釜中密封,在一定温度下腐蚀4 h,对比腐蚀后钢片状态及计算腐蚀速率。
使用Material Studio软件包中Visualizer模块构建乌洛托品与合成缓蚀剂的分子结构;采用Dmol3模块,运用广义梯度近似GGA/PBE方法,在DNP基组水平对分子进行优化,收敛精度为Fine,并在同一基组水上计算各分子的前线轨道能量;采用Forcite模块,用COMPASS力场模拟在Fe (100) 面的行为,模拟在298 K,正则系统 (NVT) 下进行,时间不长1 fs,模拟时间500 ps,缓蚀剂分子在Fe表面的吸附能 (Eadsorption) 由下公式算出:
其中,Eadsorption表示缓蚀剂分子在Fe表面的吸附能,Etotal是一个缓蚀剂分子和金属表面形成的体系的总能量,Einhibitor和Esurface分别为缓蚀剂分子的能量与为吸附缓蚀剂分子时金属表面的能量。
采用S-4800型SEM对试样在不同溶液中腐蚀后的表面进行SEM微观形貌分析。利用Nicolet 6700型红外光谱仪对加入季铵盐缓蚀剂后腐蚀的QT-800钢片表面进行表征。
2 结果与讨论
2.1 缓蚀剂性能及评价
合成缓蚀剂分子外观呈淡黄色,具有微苦杏仁味,在25 ℃条件下,测得密度为1.16 g·cm-3,在水中溶解度为15.43 g/100 g。
固定盐酸质量浓度为15%,腐蚀时间为4 h,分别在60和90 ℃下按照实验方法测定不同缓蚀剂加量对腐蚀速率的影响,实验结果见表1。
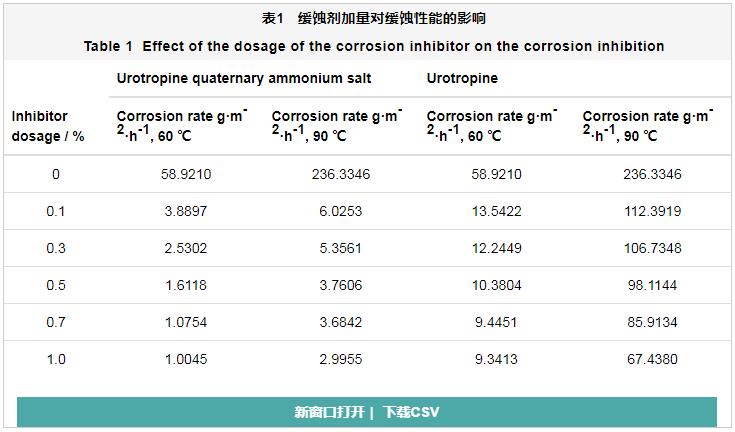
从表1可以看出,随缓蚀剂加量的增大腐蚀速率逐渐降低,随温度升高腐蚀速率明显加快。合成的乌洛托品季铵盐缓蚀剂较乌洛托品具有更好的缓蚀性能,这是因为合成缓蚀剂的氮正离子可以有效吸附在钢片表面,而缓蚀剂分子的疏水碳链可以均匀分布吸附点周围,从而有效阻止H+与金属表面的接触,提高了其缓蚀性能。当合成缓蚀剂加量为0.5%时,腐蚀速率均达到一级指标;随着季铵盐缓蚀剂加量的升高,腐蚀速率持续下降,但降低幅度逐渐减小,这是因为缓蚀剂加量越高,缓蚀剂分子在钢表面覆盖率越高,腐蚀速率越低,直到缓蚀剂分子达到吸附与脱附的动态平衡,腐蚀速率趋于平稳。
2.2 缓蚀剂的复配性能评价
2.2.1 缓蚀剂与表面活性剂复配研究
表面活性剂的加入可以改变金属表面的润湿性,且具有分散作用,可以提高缓蚀剂在酸液中的分散性及吸附性能,从而提高缓蚀效果。由图1可知,随着表面活性剂加量的增加,腐蚀速率先降低后增大,聚乙二醇相比其他3种表面活性剂具有更好协同作用。加入适量聚乙二醇可以明显的降低腐蚀速率,与仅加入0.5%缓蚀剂相比较,加入0.008%~0.01%的聚乙二醇可使腐蚀速率由3.76 g·m-2·h-1降至2.1 g·m-2·h-1附近,这表明表面活性剂的加入,提高了缓蚀剂的缓蚀效果。继续增大表面活性剂加量,腐蚀速率增大,这是因为表面活性剂在钢片表面也具有较强吸附能力,加量过高与缓蚀剂分子形成竞争吸附,减弱了缓蚀剂的吸附性能,使其不能形成稳定的吸附保护膜,从而降低缓蚀效果,因此表面活性剂存在一个最佳用量。
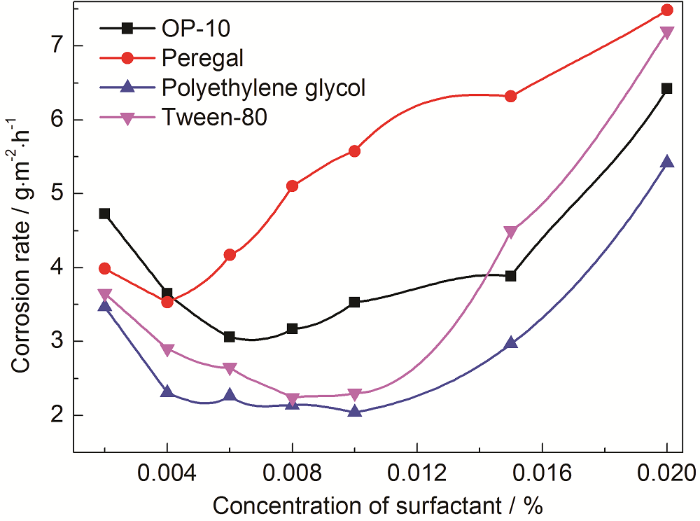
图1 表面活性剂加量与腐蚀速率的关系
Fig.1 Relationship between the mass fraction of surfactant and corrosion rate
2.2.2 缓蚀剂与增效剂复配研究
在一定条件下加入适量缓蚀增效剂,可以进一步提高缓蚀效果。因此,实验选取常用两种增效剂 (丙炔醇、KI),研究两者对缓蚀剂增效作用。由图2可知,随着丙炔醇、KI的加入,试片腐蚀速率逐渐降低,然后趋于平稳,特别是丙炔醇的加入可使腐蚀速率降至1 g·m-2·h-1以下,这是因为丙炔醇分子含有C≡C,可以吸附在金属表面没有吸附缓蚀剂的空白点,与缓蚀剂形成协同作用,降低腐蚀速率。
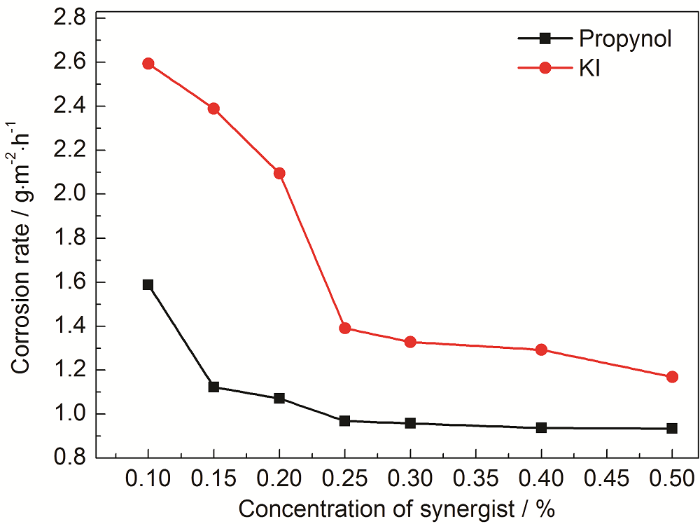
图2 增效剂加量与腐蚀速率的关系
Fig.2 Relationship between the mass fraction of synergist and corrosion rate
2.2.3 缓蚀剂与表面活性剂、增效剂复配效果评价
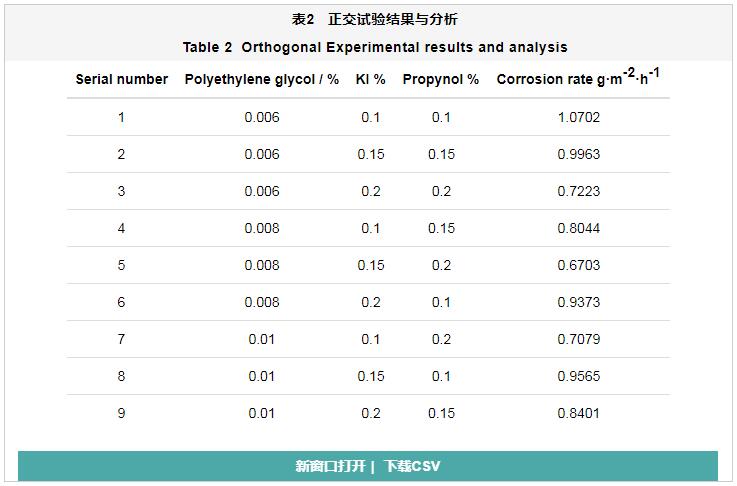
由以上实验可知,在合适的加量下,合成缓蚀剂与聚乙二醇、KI、丙炔醇均有良好缓蚀协同作用,因此实验进一步研究合成缓蚀剂与聚乙二醇、KI、丙炔醇综合复配效果,实验条件与以上复配实验相同,分别对聚乙二醇、KI、丙炔醇三因素取三个水平,进行正交试验,正交试验结果如表2所示。由表2可知,将聚乙二醇、KI、丙炔醇共同与缓蚀剂复配后的缓蚀效果比单独复配效果要好,腐蚀速率可以降至1 g·m-2·h-1以下,特别是在聚乙二醇加量0.008%,KI加量0.15%,丙炔醇加量0.2%时,腐蚀速率低至0.6703 g·m-2·h-1。通过正交试验分析也可看出丙炔醇对复配缓蚀效果影响最大,聚乙二醇次之,因此想要更好的控制腐蚀速率,首先需要考虑丙炔醇加量,但是由于丙炔醇价格相对较高,所以对于具体问题还需通过实验研究才能够达到既能控制腐蚀速率又能节约成本的要求。
2.3 量子化学分析
2.3.1 缓蚀剂前线轨道分布分析
在分子几何优化的基础上,利用密度泛函理论对乌洛托品季铵盐与乌洛托品各种量化参数进行计算。根据前线轨道理论可知,分子EHOMO越大,分子最外层电子越易摆脱原子核的束缚,越易提供电子;ELUMO与分子的电子亲和能密切相关,分子ELUMO越小,分子越易接受电子,EHOMO与ELUMO能量差 (ΔE) 反应了分子稳定性,ΔE越小越易参与化学反应[16]。由图3可知,乌洛托品与乌洛托品季铵盐缓蚀剂两种分子的HOMO和LUMO具有相同的分布中心,主要离域在分子环上,从而使分子环优先吸附,这种分布既有利于金属表面空的d轨道接受缓蚀剂分子所提供的电子形成配位键,也可使缓蚀剂分子利用其反键轨道接受来自金属表面的电子而形成反馈键,使缓蚀剂分子在金属表面形成稳定吸附。另外由于乌洛托品季铵盐ELUMO低于乌洛托品ELUMO,所以铁原子易提供电子给乌洛托品季铵盐,并且乌洛托品季铵盐的轨道能量差 (ΔE=6.072 eV) 小于乌洛托品轨道能量差 (ΔE=6.127 eV),所以合成的乌洛托品季铵盐缓蚀剂更具良好的缓蚀性能。
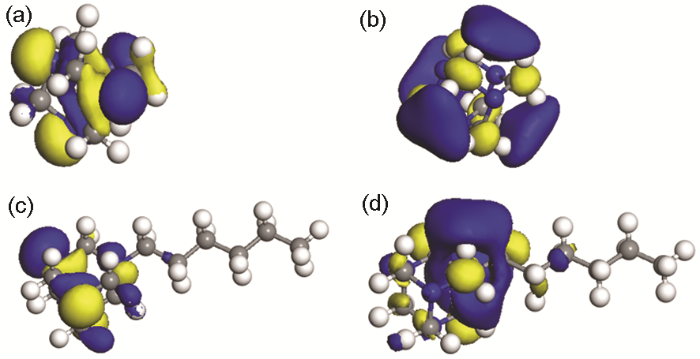
图3 最高占有轨道及最低空轨道的0.03 a.u.等值面图形
Fig.3 HOMO and LUMO isosurfaces with a value of 0.03 a.u. for urotropine (a, b) and urotropine quaternary amm-onium salts (c, d): (a) EHOMO=-5.621 eV, (b) ELUMO=0.506 eV, (c) EHOMO=-9.495 eV, (d) ELUMO=-3.423 eV
2.3.2 分子动力学分析
采用分子动力学,模拟缓蚀剂分子在Fe(100) 晶面真空环境下的吸附行为并计算吸附能,吸附能 (kcal·mol-1) 计算结果分别为:乌洛托品45.708,乌洛托品季铵盐90.976,H2O 6.150,HCl 11.891。缓蚀剂分子吸附平衡状态如图4所示。吸附能的大小可以表明吸附系统的稳定性,吸附能越高说明缓蚀剂越易吸附在铁表面,吸附也越稳定,缓蚀效率也越高[17,18,19,20]。由表2数据可知:乌洛托品季铵盐具有最高吸附能,因此具有更好的缓蚀性能,另外乌洛托品季铵盐吸附能是乌洛托品两倍,且吸附能均大于水分子及盐酸分子在Fe表面的吸附能,因此能够水分子驱吸附在Fe表面,从而抑制腐蚀作用。
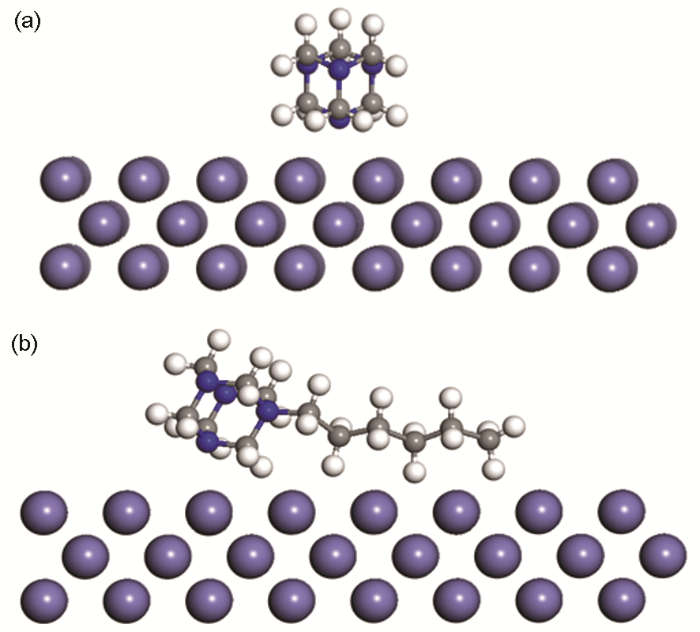
图4 分子动力学模拟中缓蚀剂分子在Fe表面达到平衡的状态图
Fig.4 Molecular dynamics simulation of corrosion inhibitor molecules in the balance of Fe surface state diagram: (a) Urotropine, (b) Urotropine quaternary ammonium salt
由图4可知乌洛托品季铵盐缓蚀剂分子达到吸附平衡时,几乎都以平躺方式吸附在Fe表面,这种吸附方式可以使缓蚀剂分子与Fe的d轨道交盖,有效增大缓蚀剂分子在Fe表面的覆盖面积,提高缓蚀效果[21,22]。从以上分析可知,乌洛托品季铵盐缓蚀剂可以在试片表面发生吸附形成保护膜,增加试片表面缓蚀剂的覆盖率,提高了缓蚀效果。
2.4 QT-800钢片表面分析
2.4.1 FT-IR分析
为了验证季铵盐缓蚀剂在金属表面是否发生吸附作用,对加入季铵盐缓蚀剂后腐蚀的QT-800钢片表面表征红外谱图如图5所示。由图5可知,乌洛托品与溴己烷的特征峰在腐蚀后钢表面的红外谱图中都出现,而图5中3400~ 3500 cm-1处为吸附在钢片表面水化层的—OH振动峰;与溴己烷对比可知,2960 cm-1处是季铵盐缓蚀剂疏水碳链中的C—H的伸缩振动吸收峰,这也与溴己烷的饱和C—H链吸收峰相对应;而图5c中,1490 cm-1为C—N+—C的季氮特征峰,1270 cm-1处为季铵盐环中C—N伸缩振动吸收峰,648 cm-1处为C—N弯曲振动峰,这也与图5b中乌洛托品的红外特征峰相对应。这些官能团的出现表明季铵盐缓蚀剂吸附在钢片表面,也证明合成化合物为乌洛托品季铵盐。
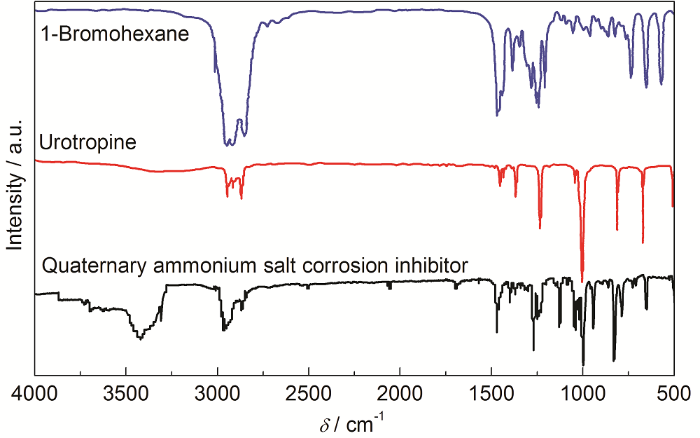
图5 腐蚀后钢片表面与乌洛托品、溴己烷的红外谱图
Fig.5 FT-IR spectrums of QT-800 steel surface after immersion with quaternary ammonium salt corrosion inhibitor, urotropine, and 1-Bromohexane
2.4.2 SEM形貌分析
为进一步了解季铵盐缓蚀剂的缓蚀效果,对QT-800钢片在不同溶液中腐蚀后的表面进行SEM微观形貌分析如图6所示 (溶液温度90 ℃,腐蚀时间4 h)。对比图6中试片表面的状态可知,原始试片表面光滑均匀;未加缓蚀剂的QT-800试片在15%HCl溶液中发生剧烈的溶解腐蚀反应,钢片表面呈现蜂窝状,且有大量点蚀坑,局部腐蚀较为严重;而当加入季铵盐缓蚀剂与聚乙二醇、丙炔醇的复配剂后,钢片表面均匀覆盖一层腐蚀产物膜,无明显点蚀现象,试片腐蚀得到抑制,这表明季铵盐缓蚀剂具有良好的缓蚀性能,能够有效吸附在金属表面,减缓金属表面腐蚀。

图6 QT-800钢片在有、无缓蚀剂的15%HCl溶液中腐蚀4 h后的表面形貌
Fig.6 Surface morphologies of QT-800 steel in 15%HCl without corrosion (a), without inhibitor (b) with inhibitor and polyethylene glycol (c) and with inhibitor and propynol (d)
3 结论
(1) 乌洛托品季铵盐在HCl腐蚀介质中具有良好的缓蚀性能。在15%HCl中加入0.5%季铵盐缓蚀剂,60 ℃时腐蚀速率为1.6118 g·m-2·h-1,90 ℃时腐蚀速率为3.7606 g·m-2·h-1,缓蚀性能明显优于乌洛托品。
(2) 乌洛托品季铵盐与聚乙二醇、丙炔醇、碘化钾复配时,在合适的复配配比下具有良好的协同效果,可使腐蚀速率控制在1 g·m-2·h-1以下。
(3) 乌洛托品季铵盐与乌洛托品相比具有较低能隙,因此乌洛托品季铵盐活性相对乌洛托品活性更高;动力学模拟可知乌洛托品季铵盐吸附能是乌洛托品2倍,且吸附能远大于水分子吸附能。
(4) FT-IR和SEM分析验证了乌洛托品季铵盐能够有效吸附金属表面,抑制金属的腐蚀。
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。
相关文章

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414
点击排行
PPT新闻
“海洋金属”——钛合金在舰船的
点击数:7130
腐蚀与“海上丝绸之路”
点击数:5741





